Liệu pháp CAR-T có độ nhạy cao với CD70 mang lại triển vọng loại bỏ hoàn toàn tế bào ung thư trong khối u đặc
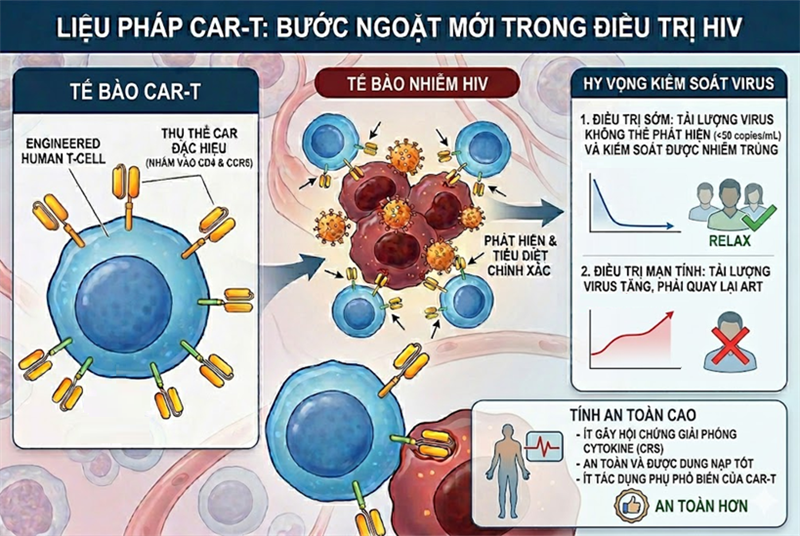
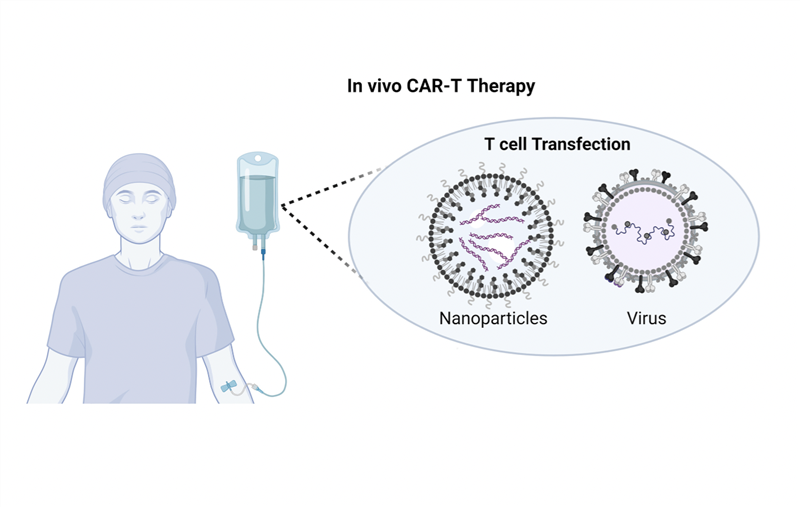
Liệu pháp tế bào T mang thụ thể kháng nguyên khảm (chimeric antigen receptor T-cell, CAR-T) đã tạo nên bước ngoặt trong điều trị nhiều bệnh ung thư máu. Những tế bào T mang cấu trúc CAR được thiết kế để hướng đích một thụ thể xác định trên tế bào ác tính, nhờ đó phát hiện đặc hiệu và tiêu diệt hiệu quả những tế bào đó. Tế bào ung thư máu thường biểu hiện mạnh CD19, nên dễ dàng bị phát hiện bởi tế bào CAR-T mang CAR đặc hiệu với đích này.
Tuy nhiên, liệu pháp CAR-T gặp nhiều hạn chế khi ứng dụng trong các bệnh ung thư dạng u đặc, chiếm tới hơn 85% tổng số ca ung thư. Thách thức đầu tiên là xác định đích phân tử biểu hiện ở hầu hết các tế bào u, giống như CD19 ở các tế bào máu ác tính. Trong các khối u đặc, tế bào ung thư đa dạng hơn, và không có một phân tử duy nhất nào có thể đóng vai trò là mục tiêu duy nhất cho liệu pháp tế bào. Mặc dù liệu pháp nhắm vào những đích phân tử biểu hiện ở lượng lớn tế bào ác tính, nhưng bệnh nhân không thể được chữa khỏi nếu chỉ loại bỏ phần nhỏ, hay thậm chí là 90% tế bào ung thư, mà cần tiêu diệt đến tế bào cuối cùng.
Trước đây, CD70 được xác định là biểu hiện ở nhiều mức độ khác nhau giữa các tế bào trong khối u. Gần đây, người ta phát hiện CD70 được biểu hiện ở hầu hết các tế bào ung thư trong khối u đặc, với mức độ thay đổi rất nhiều, ít nhất có một vài phân tử trên bề mặt của chúng. Nhờ đó, CD70 có thể hoạt động như một tín hiệu dẫn đường cho liệu pháp CAR-T.
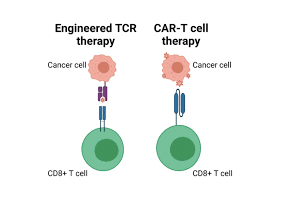
Mặc dù vậy, các tế bào CAR-T thông thường chỉ có thể phát hiện những tế bào ác tính có hàm lượng cao phân tử mục tiêu, dẫn đến liệu pháp CAR-T nhắm đích CD70 không mang lại hiệu quả cao khi điều trị các khối u đặc. Các nhà khoa học tại Đại học Columbia (Hoa Kỳ) đã phát triển một loại liệu pháp tế bào mới, gọi là HIT (viết tắt từ “HLA-independent T cell” – tế bào T độc lập với HLA), được lập trình giống như tế bào CAR-T, nhưng có độ nhạy của tế bào T tự nhiên, có thể phát hiện các tế bào ung thư chỉ có số lượng phân tử mục tiêu cực kỳ nhỏ. Các tế bào HIT được thiết kế nhắm đích CD70 đã loại bỏ hoàn toàn các khối u ở chuột mắc ung thư thận, tuyến tụy và buồng trứng, trong khi các tế bào CAR-T thông thường chỉ loại bỏ được một phần. Các tế bào HIT không tác động đến các tế bào khỏe mạnh vì hầu hết chúng không biểu hiện CD70.
Tế bào HIT nhắm đích CD70 cũng có tiềm năng với nhiều loại u đặc khác, bao gồm u nguyên bào thần kinh đệm, ung thư tuyến tụy, ung thư phổi,… Mặc dù các khối u đặc gây nhiều trở ngại khác với liệu pháp tế bào, tuy nhiên khó khăn lớn nhất vẫn là sự thoát kháng nguyên – khi các tế bào ung thư chọn lọc theo hướng giảm biểu hiện kháng nguyên đích xuống ngưỡng rất thấp để trốn tránh tế bào CAR-T. Vì vậy, tế bào HIT có độ nhạy cao được hy vọng sẽ phát hiện và tiêu diệt toàn bộ các tế bào ác tính mặc dù chúng biểu hiện kháng nguyên ở mức độ rất thấp.
Những kết quả trên cho thấy CD70 được biểu hiện ở hầu hết các tế bào ung thư trong khối u đặc, mặc dù có thể với mức rất thấp. Đây có thể là một mục tiêu tiềm năng cho liệu pháp CAR-T, nhưng chỉ khi sử dụng thụ thể nhắm đích với độ nhạy cao (ví dụ như tế bào HIT). Với những thành công trong nghiên cứu tiền lâm sàng, các nhà khoa học đang tiến tới triển khai thử nghiệm lâm sàng liệu pháp này đối với một số loại ung thư dạng u đặc.
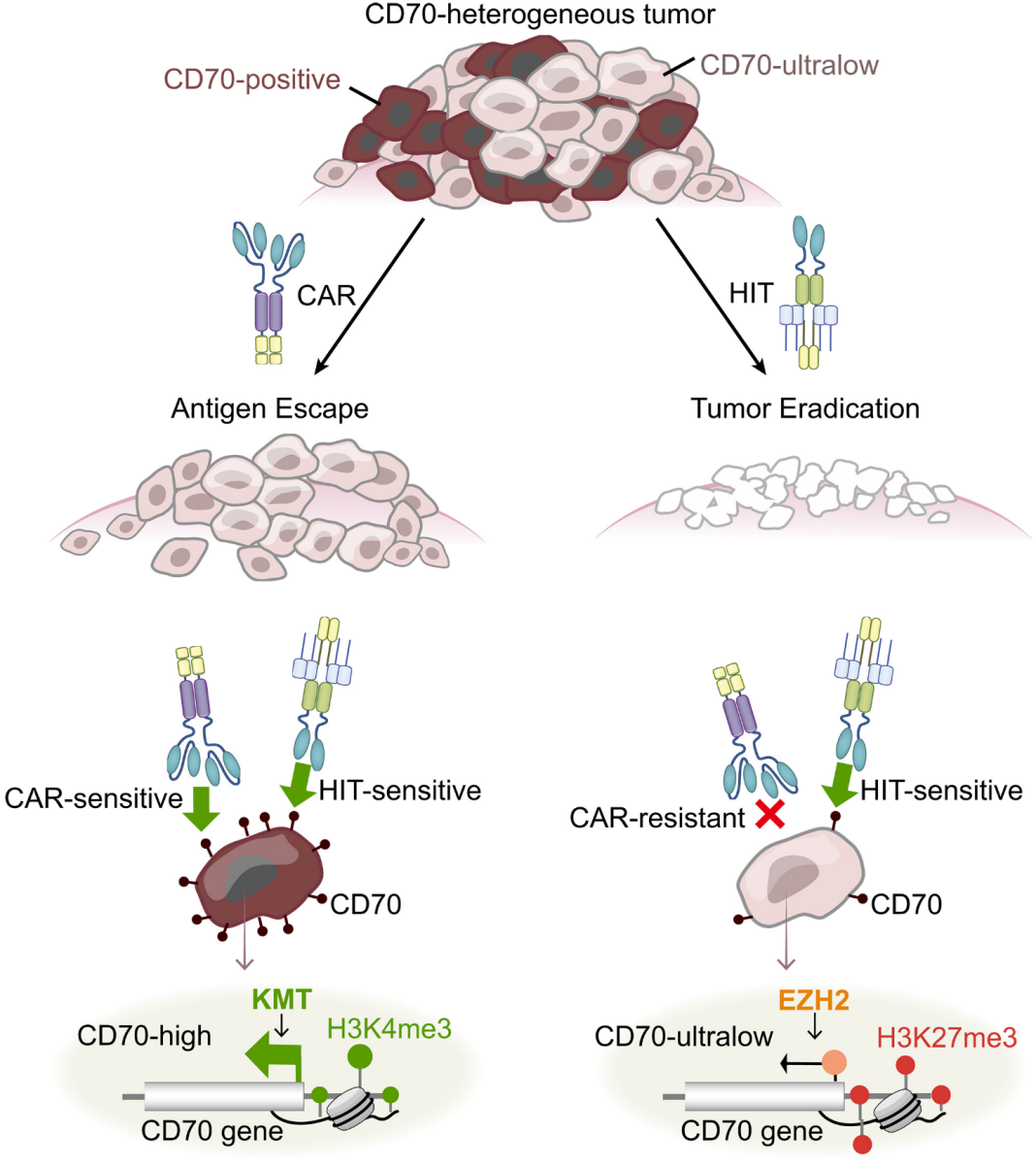
Trong các khối u đặc, tế bào CAR-T nhắm đích CD70 tiêu diệt các tế bào ung thư dương tính với thụ thể này, nhưng không loại bỏ hoàn toàn được chúng. Các tế bào ung thư thoát điều trị dường như âm tính với CD70, thực ra biểu hiện thụ thể này ở mức độ cực thấp mà các xét nghiệm thông thường và các tế bào CAR thường được sử dụng không thể phát hiện. Tuy nhiên, liệu pháp HIT có độ nhạy cao hơn có thể nhận biết và loại bỏ hoàn toàn các tế bào trên, đạt được sự tiêu diệt khối u hoàn toàn. Sự điều hòa biểu hiện CD70 do cơ chế di truyền ngoại gen (epigenetic), với sự trimethyl hóa lysine 27 trên histon H3 (H3K27me3).
TÀI LIỆU THAM KHẢO
Hanina S. A., et al. (2026). Sensitive CAR T cells redefine targetable CD70 expression in solid tumors. Science, 391(6788), 896-905. https://doi.org/10.1126/science.adv7378