YÊU CẦU, QUY ĐỊNH
Quy định về sàng lọc người hiến mẫu để tạo ra sản phẩm Liệu pháp tế bào tại Hoa Kỳ và châu Âu
Các quy định chung về sáng lọc người hiến mẫu
21/01/2026

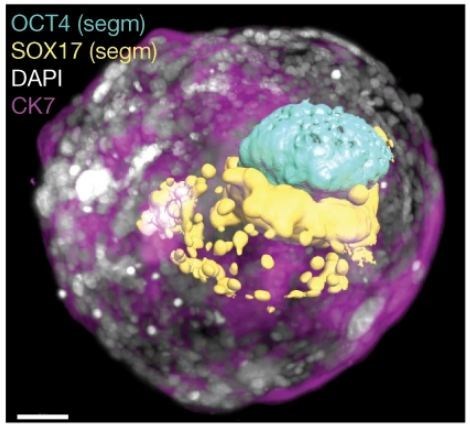
Nhật Bản phê duyệt việc tạo phôi người từ tế bào gốc để phục vụ nghiên cứu
Theo thông tin từ Japan Today, ngày 24 tháng 7 năm 2025, một hội đồng của chính phủ Nhật Bản đã nhất trí cho phép tạo ra phôi người bằng cách sử dụng trứng hoặc tinh trùng có nguồn gốc từ tế bào gốc đa tiềm năng, nhưng chỉ nhằm mục đích nghiên cứu các vấn đề như vô sinh và bệnh di truyền.
21/01/2026
Cập nhật 2025 về hướng dẫn nghiên cứu tế bào gốc của Hiệp hội Quốc tế về Nghiên cứu Tế bào gốc (ISSCR)
Ngày 11 tháng 8 năm 2025, Hiệp hội Quốc tế về Nghiên cứu Tế bào gốc (International Society for Stem Cell Research – ISSCR) đã công bố bản cập nhật Guidelines for Stem Cell Research and Clinical Translation năm 2021.
21/01/2026

FDA trì hoãn việc phê duyệt liệu pháp tế bào và gen do các vấn đề về quy trình sản xuất và kiểm soát sản phẩm
Giai đoạn gần đây, Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (US Food and Drug Administration – FDA) đã liên tục từ chối hoặc trì hoãn phê duyệt các liệu pháp tế bào và gen.
21/01/2026

Hiệp hội Quốc tế về Nghiên cứu Tế bào gốc (ISSCR) phát hành hướng dẫn phát triển các liệu pháp tế bào có nguồn gốc từ tế bào gốc đa tiềm năng.
Ngày 09 tháng 10 năm 2025, ISSCR công bố phát hành “Những thực hành tốt nhất để phát triển các liệu pháp tế bào có nguồn gốc từ tế bào gốc đa tiềm năng” nhằm đẩy nhanh quá trình chuyển đổi loại liệu pháp này sang các thử nghiệm lâm sàng và mục đích sử dụng thương mại.
21/01/2026
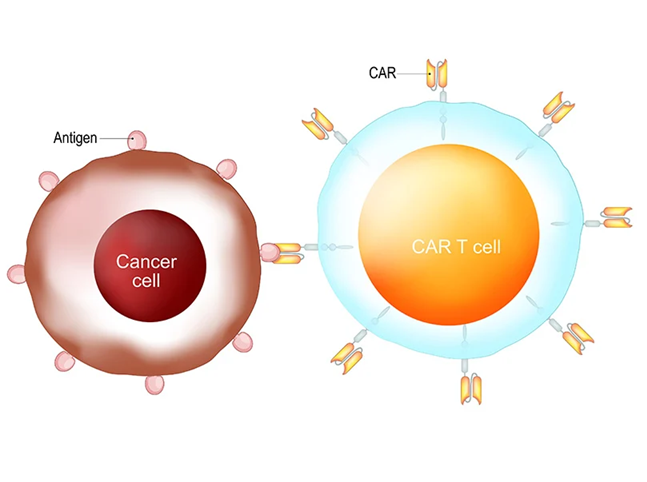
FDA sẽ siết chặt điều kiện cấp phép đối với liệu pháp tế bào CAR-T
Các quan chức cấp cao tại Trung tâm Nghiên cứu và Đánh giá Sinh học (Center for Biologic Research and Evaluation – CBER) thuộc Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (the US Food and Drug Administration – US FDA) cho biết cơ quan này nhìn chung sẽ yêu cầu các thử nghiệm lâm sàng phải phân nhóm ngẫu nhiên có đối chứng (randomized controlled trial) để hỗ trợ việc phê duyệt các liệu pháp CAR-T điều trị ung thư, ngoại trừ một số trường hợp nhất định như các nhóm bệnh nhân hiếm gặp hoặc tái phát nhiều lần hoặc kháng trị.
21/01/2026
FDA công bố kế hoạch loại bỏ dần thử nghiệm trên động vật - Một trong những điểm nhấn đáng chú ý nhất năm 2025 của công nghệ tế bào
Tháng 04/2025, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (the Food and Drug Administration – FDA) đã công bố một lộ trình mới nhằm thay thế thử nghiệm trên động vật trong quá trình phát triển thuốc mới bằng các phương pháp phù hợp hơn với con người. Mục tiêu là cải thiện độ an toàn của thuốc, đẩy nhanh quá trình đánh giá, rút ngắn thời gian phát triển thuốc, giảm chi phí nghiên cứu,… FDA mong muốn thử nghiệm trên động vật là ngoại lệ chứ không phải quy chuẩn trong vòng 3–5 năm tới.
21/01/2026

ISCT nói gì và quy ước thế nào về tế bào gốc trung mô/tế bào đệm trung mô (MSC)
ISCT là tên viết tắt của Hiệp hội Quốc tế về Liệu pháp Tế bào và Gen (International Society for Cellular Therapy), họ có riêng một Ủy ban về MSC (ISCT’s MSC committee).
19/01/2026

Tổ chức AABB và Tiêu chuẩn AABB
Tiêu chuẩn AABB là tiêu chuẩn quốc tế cao nhất mà các ngân hàng sinh học và các cơ sở ứng dụng liệu pháp tế bào hướng đến hiện nay. Tiêu chuẩn AABB kết hợp cả tiêu chuẩn hệ thống kỹ thuật và chất lượng để đảm bảo xem xét mọi khía cạnh của đơn vị được cấp chứng nhận.
19/01/2026







