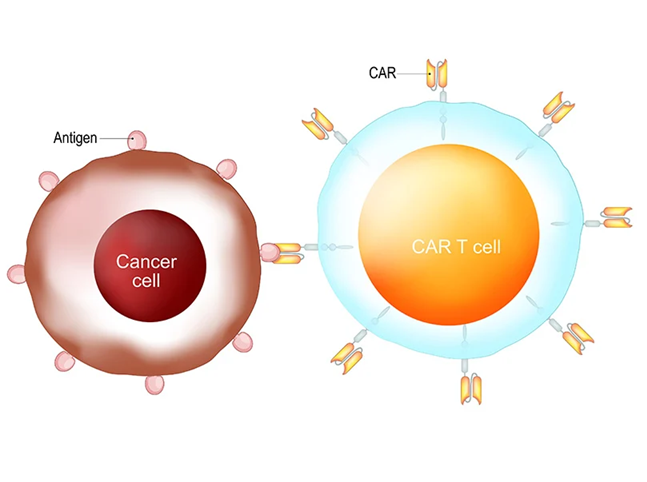
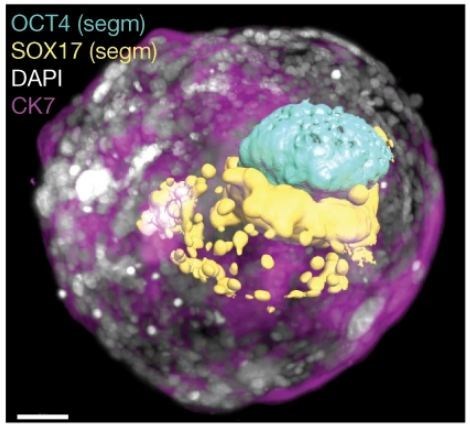
Quy định về sàng lọc người hiến mẫu để tạo ra sản phẩm Liệu pháp tế bào tại Hoa Kỳ và châu Âu
1. Quy định chung
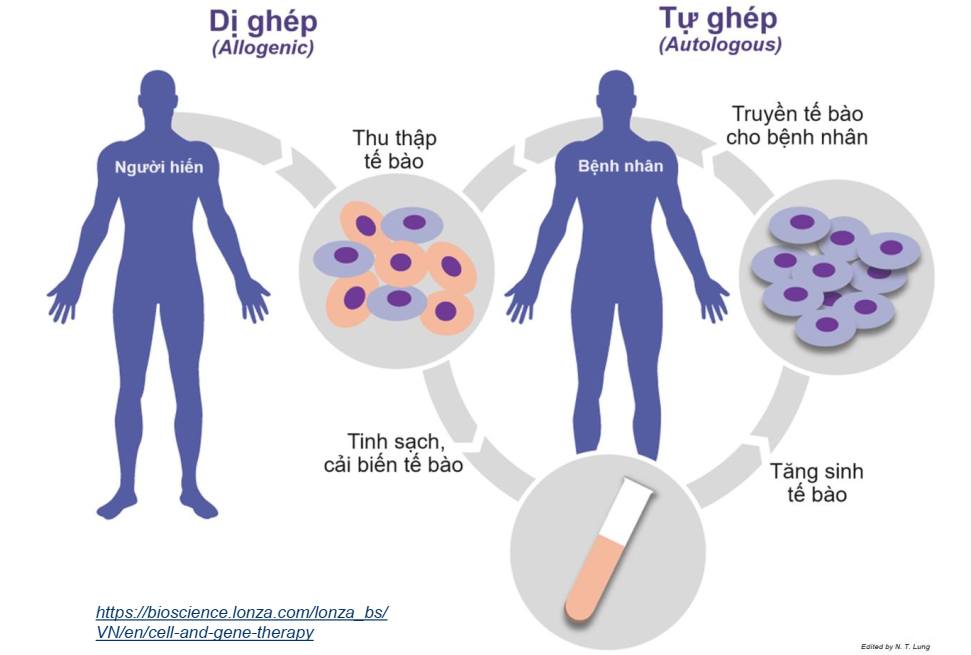
- Lựa chọn người hiến phù hợp, đảm bảo truy xuất được nguồn gốc mẫu hiến và quá trình xử lý chúng
- Việc hiến tặng phải là tự nguyện
- Bảo mật thông tin mẫu hiến tặng
- Việc thu thập, xử lý, bảo quản, vận chuyển mẫu phải được thực hiện theo quy trình đã được phê duyệt tại cơ sở được cấp giấy phép, có thể truy xuất hồ sơ về các quá trình này
(Quy định liên bang 21 CFR 1271, chỉ thị châu Âu 2004/23/EC)
2. Các xét nghiệm sàng lọc (theo FDA Hoa Kỳ)
- Những sàng lọc cần thiết: Virus suy giảm miễn dịch ở người, type 1 và 2 (HIV-1, HIV-2); virus viêm gan B (HBV), viêm gan C (HCV); Treponema pallidum (giang mai)
- Với nguồn mô đi qua cơ quan sinh sản như dây rốn, màng ối, bánh nhau,… cần sàng lọc thêm: Chlamydia trachomatis, Neisseria gonorrhea (vi khuẩn lậu)
- Sản phẩm giàu bạch cầu cần sàng lọc thêm: Virus bạch cầu T ở người, type I và II (HTLV-I, HTLV-II); Cytomegalovirus (CMV)
- Một số tác nhân cần xem xét: Virus tây sông Nile (WNV), Zika (ZIKV), Epstein-Barr (EBV), Bệnh bò điên (TSE), rối loạn não Creutzfeldt-Jakob (CJD), Hormone tăng trưởng
* FDA khuyến cáo xem xét sự cần thiết của từng xét nghiệm sàng lọc dựa trên 3 yếu tố: nguy cơ lây nhiễm, mức độ nguy hiểm khi lây nhiễm, sự sẵn có của xét nghiệm phát hiện (ví dụ như ở Việt Nam thì việc xét nghiệm virus tây sông Nile hay Zika là không cần thiết)
* Xét nghiệm sàng lọc nên được thực hiện theo phương pháp/sinh phẩm được FDA cấp phép (nên không thể sử dụng kết quả test nhanh)
TÀI LIỆU THAM KHẢO