Chỉnh sửa vùng khởi động của gen HBG1 và HBG2 trên tế bào gốc tạo máu để điều trị bệnh thiếu máu hồng cầu hình liềm
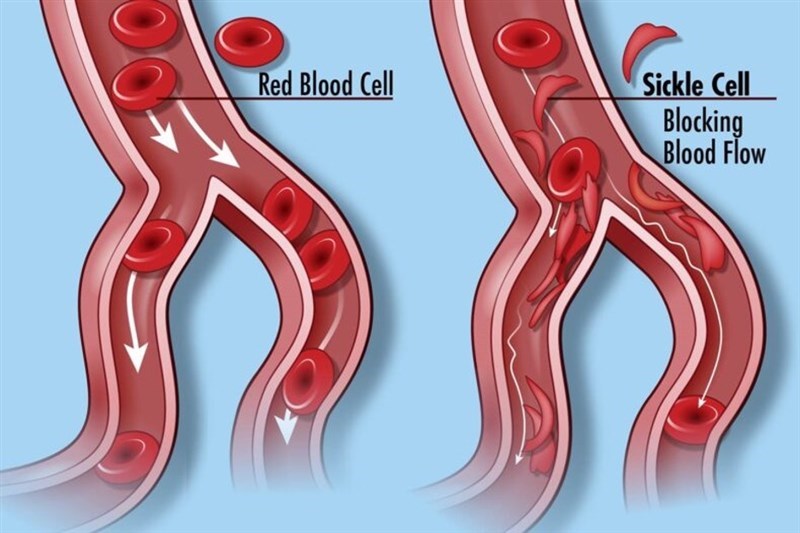
Bệnh hồng cầu hình liềm (Sickle Cell Disease) gây ra bệnh thiếu máu tán huyết mạn tính, là một dạng thiếu máu di truyền do không có đủ các tế bào hồng cầu khỏe mạnh để mang đầy đủ oxy trong cơ thể người bệnh. Đây là một rối loạn di truyền do đột biến gen hemoglobin gây ra, dẫn đến protein hemoglobin (huyết sắc tố, thành phần quan trọng của hồng cầu) bị lỗi, làm biến đổi các tế bào hồng cầu mềm dẻo thành các tế bào cứng, có hình liềm. Các tế bào này dễ bị vỡ, ngưng kết với nhau gây tắc mạch, dẫn đến các cơn đau dữ dội và thiếu máu cục bộ cơ quan. Các cơn tan máu trầm trọng ngày càng thường xuyên, gây nên các biến chứng như nhiễm trùng, bất sản tủy xương, hoặc bệnh phổi có thể phát triển nghiêm trọng gây tử vong. Các phương pháp điều trị bao gồm chống nhiễm trùng (tiêm phòng, thuốc kháng sinh), giảm đau, Hydroxyurea (kích thích sản xuất huyết sắc tố bào thai), truyền máu, cấy ghép tủy xương,…
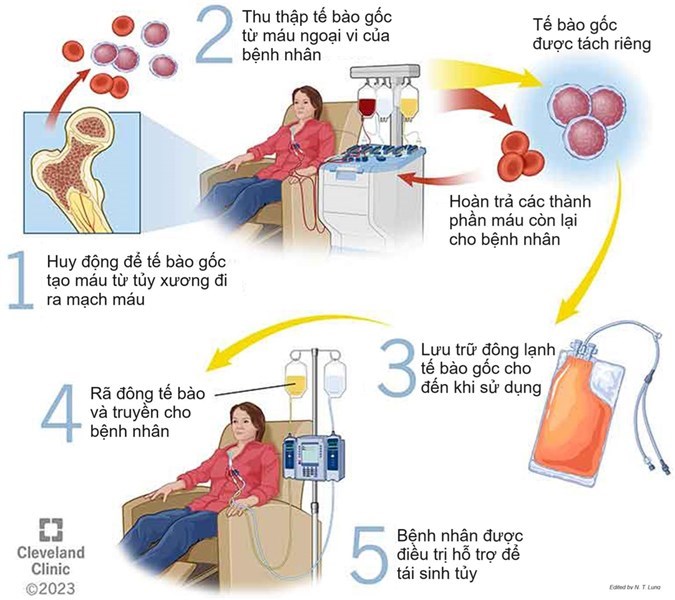
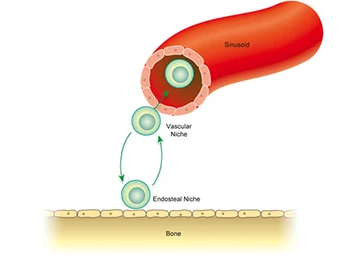
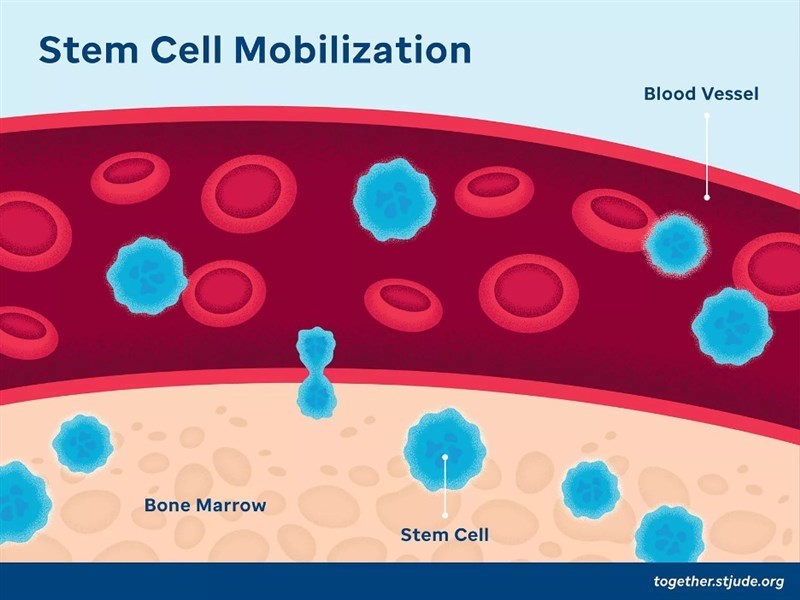
Trong thử nghiệm lâm sàng RUBY (mã số NCT04853576, https://clinicaltrials.gov/study/NCT04853576), các nhà khoa học Hoa Kỳ đã sử dụng công cụ chỉnh sửa gen CRISPR/Cas12a để kích hoạt vùng khởi động (promoter) của gen HBG1 và HBG2 trên tế bào gốc tạo máu tự thân của các bệnh nhân mắc hồng cầu hình liềm. HBG1 và HBG2 cùng mã hóa chuỗi gamma-globin, kết hợp với chuỗi alpha-globin tạo thành hemoglobin thai nhi. Các gen này thường biểu hiện ở gan, lách và tủy xương của thai nhi. Việc kích hoạt vùng khởi động của các gen này ở tế bào gốc tạo máu giúp chúng sản xuất hemoglobin thai nhi, ngăn ngừa hồng cầu chuyển thành dạng hình liềm, và cải thiện nồng độ hemoglobin tổng thể, giảm các biến chứng của bệnh. Liệu pháp tế bào gốc tạo máu được chỉnh sửa vùng khởi động của gen HBG1 và HBG2 có tên Renizgamglogene autogedtemcel (thường được gọi là reni-cel hoặc EDIT-301).
Ngày 01/04/2026, kết quả thử nghiệm RUBY được công bố trên Tạp chí Y học New England. Các bệnh nhân (28 bệnh nhân 12 – 50 tuổi, mắc bệnh thiếu máu hồng cầu hình liềm nặng, trải qua ít nhất 2 biến cố tắc mạch nghiêm trọng mỗi năm trong 2 năm trước đó) được điều trị ức chế tủy xương bằng busulfan, sau đó truyền một liều reni-cel duy nhất. Các bệnh nhân được theo dõi về các chỉ số liên quan đến hemoglobin, các biến cố tắc mạch và các tác dụng phụ trong khoảng thời gian 24 tháng. Nghiên cứu đã bị chấm dứt sớm dựa trên việc nhà tài trợ đánh giá lại các ưu tiên phát triển lâm sàng.
Theo kết quả thử nghiệm, 27/28 bệnh nhân không bị bất kỳ cơn đau dữ dội nào do bệnh sau điều trị, đạt được điều mà các bác sỹ gọi là “chữa khỏi hoàn toàn về mặt chức năng”. Hầu hết bệnh nhân đều thấy các tế bào máu quan trọng phục hồi trong vòng một tháng sau điều trị (bạch cầu trung tính phục hồi sau trung bình 23 ngày, và với tiểu cầu là trung bình 25 ngày). Sau sáu tháng, mức hemoglobin tổng trung bình tăng từ 9,8 g/dL lên 13,8 g/dL – mức gần như bình thường. Mức hemoglobin bào thai (HbF) trung bình là 48,1%, duy trì ổn định theo thời gian. Các tác dụng phụ phù hợp với những tác dụng phụ xảy ra sau khi điều trị tiền ghép tủy bằng busulfan và ghép tế bào gốc tạo máu tự thân.
Những kết quả trên cho thấy đây là phương pháp điều trị đầy hứa hẹn đối với bệnh hồng cầu hình liềm, một rối loạn di truyền có rất ít lựa chọn chữa khỏi. Lợi ích của công nghệ chỉnh sửa gen CRISPR/Cas12a là không gây ra hiện tượng đào thải, khác với phương pháp ghép tủy xương truyền thống, hiện đang là phương pháp điều trị tiêu chuẩn cho bệnh này. Những kết quả đạt được ủng hộ việc nghiên cứu sâu hơn về phương pháp chỉnh sửa gen này trong điều trị bệnh thiếu máu hồng cầu hình liềm nặng.
.png)
TÀI LIỆU THAM KHẢO
Hanna R., et al. (2026). CRISPR-Cas12a gene editing of HBG1 and HBG2 promoters to treat sickle cell disease. New England Journal of Medicine, 394(13), 1281-1291. https://doi.org/10.1056/NEJMoa2415550