Marne-Cel - liệu pháp tế bào gốc chỉnh sửa gen được FDA phê duyệt nhanh để điều trị hội chứng thiếu hụt sự bám dính bạch cầu loại I (LAD-I)
Hội chứng thiếu hụt sự bám dính bạch cầu loại I (Leukocyte adhesion deficiency type I, LAD-I) là một rối loạn suy giảm miễn dịch bẩm sinh khiến hệ miễn dịch không thể bảo vệ cơ thể một cách hiệu quả khỏi các tác nhân gây bệnh như virus, vi khuẩn, nấm. Đây là một hội chứng rất hiếm gặp (tỷ lệ 1/1.000.000 trẻ em), gây ra bởi đột biến gen ITGB2. Gen này bình thường tạo ra một tiểu đơn vị (tiểu đơn vị b2, còn gọi là CD18) của integrin b2 (còn gọi là integrin CD11/CD18), có chức năng nhận biết các dấu hiệu viêm và liên kết với các protein trên lớp lót mạch máu, nhờ đó thu hút bạch cầu tập trung đến bám vào đó, di chuyển qua thành mạch để tìm và tiêu diệt mầm bệnh. Đột biến gen ITGB2 tạo ra tiểu đơn vị b2 (CD18) không thể liên kết với các tiểu đơn vị khác (các tiểu đơn vị a là CD11a, CD11b, CD11c, hoặc CD11d) để tạo thành integrin b2, khiến bạch cầu không thể bám vào thành mạch máu hoặc vượt qua thành mạch để tham gia vào phản ứng miễn dịch.
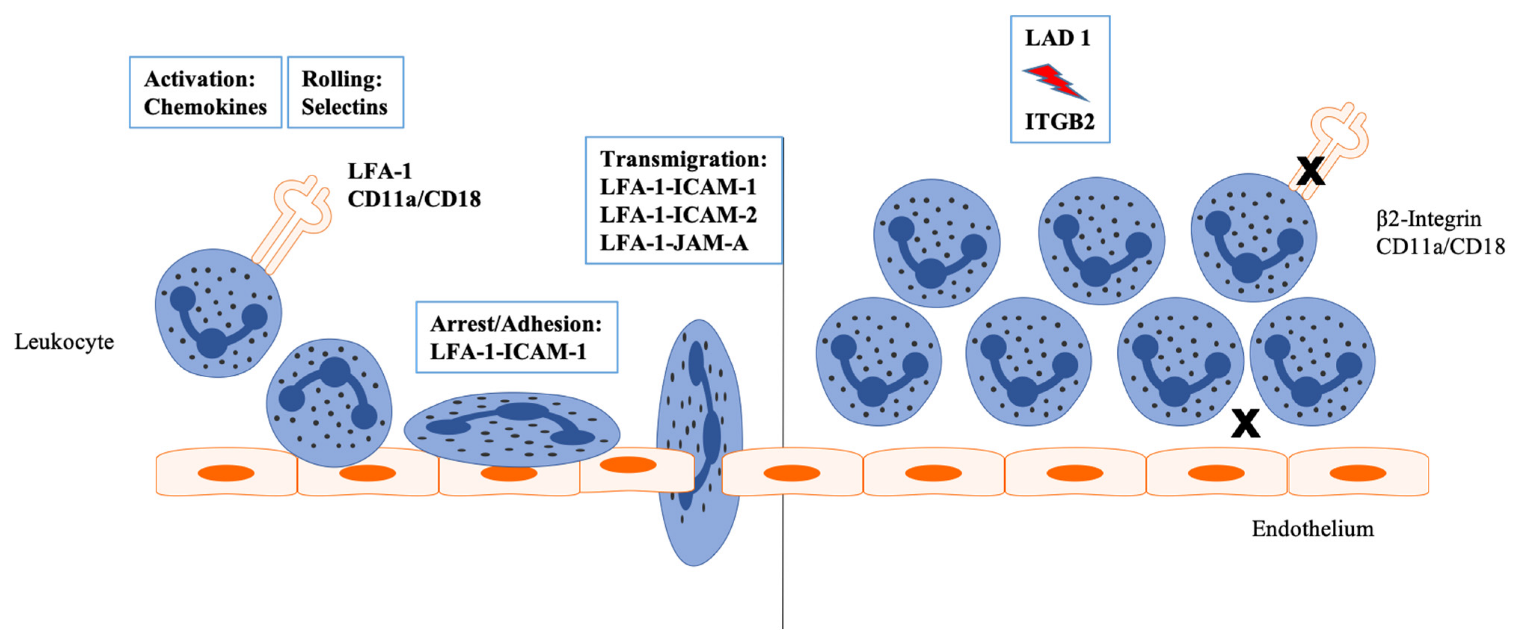
Tình trạng viêm dẫn đến sự hoạt hóa nội mô, integrin β2 tương tác với các protein như ICAM-1 và ICAM-2 giúp bạch cầu bám dính vào nội mô bị viêm, di chuyển xuyên qua thành mạch để tham gia phản ứng miễn dịch. Trong LAD-1, sự thiếu hụt hoặc biểu hiện khiếm khuyết của integrin β2 dẫn đến sự dính và di chuyển xuyên thành mạch của tế bào bạch cầu bị giảm mạnh.
Nguồn: Fekadu J., et al. (2022). Understanding the role of LFA-1 in leukocyte adhesion deficiency type I (LAD I): moving towards inflammation?. International journal of molecular sciences, 23(7), 3578.
Những người mắc LAD-I thường dễ bị nhiễm trùng nghiêm trọng ngay từ khi sinh ra. Một trong những dấu hiệu đầu tiên của bệnh là chậm rụng cuống rốn sau khi sinh, thường vào tuần thứ ba hoặc muộn hơn (trẻ sơ sinh thường rụng cuống rốn trong vòng hai tuần đầu đời). Ngoài ra, trẻ mắc bệnh thường bị viêm rốn. Trong suốt cuộc đời, bệnh nhân thường xuyên bị nhiễm trùng do vi khuẩn và nấm tái phát, thường gặp nhất là viêm lợi (nướu) và viêm nha chu, mất răng sữa và răng vĩnh viễn. Tình trạng này lan rộng ra các vùng khác, biến chứng đe dọa tính mạng, tỷ lệ tử vong cao trước 10 tuổi. Ghép tế bào gốc tạo máu đồng loại được cân nhắc khi điều trị, tuy nhiên tỷ lệ tử vong tương đối cao, đặc biệt là ở những bệnh nhân không có người hiến là anh chị em ruột phù hợp miễn dịch.
Ngày 26/03/2026, Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (U.S. Food and Drug Administration – US FDA) đã phê duyệt liệu pháp tế bào marnetegragene autotemcel (marne-cel, tên thương mại: Kresladi, hãng sản xuất: Rocket Pharmaceuticals) để điều trị LAD-I nghiêm trọng do đồng hợp đột biến ITGB2 mà không có anh chị em ruột phù hợp miễn dịch để ghép tế bào gốc tạo máu. Kresladi bao gồm tế bào gốc tạo máu của chính bệnh nhân, được biến đổi gen để mang các bản sao bình thường của gen ITGB2, nhờ đó có thể tạo nên integrin β2 bình thường. Bệnh nhân được sử dụng một liều duy nhất Kresladi bằng đường truyền tĩnh mạch để khắc phục tình trạng bệnh. Đây là một lựa chọn điều trị tiềm năng, nhắm vào nguyên nhân gốc rễ của hội chứng này.
Tính an toàn và hiệu quả của sản phẩm này đã được chứng minh trong một thử nghiệm lâm sàng giai đoạn I/II đa trung tâm, nhãn mở, đơn nhánh, mã số NCT03812263. Thử nghiệm này đã đánh giá kết quả điều trị bằng marne-cel của 9 trẻ em mắc LAD-I, không có bệnh nhân nào bị thất bại ghép. Sự gia tăng biểu hiện CD18 và CD11a của bạch cầu trung tính vào tháng thứ 12 và duy trì hiệu quả đến tháng thứ 24 sau khi truyền thuốc. Tình trạng tăng bạch cầu trước điều trị và các bất thường khác liên quan đến bệnh đều đã được giải quyết. Tỷ lệ nhập viện do nhiễm trùng hàng năm trong nghiên cứu đều thấp hơn so với con số thống kê về tình trạng chung của bệnh. Các biến cố bất lợi nghiêm trọng được ghi nhận đều được cho là không liên quan đến sản phẩm. Các tác dụng phụ thường gặp nhất được xác định bao gồm thiếu máu, giảm tiểu cầu và bạch cầu, loét miệng, nhiễm trùng đường hô hấp trên, nhiễm trùng do virus, sốt, giảm bạch cầu trung tính kèm sốt, buồn nôn, nôn mửa, nhiễm trùng da, phát ban, tăng men gan.
FDA đã cấp phép nhanh cho sản phẩm Kresladi, do những thông số về tính an toàn và hiệu quả của thử nghiệm trên, đồng thời LAD-I là một bệnh rất hiếm gặp. Đơn vị phát triển sản phẩm (Rocket Pharmaceuticals, Inc.) phải tiến hành các nghiên cứu sau phê duyệt để xác minh và mô tả lợi ích lâm sàng của Kresladi, việc tiếp tục phê duyệt hay thu hồi có thể phụ thuộc vào việc chứng minh lợi ích lâm sàng của sản phẩm này. Việc phê duyệt Kresladi gần như không mang lại lợi nhuận lớn cho Rocket Pharmaceuticals, do LAD-1 là căn bệnh rất hiếm gặp.
TÀI LIỆU THAM KHẢO
1. Fekadu J., et al. (2022). Understanding the role of LFA-1 in leukocyte adhesion deficiency type I (LAD I): moving towards inflammation?. International journal of molecular sciences, 23(7), 3578. https://doi.org/10.3390/ijms23073578
2. Booth C., et al. (2025). Lentiviral gene therapy for severe leukocyte adhesion deficiency type 1. New England Journal of Medicine, 392(17), 1698-1709. https://doi.org/10.1056/NEJMoa2407376
3. U.S. Food and Drug Administration. Thông cáo báo chí (News release) “FDA Approves First Gene Therapy for Severe Leukocyte Adhesion Deficiency Type I”, ngày 26/03/2026. https://www.fda.gov/news-events/press-announcements/fda-approves-first-gene-therapy-severe-leukocyte-adhesion-deficiency-type-i