LIỆU PHÁP TẾ BÀO MIỄN DỊCH
Liệu pháp tế bào miễn dịch khai thác sức mạnh của chính hệ miễn dịch để hỗ trợ cơ thể chống lại các tác nhân gây bệnh và tế bào bất thường. Các loại tế bào miễn dịch như tế bào T, tế bào NK hay tế bào đuôi gai đóng vai trò trung tâm trong phương pháp này.
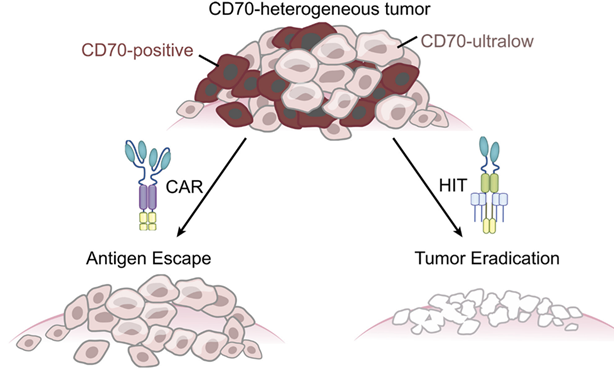
Liệu pháp CAR-T có độ nhạy cao với CD70 mang lại triển vọng loại bỏ hoàn toàn tế bào ung thư trong khối u đặc
Liệu pháp CAR-T đã chứng minh hiệu quả trong điều trị nhiều bệnh huyết học ác tính, nhưng lại gặp rất nhiều hạn chế với các khối u đặc. Một nghiên cứu một công bố trên tạp chí Science cho thấy liệu pháp CAR-T có độ nhạy cao hướng đích CD70 có thể loại bỏ hoàn toàn tế bào ung thư thận, tuyến tụy và buồng trứng ở chuột.
23/03/2026
Liệu pháp tế bào miễn dịch mang cấu trúc CAR: so sánh CAR-T, CAR-NK và CAR-M
Cấu trúc CAR có thể được thiết kế cho nhiều loại tế bào miễn dịch khác nhau, như tế bào T (CAR-T), tế bào giết tự nhiên (CAR-NK), đại thực bào (CAR-M) - mỗi loại đều có những ưu điểm để mang lại tiềm năng điều trị, và có những rào cản cần vượt qua để ứng dụng lâm sàng.
16/03/2026
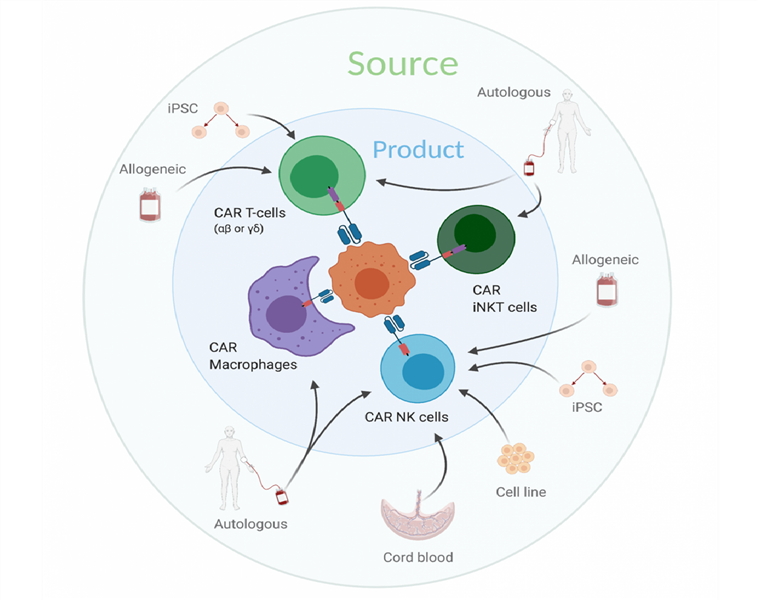
Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh (P4)
Phần 4: Liệu pháp CAR cho các loại tế bào miễn dịch bẩm sinh và những chiến lược kết hợp khi sử dụng lâm sàng
05/03/2026
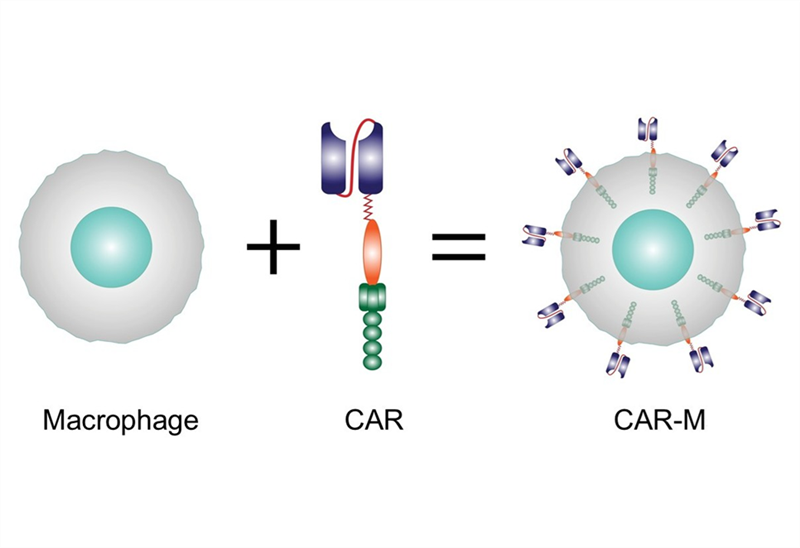
Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh (P3)
Phần 3. Liệu pháp CAR-M – giải pháp đến từ các đại thực bào
26/02/2026
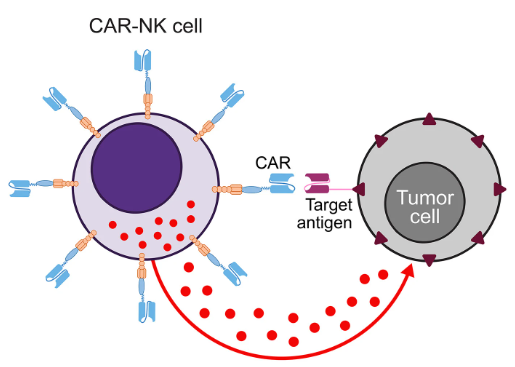
Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh (P2)
Phần 2. Liệu pháp CAR-NK – hiện trạng, thách thức và triển vọng tương lai
15/02/2026
Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh (P1)
Phần 1 - Các tế bào miễn dịch bẩm sinh và lợi thế trong điều trị ung thư u đặc
12/02/2026

Liệu pháp tế bào NK mang lại hy vọng trong điều trị HIV
Các tế bào miễn dịch NK được tăng cường cho thấy tiềm năng trong việc nhắm đích vào những ổ virus HIV mà các loại thuốc hiện nay không thể loại bỏ.
09/02/2026
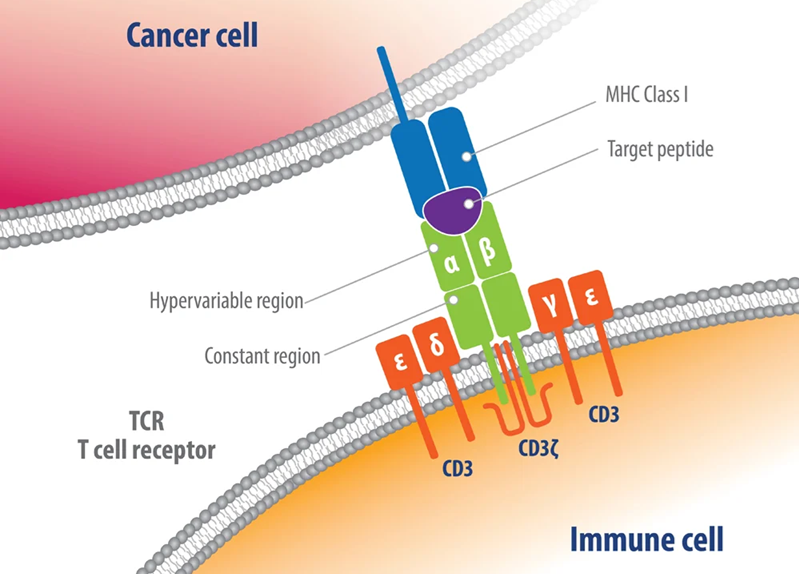
Liệu pháp tế bào T tự thân nhắm đích nhiều kháng nguyên cho thấy triển vọng trong điều trị ung thư tuyến tụy
Một bài báo gần đây trên tạp chí Nature Medicine về thử nghiệm lâm sàng giai đoạn I/II có tên TACTOPS, nghiên cứu về tính an toàn và hiệu quả lâm sàng của liệu pháp tế bào T tự thân nhắm vào nhiều kháng nguyên liên quan đến khối u (Tumor-Associated Antigen, TAA) của ung thư tuyến tụy, đã cho thấy kết quả đầy hứa hẹn.
25/01/2026
Tế bào đuôi gai biểu hiện CD5 đóng vai trò quan trọng đối với khả năng đáp ứng liệu pháp miễn dịch của bệnh nhân ung thư
Liệu pháp miễn dịch đã cho thấy hiệu quả đáng kinh ngạc trong điều trị ung thư. Ví dụ ở bệnh nhân ung thư hắc tố tiến triển (dạng ung thư da gây tử vong nhiều nhất), tỷ lệ sống sót sau năm năm đã tăng từ dưới 10% lên hơn 50% kể từ khi liệu pháp miễn dịch được áp dụng vào năm 2011. Tuy nhiên, tỷ lệ bệnh nhân ung thư đáp ứng với liệu pháp miễn dịch còn thấp. Hệ thống miễn dịch bảo vệ cơ thể chống ung thư bằng cách kích hoạt tế bào lympho T tiêu diệt tế bào khối u, nhưng không tấn công các tế bào khỏe mạnh nhờ hệ thống các điểm kiểm soát miễn dịch. Để đáp ứng lại, các tế bào khối u thao túng hệ thống điểm kiểm soát miễn dịch để tránh sự nhận diện bởi tế bào T. Một trong những hướng đi thành công nhất của liệu pháp miễn dịch ung thư là ức chế các điểm kiểm soát này để tế bào T nhận diện và tiêu diệt tế bào khối u, tuy nhiên tỷ lệ đáp ứng vẫn chưa được như kỳ vọng. Bằng cách phân tích dữ liệu từ The Cancer Genome Atlas - một cơ sở dữ liệu công khai với thông tin về 20.000 khối u đại diện cho 33 loại ung thư, các nhà khoa học Hoa Kỳ đã phát hiện ra rằng những bệnh nhân mắc các loại ung thư da, phổi, xương, mô mềm, vú và cổ tử cung sẽ có kết quả tốt hơn nếu họ có lượng tế bào đuôi gai biểu hiện CD5 cao hơn trong khối u. Tế bào đuôi gai là một thành phần của hệ thống miễn dịch trong cơ thể, giữ vai trò rất quan trọng với khả năng miễn dịch ung thư, có vai trò kích hoạt phản ứng của tế bào T để chống lại khối u ác tính, còn CD5 là một loại glycoprotein được biểu hiện trên bề mặt nhiều loại tế bào miễn dịch nhưng người ta chưa hiểu rõ về chức năng của nó. Các thí nghiệm tiếp theo với tế bào ung thư và mô hình chuột cho thấy tế bào đuôi gai biểu hiện CD5 cần thiết cho hoạt động chống lại tế bào ung thư, chúng kích thích tế bào T tăng sinh và thực hiện chức năng, từ đó làm tăng khả năng sống sót ở bệnh nhân và khả năng đào thải miễn dịch đối với khối u. Những tế bào này cũng đóng góp quan trọng vài việc phong tỏa điểm kiểm soát miễn dịch – một liệu pháp miễn dịch giúp tái kích hoạt phản ứng miễn dịch của chính cơ thể trong điều trị ung thư. IL-6 thúc đẩy sự gia tăng của các tế bào đuôi gai biểu hiện CD5, làm tăng khả năng kích hoạt tế bào T nhận diện và tiêu diệt tế bào khối u. Số lượng tế bào đuôi gai biểu hiện CD5 giảm ở các hạch bạch huyết làm giảm khả năng đáp ứng với các thuốc ức chế điểm kiểm soát miễn dịch, từ đó giảm hiệu quả tiêu diệt khối u của tế bào T. Nhóm nghiên cứu cũng phát hiện số lượng tế bào đuôi gai biểu hiện CD5 bên trong khối u có thể được sử dụng để đánh giá khả năng bệnh nhân nhận được lợi ích từ liệu pháp miễn dịch hay không. Việc làm tăng số lượng hoặc tăng cường hoạt động của tế bào đuôi gai biểu hiện CD5 có khả năng là giải pháp hỗ trợ hiệu quả trong điều trị ung thư bằng liệu pháp miễn dịch. Một trong những giải pháp để thực hiện điều này, các nhà khoa học đã chứng minh protein miễn dịch IL-6 giúp làm tăng lượng tế bào đuôi gai biểu hiện CD5. TÀI LIỆU THAM KHẢO He M., et al. (2023). CD5 expression by dendritic cells directs T cell immunity and sustains immunotherapy responses. Science, 379(6633), eabg2752. DOI: https://doi.org/10.1126/science.abg2752
23/01/2026
Tế bào NK có khả năng ghi nhớ và tấn công hiệu quả ung thư buồng trứng
Tế bào giết tự nhiên (natural killer – NK) là loại tế bào bạch cầu đóng vai trò quan trọng trong hệ miễn dịch bẩm sinh, có khả năng tiêu diệt các tế bào nhiễm virus và tế bào bất thường, bao gồm các tế bào có khả năng hình thành ung thư.
23/01/2026
Các dấu ấn sinh học để dự đoán khả năng đáp ứng với liệu pháp TIL
Liệu pháp tế bào lympho thâm nhiễm khối u (Tumor Infiltrating Lymphocyte - TIL) là phương pháp điều trị ung thư bằng cách phân lập các tế bào lympho T từ khối u của bệnh nhân, nuôi cấy tăng sinh, sau đó truyền trở lại cơ thể bệnh nhân. Liệu pháp TIL đã được chứng minh hiệu quả trong điều trị ung thư hắc tố (trong đó sản phẩm AMTAGVI (Lifileucel) đã được FDA phê duyệt), bên cạnh những tác dụng tích cực trên bệnh nhân ung thư cổ tử cung, đại trực tràng, đường mật,…
23/01/2026
Liệu pháp TIL trong điều trị u đặc: Triển vọng và thách thức
Liệu pháp tế bào lympho thâm nhiễm khối u (Tumor Infiltrating Lymphocyte - TIL) là một loại liệu pháp miễn dịch sử dụng các tế bào lympho T được lấy từ khối u của bệnh nhân, nuôi cấy và nhân lên trong phòng thí nghiệm, sau đó truyền trở lại cơ thể bệnh nhân để tấn công các tế bào ung thư. Hiện nay, nhiều trung tâm ung thư lâm sàng trên thế giới triển khai liệu pháp TIL và đã cho thấy những kết quả ấn tượng trong điều trị nhiều loại u đặc khác nhau. 1. Dữ liệu lâm sàng về liệu pháp TIL trong điều trị u đặc Tháng 02/2024, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (U.S. Food and Drug Administration – US FDA) đã chấp thuận sản phẩm AMTAGVI (Lifileucel) của Iovance Biotherapeutics trong điều trị ung thư hắc tố – liệu pháp TIL đầu tiên và duy nhất tính đến nay được FDA phê duyệt. Việc chấp thuận này dựa trên những kết quả thử nghiệm lâm sàng trên hơn 70 bệnh nhân, trong đó tỷ lệ kiểm soát bệnh là 80%, kích thước khối u giảm ở 1/3 số bệnh nhân, trong đó có một số bệnh nhân đáp ứng hoàn toàn (không còn u), khoảng 40% bệnh nhân đáp ứng liệu pháp không thấy bệnh tiến triển sau 1 năm. Ngoài Lifileucel đã được chấp thuận, có rất nhiều sản phẩm liệu pháp TIL đang được thử nghiệm lâm sàng, chủ yếu để điều trị bước hai cho các loại u đặc. U hắc tố vẫn là loại ung thư chiếm hầu hết các thử nghiệm, với những kết quả rất khả quan về tỷ lệ đáp ứng, ngoài ra TIL có lợi ích lâm sàng ấn tượng với bệnh nhân ung thư cổ tử cung, có hiệu quả ban đầu trong ung thư phối không tế bào nhỏ, đại trực tràng, đường mật và vú. 2. Quy trình thực hiện liệu pháp TIL trong điều trị u đặc - Phẫu thuật cắt khối u từ bệnh nhân - Phân lập tế bào lympho T từ mô khối u - Nuôi cấy tăng sinh TIL, sàng lọc TIL có hoạt tính - Chuẩn bị bệnh nhân: làm suy giảm lympho mà không phá hủy tủy bằng cách hóa trị hoặc xạ trị toàn thân - Truyền các tế bào TIL cho bệnh nhân, kích thích TIL khi vào cơ thể bằng Interleukin-2 (IL-2) 3. Các liệu pháp kết hợp với TIL trong điều trị u đặc - Chất ức chế điểm kiểm soát miễn dịch: Ở bệnh nhân ung thư, sự tăng cường biểu hiện các điểm kiểm soát miễn dịch (PD-1/PD-L1, CTLA-4, LAG-3,…) làm ức chế chức năng của tế bào T. Việc sử dụng TIL kết hợp các chất ức chế PD-1/PD-L1 và CTLA-4 làm tăng hiệu quả điều trị. - Chất ức chế BRAF: Đột biến BRAF là đột biến phổ biến nhất gây ra hoạt hóa quá mức con đường truyền tin tế bào MAPK, làm tế bào tăng sinh mất kiểm soát, có thể gây cơ chế thoát miễn dịch. Chất ức chế BRAF như vemurafenib có thể làm giảm tín hiệu ức chế miễn dịch liên quan, giảm các tế bào ức chế miễn dịch, tạo điều kiện cho sự xâm nhập của tế bào lympho và tăng cường hiệu quả của liệu pháp TIL. - Vaccine tế bào tua (DC): Vaccine DC có thể gây các phản ứng miễn dịch, kích hoạt và tăng số lượng TIL. Sự kết hợp của nó với TIL đang được đánh giá. - Virus tiêu ung thư: Virus có thể chống lại tình trạng ức chế miễn dịch của khối u bằng cách sản xuất các cytokine thúc đẩy tác dụng chống khối u của TIL. Một thử nghiệm cho thấy TIL kết hợp adenovirus trong điều trị u hắc tố di căn đã mang lại những lợi ích lâm sàng đáng khích lệ 4. Những hạn chế của liệu pháp TIL và triển vọng trong tương lai Liệu pháp TIL có một số ưu điểm so với các liệu pháp tế bào miễn dịch khác như: TIL mang nhiều thụ thể tế bào T (T Cell Receptor – TCR) nên có thể tác động lên phổ rộng kháng nguyên đặc hiệu khối u, giúp hiệu quả hơn trong việc đáp ứng với tính không đồng nhất của khối u; TIL dễ dàng định vị trong mô khối u sau khi truyền; có độc tính thấp do lấy tự thân mà chưa qua chỉnh sửa gen. Tuy nhiên, liệu pháp TIL cũng có những hạn chế: không phải tách được TIL từ tất cả các khối u, do tế bào T hiệu lực có hoạt tính kháng u nhiều khi không có mặt trong khối u; việc lựa chọn TIL có hoạt tính gặp khó khăn đối với những khối u mang kháng nguyên đặc mới; vi môi trường khối u ức chế miễn dịch làm giảm mạnh các tế bào T độc thâm nhiễm khối u; TIL có thời gian sống sót ngắn trong cơ thể sau khi truyền. Những hạn chế này đang được các nhà khoa học đẩy lùi dần với nhiều cách thức khác nhau. Hiện tại, nhiều nghiên cứu và thử nghiệm lâm sàng vẫn đang tìm cách xây dựng các chiến lược để khắc phục những hạn chế trên, đẩy mạnh hiệu quả của TIL, đồng thời khám phá những liệu pháp kết hợp thay thế. --------- TÀI LIỆU THAM KHẢO 1. Zhao Y., et al. (2022). Tumor infiltrating lymphocyte (TIL) therapy for solid tumor treatment: progressions and challenges. Cancers, 14(17), 4160. DOI: 10.3390/cancers14174160. 2. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-accelerated-approval-lifileucel-unresectable-or-metastatic-melanoma
23/01/2026







