Liệu pháp tế bào miễn dịch mang cấu trúc CAR: so sánh CAR-T, CAR-NK và CAR-M
Các tế bào T có khả năng nhận diện tế bào bất thường nhờ các thụ thể trên bề mặt của chúng. Để phát hiện dễ dàng và đặc hiệu hơn, các nhà khoa học đã thiết kế thụ thể kháng nguyên khảm (Chimeric Antigen Receptor, CAR) có khả năng nhận diện kháng nguyên nhất định trên tế bào ác tính. Liệu pháp sử dụng tế bào T mang cấu trúc CAR (CAR-T) mang đến một phương pháp đầy hứa hẹn để điều trị ung thư, trong đó có 7 sản phẩm đã được FDA Hoa Kỳ phê duyệt cho các tình trạng huyết học ác tính, bên cạnh các thử nghiệm lâm sàng điều trị các bệnh lý khác.
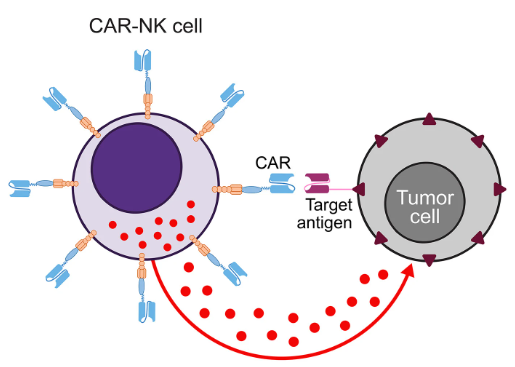
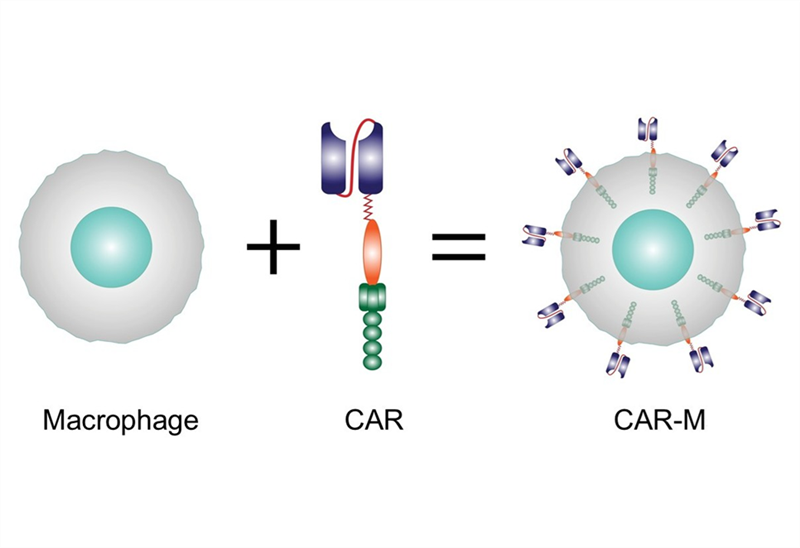
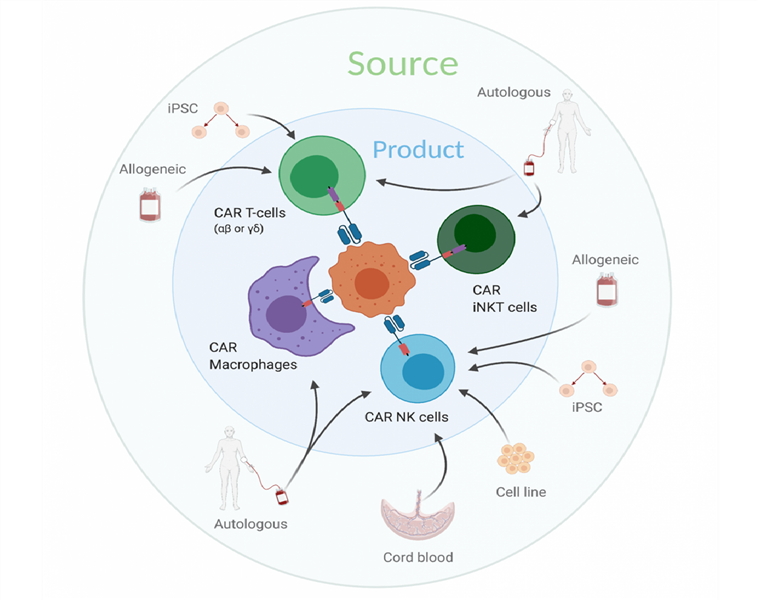
Ngoài tế bào T, cấu trúc CAR có thể được thiết kế cho nhiều loại tế bào miễn dịch khác, trong đó được thử nghiệm nhiều nhất là tế bào giết tự nhiên (CAR-NK) và đại thực bào (CAR-M). Những loại tế bào này có cơ chế tiêu diệt tế bào bất thường đa dạng hơn, độ an toàn cao hơn (ít độc tính thần kinh và hội chứng giải phóng cytokine hơn), có tiềm năng sản xuất hàng loạt giúp bệnh nhân dễ tiếp cận hơn và giảm chi phí sản xuất so với CAR-T. Tuy nhiên, CAR-NK và CAR-M mới được phát triển gần đây nên vẫn dừng ở giai đoạn thử nghiệm, chưa có liệu pháp được phê duyệt như CAR-T, thời gian tồn tại trong cơ thể ngắn hơn CAR-T, nên vẫn còn nhiều rào cản cần vượt qua để có thể ứng dụng lâm sàng.
|
Liệu pháp |
CAR-T |
CAR-NK |
CAR-M |
|
Nguồn tế bào |
Tế bào T tự thân, tế bào T đồng loại phù hợp MHC |
Tế bào NK tự thân, tế bào đồng loại không tương thích MHC |
Tự thân (thử nghiệm lâm sàng), iPSC và dòng đại thực bào thương mại (thử nghiệm tiền lâm sàng) |
|
Cấu trúc CAR
|
Miền truyền tín hiệu/vùng nội bào (ICD), miền bản lề/vùng xuyên màng (HD/TMD), yếu tố nhận diện mục tiêu (TRE) |
- Tương tự như cấu trúc CAR-T - Có thể cải biến ICD và HD/TMD đặc hiệu cho tế bào NK |
- Tương tự như cấu trúc CAR-T - Có thể cải biến ICD và HD/TMD đặc hiệu cho đại thực bào, ICD có thể thêm yếu tố để tăng tiết cytokine điều chỉnh vi môi trường khối u |
|
Tế bào tiếp nhận chuyển gen CAR |
Tế bào T sơ cấp |
- Tế bào NK sơ cấp - Tế bào iPSC hoặc dòng tế bào thương mại |
- Tế bào sơ cấp - Tế bào iPSC hoặc dòng tế bào thương mại |
|
Tăng sinh in vitro |
Tăng sinh CAR-T tự thân |
- Tăng sinh CAR-NK tự thân - Tăng sinh dòng tế bào sau khi chuyển gen và chọn lọc |
- Tăng sinh CAR-M tự thân - Tăng sinh dòng tế bào và iPSC sau khi chuyển gen và chọn lọc |
|
Cơ chế tiêu diệt tế bào đích |
Phụ thuộc CAR: tiêu diệt tế bào mang kháng nguyên đặc hiệu với CAR |
- Phụ thuộc CAR: tiêu diệt tế bào mang kháng nguyên đặc hiệu với CAR; - Không phụ thuộc CAR: độc tính tự nhiên của tế bào NK |
- Phụ thuộc CAR: Thực bào đối với tế bào mang kháng nguyên đặc hiệu CAR - Không phụ thuộc CAR: trình diện kháng nguyên kích thích phản ứng miễn dịch, điều hòa miễn dịch, thay đổi vi môi trường khối u |
|
Tác dụng phụ |
Bệnh ghép chống chủ, hội chứng giải phóng cytokine và độc tính thần kinh xuất hiện phổ biến và thường nghiêm trọng |
Ít phổ biến hơn và nếu có cũng ít nghiêm trọng hơn |
Chưa có dữ liệu lâm sàng |
|
Thâm nhiễm u đặc |
Rất khó |
Có khả năng |
Rất dễ dàng |
|
Ứng dụng lâm sàng |
Hiệu quả đã được chứng minh, với 7 liệu pháp CAR-T được FDA Hoa Kỳ phê duyệt. |
Chưa có liệu pháp CAR-NK nào được phê duyệt; các thử nghiệm lâm sàng đã cho thấy tính an toàn và hiệu quả bước đầu |
Chưa có liệu pháp CAR-M nào được phê duyệt; các thử nghiệm lâm sàng đã cho thấy tính an toàn và hiệu quả bước đầu |
|
Sản phẩm tế bào mang CAR có sẵn (Off-the-shelf) |
Chưa chắc chắn thực hiện được (thường là CAR-T tự thân hoặc tế bào CAR-T đồng loài phù hợp MHC) |
- Có thể sản xuất với dòng tế bào NK thương mại - Có tiềm năng sản xuất được với các tế bào NK đồng loại, nhưng khả năng phục hồi kém khi được bảo quản đông lạnh. |
Về mặt lý thuyết, điều này có thể thực hiện được với các dòng tế bào đại thực bào. Tuy nhiên, hiện chưa có dữ liệu lâm sàng nào. |
|
Khả năng tồn tại trong cơ thể |
Có thể tồn tại lâu trong cơ thể, mang lại hiệu quả kéo dài. |
Tế bào CAR-NK thường có tuổi thọ ngắn hơn tế bào CAR-T trong cơ thể |
Tuổi thọ của CAR-M khác nhau và có thể bị ảnh hưởng bởi mô. |
|
Tính sinh miễn dịch |
Nguy cơ mắc hội chứng giải phóng cytokine và độc tính thần kinh. |
Ít gây phản ứng miễn dịch hơn so với tế bào CAR-T. |
Có thể điều hòa phản ứng miễn dịch nhưng có thể có những hạn chế về mặt sử dụng toàn thân. |
|
Các loại bệnh lý tiềm năng |
Chủ yếu được sử dụng trong điều trị các bệnh ác tính về huyết học, ngoài ra đang cho thấy hiệu quả trên các bệnh tự miễn |
Có thể là nhiều loại ung thư khác nhau (cả bệnh huyết học ác tính và ung thư u đặc), đặc biệt là điều trị bằng ghép đồng loài; có tiềm năng điều trị bệnh tự miễn, truyền nhiễm. |
Khả năng áp dụng lâm sàng đa dạng |
.png)
A. Cơ chế tiêu diệt tế bào bất thường của CAR-T. Các tế bào CAR-T được hoạt hóa có thể nhận diện đặc hiệu kháng nguyên liên quan đến khối u (TAA). Hoạt tính gây độc của CAR-T được trung gian bởi sự tiết các hạt perforin (PFN) và granzyme (GzmB), và hoạt hóa các con đường thụ thể gây chết tế bào như Fas/Fas-L dẫn đến sự chết tế bào theo chương trình (apoptosis) và hoại tử tế bào ung thư. CAR-T được hoạt hóa cũng tiết ra Interferon-gamma (IFN-γ) và yếu tố hoại tử khối u alpha (TNFα), có thể thúc đẩy hoạt động gây độc tế bào chống khối u của tế bào NK. B. Cơ chế tiêu diệt tế bào bất thường của tế bào CAR-NK. Hoạt động của tế bào CAR-NK được điều chỉnh bởi tín hiệu của các thụ thể hoạt hóa (KAR) và ức chế (KIR) được biểu hiện trên tế bào NK. Các tế bào CAR-NK được hoạt hóa tiết ra các protein gây độc tế bào perforin và granzyme B, chúng phối hợp với nhau để gây hoại tử và thúc đẩy tế bào ung thư chết theo chương trình. Tế bào NK cũng biểu hiện các chất gây chết tế bào FasL và TRAIL, chúng liên kết với Fas và TRAIL-R trên tế bào ung thư và gây ra apoptosis. Tế bào CAR-NK kích hoạt gây độc tế bào phụ thuộc kháng thể (ADCC) thông qua thụ thể CD16 Fc. Ngoài ra, tế bào CAR-NK tiết ra IFN-γ và TNFα, thúc đẩy sự hoạt hóa của chúng và kích thích các tế bào lympho T khác, dẫn đến tăng cường đáp ứng miễn dịch chống khối u. C. Cơ chế tiêu diệt tế bào bất thường của CAR-M. Sự gắn kết của kháng nguyên đặc hiệu liên quan đến khối u (TAA) với CAR trên bề mặt CAR-M tạo ra các tín hiệu kích hoạt, dẫn đến quá trình thực bào khối u, kích hoạt các yếu tố phiên mã như NF-kB và giải phóng các cytokine gây viêm, từ đó kích hoạt miễn dịch qua trung gian tế bào T chống lại khối u.
Nguồn: Maalej K. M., et al. (2023). CAR-cell therapy in the era of solid tumor treatment: current challenges and emerging therapeutic advances. Molecular cancer, 22(1), 20. https://doi.org/10.1186/s12943-023-01723-z
TÀI LIỆU THAM KHẢO
1. Jassaud M., et al. (2026). Innate immune cells in chimeric antigen receptor therapy. Molecular Therapy, 34 (1), 97-116. https://doi.org/10.1016/j.ymthe.2025.10.003
2. Look T., et al. (2025). CAR T cells, CAR NK cells, and CAR macrophages exhibit distinct traits in glioma models but are similarly enhanced when combined with cytokines. Cell Reports Medicine, 6(2), 101931. https://doi.org/10.1016/j.xcrm.2025.101931
3. Yao P., et al. (2024). The development and application of chimeric antigen receptor natural killer (CAR-NK) cells for cancer therapy: current state, challenges and emerging therapeutic advances. Experimental Hematology & Oncology, 13 (1), 118. https://doi.org/10.1186/s40164-024-00583-7
4. Maalej K. M., et al. (2023). CAR-cell therapy in the era of solid tumor treatment: current challenges and emerging therapeutic advances. Molecular cancer, 22(1), 20. https://doi.org/10.1186/s12943-023-01723-z