Chính sách phê duyệt nhanh có điều kiện cho liệu pháp tế bào ở Nhật Bản: giữa những tia hy vọng và các câu hỏi lớn về đạo đức
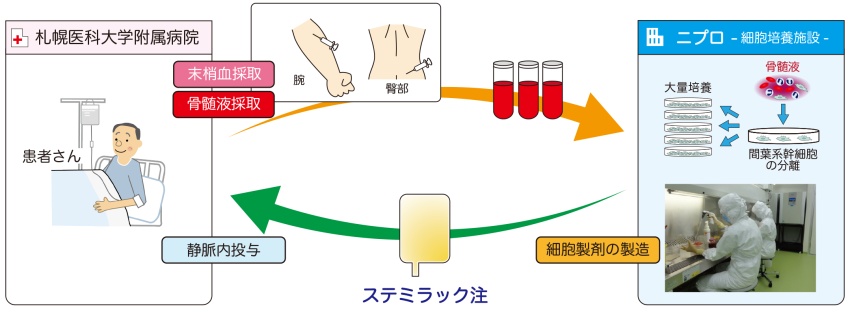
Những tranh cãi này không phải bây giờ mới xuất hiện. Năm 2018, Bộ Y tế, Lao động và Phúc lợi Nhật Bản đã cấp phép có điều kiện cho sản phẩm Stemirac (phát triển bởi Nipro Corp.), một liệu pháp tế bào gốc trung mô tủy xương tự thân để điều trị chấn thương tủy sống. Sau đó ít lâu, năm 2019, tạp chí điện tử Undark đã có bài tổng hợp những ý kiến trái chiều, xin được lược dịch (và bổ sung thêm một số thông tin về 2 sản phẩm mới được phê duyệt có điều kiện tháng 02/2026).
Xem thêm: Nhật Bản phê duyệt có điều kiện cho hai sản phẩm có nguồn gốc từ tế bào gốc đa tiềm năng cảm ứng (iPSC) https://ysinhtebao.com/tin-tuc/nhat-ban-phe-duyet-hai-san-pham-ipsc

1. Chương trình phê duyệt nhanh của Nhật Bản trong cấp phép y tế
Các chương trình phê duyệt nhanh của Nhật Bản được thiết kế để đẩy nhanh quá trình cấp phép các sản phẩm y tế sáng tạo, thuốc điều trị bệnh hiểm nghèo và các thiết bị y tế mới. Trong số này, các sản phẩm liệu pháp tế bào và gen thường nằm trong hệ thống phê duyệt sớm có điều kiện (Conditional Early Approval System), cho phép cấp phép tạm thời dựa trên bằng chứng sơ bộ. Nghĩa là, thay vì phải trải qua các thử nghiệm lâm sàng quy mô lớn, kéo dài và tốn kém như quy trình truyền thống, nhà sản xuất chỉ cần thực hiện các thử nghiệm nhỏ để chứng minh tính an toàn và gợi ý (chưa cần khẳng định chắc chắn) về hiệu quả. Sau khi được cấp phép sớm có điều kiện, các sản phẩm này được bán ra thị trường trong vòng tối đa 7 năm, trong thời gian đó công ty thu thập thêm dữ liệu thực tế để chứng minh hiệu quả cuối cùng trước khi được cấp phép chính thức.
Chính sách này được ban hành từ năm 2014, trong nỗ lực của cố Thủ tướng Shinzo Abe nhằm đưa Nhật Bản trở thành quốc gia dẫn đầu thế giới về y học tái tạo, sau khi nhà khoa học Shinya Yamanaka công bố phát hiện về tế bào gốc đa tiềm năng cảm ứng (induced pluripotent stem cell – iPSC) năm 2006 và được trao giải Nobel năm 2012.
Xem thêm: Tế bào gốc đa tiềm năng cảm ứng (iPSC) - tái lập trình tế bào soma https://ysinhtebao.com/tbg/ipsc-dai-cuong
2. Những ý kiến ủng hộ
Hệ thống phê duyệt sớm có điều kiện của Nhật Bản có nguồn gốc tinh thần từ tư tưởng tự do của Mỹ, mà nhà kinh tế học Milton Friedman (người từng đạt giải Nobel, tác giả cuốn sách “Tự do lựa chọn: một tuyên ngôn cá nhân”) từng phát biểu: “Cơ quan Quản lý Thực phẩm và Dược phẩm (FDA) đã gây ra thiệt hại to lớn cho sức khỏe người dân Mỹ bằng cách làm tăng đáng kể chi phí nghiên cứu dược phẩm, do đó làm giảm nguồn cung cấp thuốc mới và hiệu quả, và bằng cách trì hoãn việc phê duyệt những loại thuốc vượt qua được quy trình khắt khe của FDA”.
Một số người ủng hộ cho rằng chính sách này đã giúp các bệnh nhân mắc bệnh hiểm nghèo có cơ hội tiếp cận sớm với các phương pháp điều trị tiềm năng, thay vì phải chờ đợi thử nghiệm lâm sàng (có thể kéo dài hàng thập kỷ). Họ cũng cho rằng bệnh nhân nên có quyền tự quyết định tham gia các liệu pháp thử nghiệm, khi mà các phương pháp truyền thống không còn tác dụng. Chính phủ Nhật Bản cũng kỳ vọng đây là động lực tăng trưởng kinh tế mới, ước tính thị trường y học tái tạo của nước này có thể đạt 10 tỷ USD vào năm 2030. Đồng thời, các công ty công nghệ sinh học nhỏ có thể tiết kiệm chi phí thử nghiệm lâm sàng, thu hút các nhà đầu tư và doanh nghiệp nước ngoài đến Nhật Bản để ra mắt thuốc hay phương pháp điều trị mới.
3. Và làn sóng phản đối mạnh mẽ
Mặc dù vậy, chính sách này nhận được những phản ứng dữ dội ngay từ khi mới được ban hành năm 2014.
Các phương pháp được phê duyệt kiểu này thường thiếu bằng chứng khoa học, khi các thử nghiệm trên quy mô nhỏ (Stemirac thử nghiệm trên 13 người, con số này ở Amchepry là 7 và ReHeart là 8), thiếu phương pháp mù đôi và giả dược (tất cả những người tham gia đều biết các đối tượng được điều trị thử nghiệm), cơ sở lý thuyết thiếu thuyết phục (dựa trên các cơ chế đã bị cộng đồng khoa học bác bỏ từ nhiều năm trước), đi ngược lại các tiêu chuẩn vàng của nghiên cứu y sinh. Các sản phẩm truyền tĩnh mạch như Stemirac, thực ra rất dễ tạo nhóm đối chứng giả dược, nhưng nhà sản xuất đã không làm. “Tại sao họ không làm vậy? Họ nói rằng họ không cần phải làm vậy để được phê duyệt có điều kiện.”!!!
Căng thẳng hơn, nhiều nhà khoa học chỉ trích hệ thống phê duyệt của Nhật Bản thiếu minh bạch. Kết quả thử nghiệm của Stemirac và sau này là ReHeart chỉ được đăng tải trên phương tiện thông tin đại chúng, không được công bố trên tạp chí khoa học uy tín có thẩm định, bình duyệt. Câu chuyện về Stemirac năm 2018 được kể với giọng châm biếm:
Các nhà nghiên cứu Sapporo đã từ chối công bố kết quả nghiên cứu theo yêu cầu của Bộ Y tế Nhật Bản, có lẽ các quan chức cho rằng việc làm đó có thể bị coi là quảng bá cho phương pháp điều trị. Tuy nhiên, các nhà nghiên cứu và bệnh nhân đã tham gia một bộ phim tài liệu trên đài truyền hình công cộng NHK của Nhật Bản, ca ngợi phương pháp điều trị này như một cuộc cách mạng y học kỳ diệu. Bộ phim tài liệu kết thúc với lời dẫn chuyện: "Những gì đã mất nay đã được phục hồi. Kỷ nguyên của y học tái tạo đã đến."
Chính vì vậy, các sản phẩm này tiềm ẩn những nguy cơ về an toàn và hiệu quả. Như đã nói ở trên, nhà sản xuất chỉ cần thực hiện các thử nghiệm nhỏ để chứng minh tính an toàn và gợi ý (chưa cần khẳng định chắc chắn) về hiệu quả là có thể nộp hồ sơ cấp phép có điều kiện. Vì vậy, những rủi ro về sức khỏe chưa hề được lường trước, trong khi hiệu quả nhiều khi chỉ là phỏng đoán. Bệnh nhân có thể hy vọng hão huyền về những phương pháp chữa bệnh thần kỳ, và dẫn đến sự hoài nghi về giá trị của nghiên cứu. Tuy nhiên, bệnh nhân lại tốn một khoản tiền rất lớn (với Stemirac là khoảng 140.000 USD), có thể được bảo hiểm thanh toán nhưng khi đó, quỹ bảo hiểm đã phải chi trả một khoản tiền không nhỏ để hỗ trợ cho các bệnh khác được điều trị hiệu quả. Các công ty, lẽ ra phải thực hiện thử nghiệm lâm sàng rất tốn kém, trong đó có việc hỗ trợ cho bệnh nhân tham gia, thì lại thu được tiền và số liệu thử nghiệm từ bệnh nhân.
Cuối cùng, cộng đồng khoa học đã lo ngại và chỉ trích chính sách này có khả năng tạo ra tiền lệ xấu, các quốc gia liệu có nới lỏng quá mức các quy định để cạnh tranh nhau về kinh tế, tạo ra “một cuộc chạy đua xuống đáy rất nghiêm trọng và tồi tệ”, “có thể quay trở lại thời kỳ mà hầu hết các sản phẩm y tế đều không hiệu quả”, tổn hại đến uy tín của ngành y học tái tạo toàn cầu.
Thông tin này được lược dịch từ bài viết “A New Japanese Stem Cell Treatment Raises Hopes — And Ethical Questions” đăng tải trên trang Undark năm 2019 https://undark.org/2019/08/27/new-japanese-stem-cell-treatment-debate/, cập nhật thêm về hai liệu pháp mới được phê duyệt nhanh tháng 02/2026.