Nhật Bản phê duyệt có điều kiện cho hai sản phẩm có nguồn gốc từ tế bào gốc đa tiềm năng cảm ứng (iPSC)
Ngày 19/02/2026, một hội đồng chuyên gia thuộc Bộ Y tế, Lao động và Phúc lợi Nhật Bản đã thông qua đề xuất phê duyệt có điều kiện cho hai sản phẩm từ tế bào gốc đa tiềm năng cảm ứng (induced Pluripotent Stem Cell – iPSC). Sau khi được Bộ trưởng phê duyệt, hai sản phẩm này (bao gồm liệu pháp Amchepry để điều trị Parkinson – phát triển bởi Sumitomo Pharma kết hợp với Racthera Inc., và miếng dán cơ tim ReHeart để điều trị suy tim – sản phẩm của Cuorips Inc.) sẽ là những sản phẩm iPSC được thương mại hóa đầu tiên trên thế giới.

1. Tế bào gốc đa tiềm năng cảm ứng
Tế bào gốc đa tiềm năng cảm ứng (induced Pluripotent Stem Cell – iPSC) là loại tế bào gốc đa tiềm năng được tạo ra trực tiếp từ tế bào soma bằng cách tái lập trình (“reprogramming”). Trong tự nhiên, sự biệt hóa tế bào đi theo một chiều không đảo ngược theo hướng giảm dần tính gốc. Năm 2006, Yamanaka và cộng sự đã công bố nghiên cứu chuyển các gen mã hóa yếu tố phiên mã hoạt động ở giai đoạn phôi sớm vào nguyên bào sợi chuột, cảm ứng chúng đảo ngược quá trình biệt hóa để trở thành tế bào gốc đa tiềm năng (nhờ công trình này, ông đã được nhận giải Nobel Y học và Sinh lý học 2012). Năm 2007, bằng phương pháp tương tự, iPSC ở người đã được tạo nên bởi hai nhóm nghiên cứu độc lập của Yamanaka (người lần đầu tiên tạo ra iPSC năm 2006) và Thompson (người lần đầu tiên phân lập được tế bào gốc phôi người năm 1998).
.png)
Tế bào trưởng thành ở người (tế bào biểu bì da, nguyên bào sợi, tế bào bạch cầu,…) được nuôi cấy và chuyển gen mã hóa những yếu tố tái lập trình, từ đó tạo nên tế bào gốc đa tiềm năng cảm ứng. Những tế bào này có thể biệt hóa thành tất cả các loại tế bào trong cơ thể.
Nguồn: Delsing L., et al. (2020). Models of the blood-brain barrier using iPSC-derived cells. Molecular and Cellular Neuroscience, 107, 103533. https://doi.org/10.1016/j.mcn.2020.103533
Trong 20 năm qua, iPSC mang lại những hy vọng rất lớn trong y học tái tạo. iPSC có khả năng biệt hóa thành hầu hết các loại tế bào trong cơ thể, đồng thời có khả năng tăng sinh gần như vô hạn, dễ dàng chỉnh sửa gen. iPSC đã được ứng dụng rộng rãi để nghiên cứu sự phát triển và mô hình bệnh ở người, sàng lọc thuốc, phát triển các liệu pháp tế bào. Hiện tại, có khoảng hơn 50 thử nghiệm lâm sàng đang được thực hiện sử dụng iPSC. Tuy nhiên, để trở thành liệu pháp an toàn và có thể sản xuất quy mô lớn, các sản phẩm iPSC cần được kiểm soát nghiêm ngặt về sự biệt hóa thành tế bào đích, tính nhất quán trong sản xuất và sự giám sát chặt chẽ của cơ quan quản lý.
2. Liệu pháp Amchepry
Amchepry là những tế bào não có thể phát triển thành tế bào thần kinh sản sinh dopamine, có nguồn gốc từ iPSC, được phát triển bởi Sumitomo Pharma Co. Ltd. và Racthera Inc. Liệu pháp này được chỉ định cho các bệnh nhân Parkinson.
Bệnh Parkinson là một bệnh thần kinh tiến triển, do sự thoái hóa và mất đi của các tế bào não sản sinh dopamine, dẫn đến suy giảm chức năng vận động. Khác với các phương pháp điều trị bằng thuốc hiện nay chỉ tạm thời thay thế dopamine, Amchepry hướng đến khôi phục khả năng tự sản sinh dopamine của cơ thể. Trong một thử nghiệm lâm sàng giai đoạn I/II tại Bệnh viện Đại học Kyoto, 7 bệnh nhân được cấy ghép liệu pháp này vào não, sau đó theo dõi trong 24 tháng, chủ yếu tập trung vào đánh giá tính an toàn, kết quả phụ xác định hiệu quả của liệu pháp. Kết quả không ghi nhận tác dụng phụ nghiêm trọng, không hình thành khối u. Trong 6 bệnh nhân được đánh giá hiệu quả, 4-5 bệnh nhân có sự cải thiện về chức năng vận động, đồng thời tăng sự giải phóng dopamine trong não.
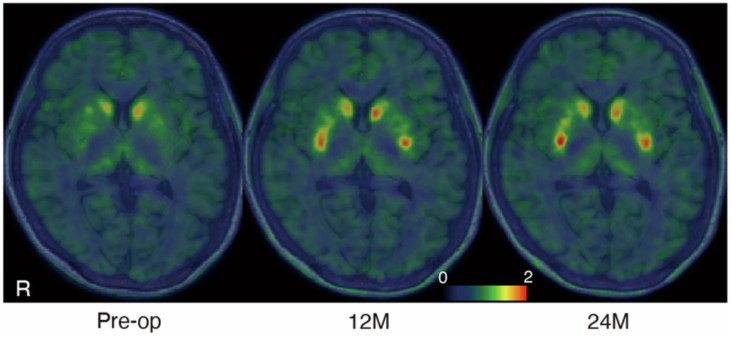
Fluorine-18-l-dihydroxyphenylalanine (18F-DOPA) được sử dụng để đánh giá quá trình tổng hợp dopamine. Hình ảnh bán định lượng 18F-DOPA được ghi nhận sau 80-90 phút tiêm thuốc, sự thay đổi màu sắc từ xanh đậm sang đỏ ở vùng nhân bèo hai bên cho thấy sự hấp thụ 18F-DOPA tăng lên, phản ánh sự tổng hợp dopamine bởi các tế bào được cấy ghép (Pre-Op: trước phẫu thuật, 12 M: 12 tháng, 24 M: 24 tháng).
Nguồn: Sawamoto N., et al. (2025). Phase I/II trial of iPS-cell-derived dopaminergic cells for Parkinson’s disease. Nature, 641(8064), 971-977. https://doi.org/10.1038/s41586-025-08700-0
3. Miếng dán cơ tim ReHeart
Công ty y học tái tạo Cuorips Inc. (tách ra từ Đại học Osaka) đã phát triển miếng dán cơ tim ReHeart có nguồn gốc từ iPSC, được đặt trên bề mặt tim của bệnh nhân suy tim để thúc đẩy sự hình thành các mạch máu mới và phục hồi chức năng tim.
Trong thử nghiệm lâm sàng, các tấm này được cấy ghép cho 8 bệnh nhân suy tim nặng (các phương pháp điều trị tiêu chuẩn như dùng thuốc hay phẫu thuật không cải thiện tình trạng bệnh). Kết quả đã xác nhận tính an toàn của sản phẩm và cho thấy hiệu quả bước đầu trên tất cả các bệnh nhân. Tình trạng mệt mỏi, khả năng chịu đựng khi vận động và hiệu suất tim tổng thể của bệnh nhân đều được cải thiện.
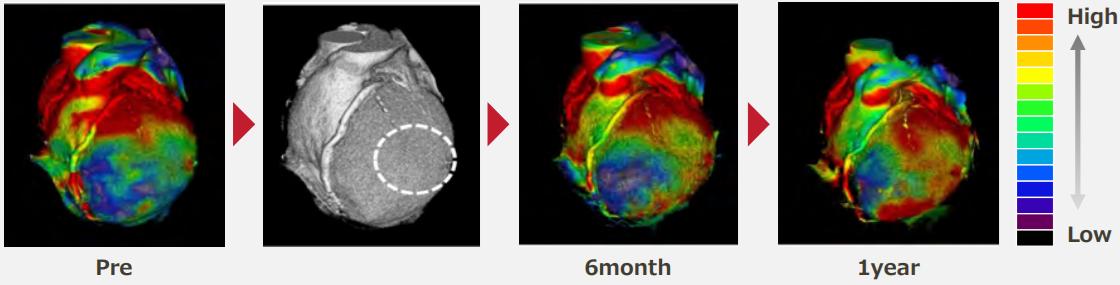
Tương ứng với vùng tim được cấy ghép ReHeart (vùng được đánh dấu tròn), sau 6 tháng và 1 năm, hoạt động co bóp tim được phục hồi, thể hiện với xung nhịp tăng lên (màu đỏ).
Nguồn: Thông tin sản phẩm từ Công ty Cuorips https://cuorips.co.jp/wp-content/themes/cuorips2019/inc/ir/pdf/Q_RSM%20E.pdf
4. Quyết định phê duyệt nhanh có điều kiện dành cho Amchepry và ReHeart
Với quyết định pháp lý mang tính lịch sử này, giới chức Y tế Nhật Bản đã cho phép thương mại hóa hai liệu pháp có nguồn gốc iPSC đầu tiên trên thế giới, đánh dấu sự chuyển mình của công nghệ iPSC từ thử nghiệm sang sản phẩm điều trị được phê duyệt.
Tuy nhiên, sự chấp thuận có điều kiện dành cho hai sản phẩm này dựa trên các nghiên cứu lâm sàng quy mô nhỏ, không có đối chứng, chỉ xác nhận tính an toàn và giả định hiệu quả của chúng. Các nhà sản xuất phải tiến hành các thử nghiệm lâm sàng sau khi đưa sản phẩm ra thị trường để xem xét chúng có thực sự mang lại lợi ích cho bệnh nhân hay không. Những thách thức mà hai sản phẩm này phải đối mặt như tỷ lệ đáp ứng của bệnh nhân, hiệu quả kéo dài bao lâu sau điều trị, khả năng tương thích miễn dịch, khả năng mở rộng quy mô và tính sẵn có (cả về sản xuất và nguồn lực y tế sử dụng sản phẩm),… Các dữ liệu sẽ được thu thập trong vòng 7 năm tới, và trong trường hợp hiệu quả không được chứng minh đầy đủ, Bộ Y tế, Lao động và Phúc lợi Nhật Bản sẽ thu hồi sự phê duyệt này.
Hệ thống phê duyệt nhanh của Nhật Bản được khởi động vào năm 2014 nhằm đẩy nhanh việc cung cấp các phương pháp điều trị mới, đã trở thành chủ đề tranh luận gay gắt. Trong các sản phẩm được phê duyệt có điều kiện theo hệ thống này, chưa có sản phẩm nào đến nay được phê duyệt chính thức, thậm chí một số sản phẩm đã bị loại bỏ sau khi không nhận được sự phê duyệt đầy đủ. Tạp chí Nature đã từng đăng một bài xã luận chỉ trích chính sách này của Nhật Bản, khi các sản phẩm được phê duyệt nhanh chỉ dựa trên tính an toàn mà chưa chứng minh được hiệu quả. Họ cho rằng Nhật Bản sẽ phải đối mặt với tình trạng tràn lan các liệu pháp không hiệu quả, khiến bệnh nhân đặt nhiều kỳ vọng nhưng không nhận được lợi ích lâm sàng thực tế. Đáng nói hơn, người bệnh đang phải chi trả số tiền lớn để tham gia vào một quá trình thực chất là thử nghiệm lâm sàng nhằm cung cấp dữ liệu cho doanh nghiệp – khoản chi phí mà lẽ ra các công ty phải tự chi trả thay vì để người bệnh hay quỹ bảo hiểm y tế gánh chịu.
TÀI LIỆU THAM KHẢO
1. Bản tin ngày 19/02/2026 của Tin tức Kyodo https://english.kyodonews.net/articles/-/70874
2. Bản tin ngày 20/02/2026 của Thời báo Nhật Bản https://www.japantimes.co.jp/news/2026/02/20/japan/science-health/ips-cell-based-products/
3. Sawamoto N., et al. (2025). Phase I/II trial of iPS-cell-derived dopaminergic cells for Parkinson’s disease. Nature, 641(8064), 971-977. https://doi.org/10.1038/s41586-025-08700-0
4. Thông tin sản phẩm từ Công ty Cuorips https://cuorips.co.jp/wp-content/themes/cuorips2019/inc/ir/pdf/Q_RSM%20E.pdf
5. (2015). Editorial: Stem the tide. Nature 528, 163–164. https://doi.org/10.1038/528163b
XEM THÊM
- Tế bào gốc đa tiềm năng https://ysinhtebao.com/tbg/tbg-da-tiem-nang
- Tế bào gốc đa tiềm năng cảm ứng: đại cương https://ysinhtebao.com/tbg/ipsc-dai-cuong, đặc điểm sinh học và ứng dụng https://ysinhtebao.com/tbg/ipsc-dac-diem-va-ung-dung
- Cập nhật 2025 về các liệu pháp tế bào gốc đa tiềm năng trong các thử nghiệm lâm sàng https://ysinhtebao.com/tin-tuc/cap-nhat-2025-thu-nghiem-lam-sang-psc
- Liệu pháp tế bào gốc đa tiềm năng: những yêu cầu cần thiết và tổng quan các dòng tế bào có thể sử dụng https://ysinhtebao.com/lp-tbg/nhung-yeu-cau-can-thiet-lieu-phap-psc
- Viện Y tế Quốc gia Hoa Kỳ (NIH) đề xuất chuyển hướng nghiên cứu tế bào gốc nhằm hạn chế sử dụng tế bào gốc phôi người https://ysinhtebao.com/tin-tuc/nih-chuyen-huong-nghien-cuu-hesc