Liệu pháp tế bào gốc đa tiềm năng: những yêu cầu cần thiết và tổng quan các dòng tế bào có thể sử dụng
1. Tế bào gốc đa tiềm năng
Một số loại tế bào gốc đa tiềm năng được chú ý nhiều nhất bao gồm:
- Tế bào gốc phôi (Embryonic Stem Cell – ESC) được thu từ phần nút phôi (inner cell mass) của túi phôi (blastocyst) ở người và động vật có vú. Phôi có thể thu nhận từ thụ tinh trong ống nghiệm (In Vitro Fertilization – IVF), chuyển nhân hoặc kích thích trinh sản. Tế bào gốc phôi người lần đầu tiên phân lập được và nghiên cứu năm 1998 bởi Thompson và cộng sự.
- Tế bào gốc đa tiềm năng cảm ứng (induced Pluripotent Stem Cell – iPSC) được thu nhận bằng cách tái lập trình tế bào chuyên hóa (như nguyên bào sợi, tế bào máu), sử dụng một số yếu tố phiên mã chỉ hoạt động ở giai đoạn phôi sớm để tái kích hoạt các gen duy trì đặc tính gốc của tế bào. Những nghiên cứu đầu tiên về iPSC ở người được công bố năm 2007 bởi các nhóm độc lập của Thompson và Yamanaka, tạo nên làn sóng mới trong nghiên cứu tế bào gốc và ứng dụng vào lâm sàng.
2. Tế bào gốc đa tiềm năng trong các thử nghiệm lâm sàng
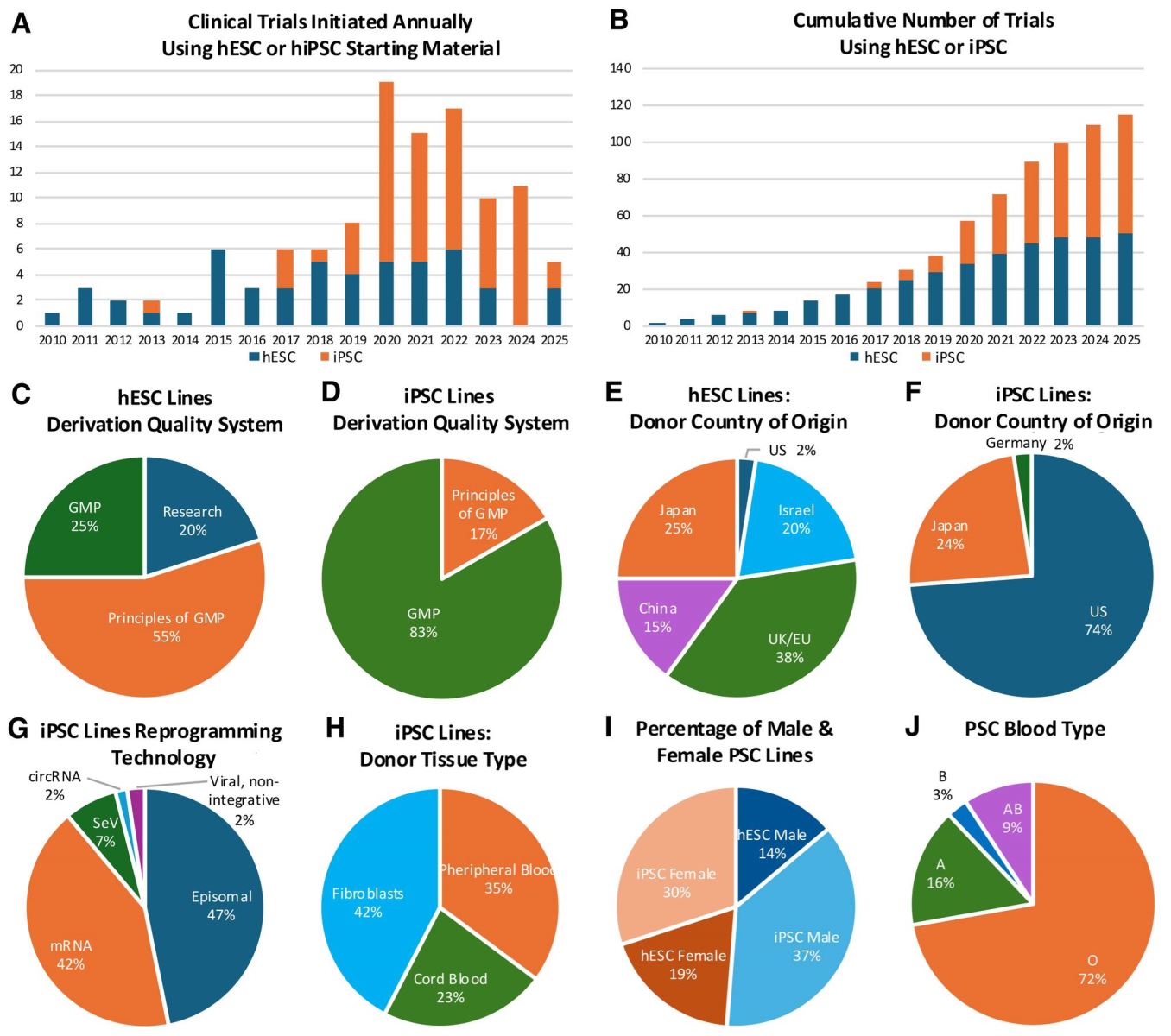
Trong một tổng hợp mới công bố trên tạp chí Stem Cell Reports, Carpenter và Ludwig cho biết đã có ít nhất 115 thử nghiệm lâm sàng sử dụng ít nhất 24 dòng PSC khác nhau (thực tế có thể nhiều hơn, vì đây chỉ là thông tin được công khai, một số thử nghiệm không tiết lộ dòng tế bào được sử dụng, hoặc sử dụng iPSC đặc thù), cùng với rất nhiều sản phẩm lâm sàng tiềm năng từ PSC đang ở giai đoạn phát triển ban đầu.
Những thử nghiệm lâm sàng sử dụng PSC được bắt đầu vào năm 2010, và luôn có những thử nghiệm mới đăng ký hàng năm tính đến 2025. Từ 2010 đến 2019, các ứng dụng lâm sàng của công nghệ PSC ưu tiên các dòng tế bào gốc phôi người (human Embryonic Stem Cell – hESC), gần đây thì số lượng nghiên cứu iPSC đã tăng trưởng mạnh mẽ - mặc dù đi sau 9 năm nhưng tổng số thử nghiệm đã đạt tương đương hESC.
Đối với các sản phẩm đồng loại có sẵn, việc xác định và lựa chọn dòng PSC phù hợp đóng vai trò quan trọng, tuy nhiên danh mục toàn diện về các dòng PSC có sẵn trên toàn thế giới để hỗ trợ việc lựa chọn dòng tế bào phục vụ lâm sàng vẫn chưa được tiếp cận đầy đủ. Carpenter và Ludwig đã xác định được 166 dòng PSC có vẻ phù hợp trong ứng dụng lâm sàng (40 dòng hESC và 126 dòng iPSC), cùng với 45 dòng PSC được tạo ra để sử dụng cho lâm sàng nhưng hiện không có sẵn hoặc chưa được xác nhận thông tin và khả năng tiếp cận. Phần lớn các dòng tế bào này thuộc sở hữu tư nhân và chưa được cấp phép sử dụng, thông tin thường khó tiếp cận. Khi chuyển dịch từ nghiên cứu cơ bản sang ứng dụng lâm sàng, nhu cầu về các dòng tế bào chất lượng cao đủ đáp ứng tiêu chuẩn ngày càng tăng, khả năng tiếp cận thông tin về các dòng tế bào có sẵn càng cần thiết để tiết kiệm thời gian và chi phí phát triển sản phẩm.
3. Những yêu cầu quan trọng cho dòng tế bào gốc đa tiềm năng có thể ứng dụng lâm sàng
Khi lựa chọn dòng PSC, cần cân nhắc những yếu tố quan trọng sau: (i) sự đồng ý của người hiến, (ii) hệ thống kiểm soát chất lượng, (iii) đặc điểm của dòng tế bào, (iv) sự cấp phép và quyền hạn sử dụng.
(i) Sự đồng ý của người hiến: Nguyên liệu tạo nên dòng PSC được thu thập dưới sự đồng ý của người hiến bằng văn bản, bao gồm thông tin về cách thức sử dụng mẫu hiến, khả năng được nhận chi phí từ việc sử dụng mẫu hiến, việc kiểm soát sử dụng dòng tế bào thu được,… (có thể tham khảo phiếu chấp thuận hiến mẫu của Hiệp hội Quốc tế về Nghiên cứu Tế bào gốc – ISSCR https://www.isscr.org/guidelines/appendices). Phiếu chấp thuận hiến mẫu cần được xem xét bởi một cơ quan đạo đức có thể đảm bảo quyền của người hiến (VD: Hội đồng Đạo đức). Cả 166 dòng PSC trong danh mục đều có sự đồng ý cung cấp của người hiến, bao gồm việc họ đã nắm được thông tin về việc mẫu của mình dùng để tạo ra dòng tế bào PSC, sử dụng chúng để thương mại hóa và đảm bảo rằng thông tin của người hiến được giữ bí mật.
(ii) Hệ thống kiểm soát chất lượng và sự tuân thủ: Các dòng tế bào được tạo ra trong các phòng thí nghiệm đạt tiêu chuẩn Thực hành Sản xuất Tốt (Good Manufacturing Practice - GMP), hoặc tuân thủ nguyên tắc GMP (phòng thí nghiệm chưa đạt GMP nhưng tuân thủ các yêu cầu theo tiêu chuẩn GMP), tuy nhiên những dòng PSC được tạo ra rất sớm nhiều năm trước trong điều kiện nghiên cứu vẫn có thể được sử dụng, khi thông tin về nguyên vật liệu và quy trình để tạo ra chúng đủ cho phép áp dụng các chiến lược giảm thiểu rủi ro và được cơ quan quản lý chấp nhận sử dụng trong các thử nghiệm lâm sàng. Khi xem xét việc tuân thủ quy định về kiểm soát chất lượng (như sàng lọc mẫu người hiến, các xét nghiệm đánh giá cho dòng PSC, điều kiện nuôi cấy,…) cần lưu ý đến yêu cầu cụ thể khác nhau giữa các khu vực pháp lý, khi các quy định tại Hoa Kỳ, châu Âu hay Nhật Bản có thể khác nhau.
(iii) Đặc điểm của dòng tế bào: Các dòng PSC cần đảm bảo khả năng biệt hóa đúng hướng và duy trì ổn định đặc tính di truyền. Khả năng biệt hóa của PSC được xác nhận bằng nuôi cấy in vitro và đánh giá biểu hiện gen, không cần thiết phải đánh giá in vivo qua việc tạo u quái. Đặc tính di truyền cần được đánh giá bằng một số phương pháp như phân tích nhiễm sắc thể, giải trình tự gen (việc giải trình tự gen được khuyến khích với các dòng tế bào được nuôi cấy dài ngày và iPSC, do chúng có khả năng tích lũy đột biến gen). Ngoài ra, các đặc điểm khác có thể ảnh hưởng đến việc lựa chọn dòng PSC như nhóm máu, giới tính, biểu hiện kháng nguyên bạch cầu người (Human Leukocyte Antigen – HLA), xét nghiệm tác nhân ngoại lai,…
(iv) Sự cấp phép và quyền hạn sử dụng: Sự hiểu rõ về quyền sở hữu trí tuệ và các quyền lợi vật chất liên quan đến dòng tế bào là rất quan trọng và cần được tiến hành thẩm định kỹ lưỡng. Cần lưu ý rằng bằng sáng chế không được cấp trên toàn cầu mà chỉ được đăng ký trong nước và có thời hạn nhất định, ngược lại quyền sở hữu vật liệu tồn tại vô thời hạn, và các dòng tế bào được cấp phép từ chủ sở hữu/nhà cung cấp bất kể tình trạng sở hữu trí tuệ. Vì vậy khi lập kế hoạch địa điểm thử nghiệm lâm sàng hoặc thương mại hóa, người ta cần xem xét các yêu cầu về thẩm quyền đối với việc cấp phép và quyền hạn sử dụng tự do, từ đó xin cấp phép trước khi sử dụng thông qua các thỏa thuận chuyển giao để đảm bảo sự tuân thủ.
4. Kết luận
Trong quá trình phát triển các sản phẩm có nguồn gốc từ tế bào gốc đa tiềm năng ở người, việc lựa chọn dòng PSC làm nguyên liệu ban đầu là một quyết định quan trọng. Việc hiểu rõ đặc tính dòng tế bào, hệ thống kiểm soát chất lượng, yêu cầu pháp lý,… là những yếu tố then chốt, đặc biệt khi có ý định thương mại hóa sản phẩm. Những thông tin về các dòng PSC sẵn có giúp tiết kiệm thời gian, công sức và chi phí trong việc đưa các sản phẩm này đến tay bệnh nhân. Danh mục 166 dòng PSC có thể ứng dụng lâm sàng và những yếu tố kể trên là nguồn tài nguyên quý giá cho cộng đồng cho cộng đồng nghiên cứu tế bào gốc khi họ tiến tới các ứng dụng lâm sàng, danh mục này có thể tìm hiểu tại https://www.cell.com/stem-cell-reports/fulltext/S2213-6711(25)00345-5.
TÀI LIỆU THAM KHẢO
Carpenter M. K., and Ludwig T. E. (2025). Pluripotent stem cell lines available for use in clinical applications: A comprehensive overview. Stem Cell Reports. DOI: https://doi.org/10.1016/j.stemcr.2025.102741








