FDA bổ sung cảnh báo tác dụng phụ viêm ruột liên quan đến sản phẩm CAR-T Carvykti
Carvykti (ciltacabtagene autoleucel) là một loại liệu pháp tế bào CAR-T được phát triển bởi hãng Janssen Biotech, sử dụng trong điều trị bệnh đa u tủy xương. Đây là những tế bào lympho T của chính bệnh nhân được cải biến di truyền để mang thụ thể nhân tạo đặc hiệu với kháng nguyên trưởng thành tế bào B (B-cell maturation antigen –– BCMA) có mặt trên bề mặt tế bào đa u tủy xương, nhờ đó có thể phát hiện dễ dàng hơn và tiêu diệt những tế bào ác tính này. Carvykti là một trong hai sản phẩm CAR-T hướng đích BCMA, và là một trong bảy sản phẩm CAR-T nói chung đã được Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (US Food and Drug Administration – US FDA) phê duyệt.
Ngày 10 tháng 10 năm 2025, FDA đã phê duyệt nhãn thuốc Carvykti được cập nhật bao gồm cảnh báo đặc biệt (cảnh báo được đóng khung – Boxed Warning) về bệnh viêm ruột liên quan đến tế bào hiệu lực miễn dịch (immune effector cell-associated enterocolitis –– IEC-EC). Việc thay đổi nhãn được thực hiện sau những báo cáo từ thử nghiệm lâm sàng và tác dụng phụ ghi nhận được khi sản phẩm lưu hành trên thị trường.
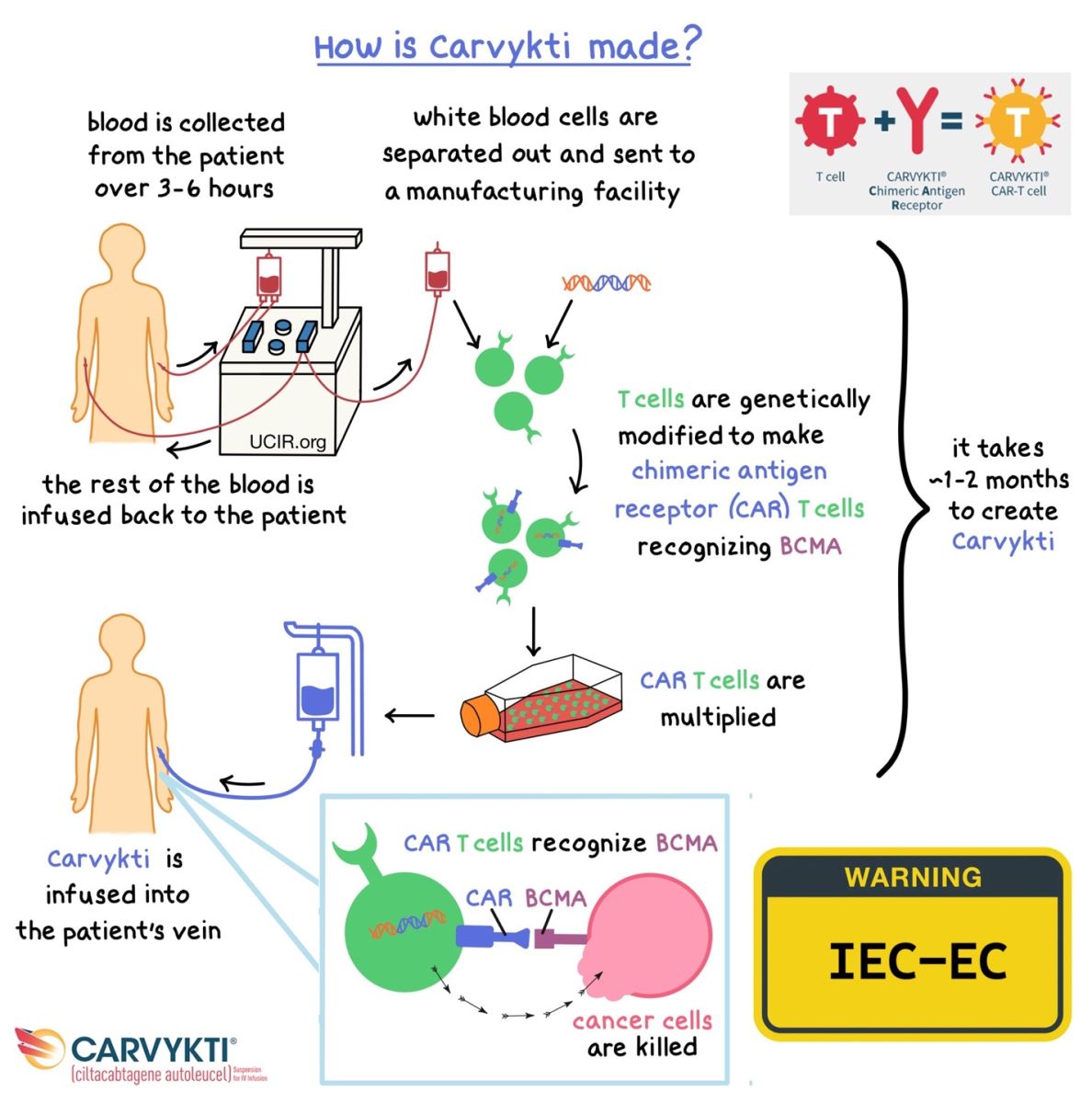
IEC-EC là tình trạng viêm ruột nghiêm trọng có thể xảy ra sau một số liệu pháp miễn dịch, bao gồm liệu pháp tế bào CAR-T. Bệnh nhân mắc IEC-EC sau khi điều trị bằng Carvykti có biểu hiện tiêu chảy kéo dài hoặc nghiêm trọng , đau bụng và sụt cân, một số trường hợp mất khả năng tiêu hóa mà cần truyền dinh dưỡng qua đường tĩnh mạch. Trong những trường hợp nghiêm trọng, tác dụng phụ này có liên quan đến tử vong do thủng ruột và nhiễm trùng huyết. Việc quản lý IEC-EC thường bao gồm chăm sóc hỗ trợ, dinh dưỡng qua đường tiêm truyền nếu cần và liệu pháp ức chế miễn dịch, chẳng hạn như corticosteroid.
FDA cho biết IEC-EC đã được ghi nhận sau vài tuần đến vài tháng kể từ khi truyền. Đối với những bệnh nhân mắc tình trạng này mà không đáp ứng điều trị, cần cân nhắc thực hiện thêm các xét nghiệm để loại trừ u lympho tế bào T đường tiêu hóa, căn bệnh đã được báo cáo trong quá trình đưa thuốc ra thị trường. Ngoài cảnh báo đặc biệt trên, những thay đổi về nhãn còn mở rộng sang các cảnh báo, biện pháp phòng ngừa và phản ứng có hại – phần kinh nghiệm sau khi đưa thuốc ra thị trường trong thông tin kê đơn và hướng dẫn dùng thuốc.
Mặc dù vậy, FDA nhấn mạnh rằng lợi ích tổng thể của Carvykti vẫn lớn hơn những rủi ro tiềm ẩn đối với mục đích sử dụng đã được phê duyệt, bao gồm cả lợi ích sống sót tổng thể ở những bệnh nhân được điều trị bằng Carvykti. Dữ liệu sống sót tổng thể từ thử nghiệm CARTITUDE-4 đã được cập nhật vào thông tin kê đơn, với kết quả Carvykti mang lại lợi ích đáng kể về mặt thống kê so với điều trị tiêu chuẩn ở bệnh nhân đa u tủy tái phát và kháng lenalidomide (với thời gian theo dõi trung bình khoảng 33,6 tháng).
TÀI LIỆU THAM KHẢO
- “FDA bổ sung cảnh báo đặc biệt về viêm ruột liên quan đến tế bào miễn dịch vào thuốc CAR-T”, bản tin Medscape ngày 13/10/2025 https://www.medscape.com/viewarticle/fda-adds-boxed-warning-immune-effector-cell-associated-2025a1000rkg
- “FDA chấp thuận thay đổi nhãn bao gồm cảnh báo đặc biệt về bệnh viêm ruột liên quan đến tế bào miễn dịch sau khi điều trị bằng Ciltacabtagene Autoleucel (CARVYKTI, Janssen Biotech, Inc.)”, thông báo của FDA ngày 10/10/2025 https://www.fda.gov/safety/medical-product-safety-information/fda-approves-labeling-changes-include-boxed-warning-immune-effector-cell-associated-enterocolitis
XEM THÊM
- Cải biến di truyền giúp tăng cường hiệu quả liệu pháp tế bào miễn dịch trong điều trị ung thư: TCR-T và CAR-T https://www.facebook.com/share/p/18mRyiUvJb/
- Liệu pháp CAR-T – bước đột phá của liệu pháp tế bào trong điều trị ung thư https://www.facebook.com/share/p/1ACHF2K2wY/
- FDA loại bỏ các chiến lược đánh giá và giảm thiểu rủi ro cho liệu pháp CAR-T tự thân trong điều trị ung thư https://www.facebook.com/share/p/19ZgegsBHs/