Thử nghiệm lâm sàng điều trị bại não bằng tế bào gốc từ răng sữa sẽ sớm khởi động tại Hoa Kỳ
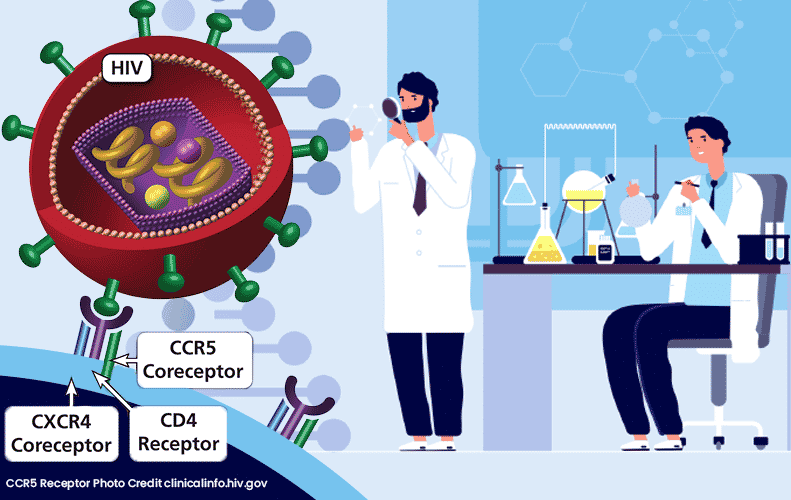
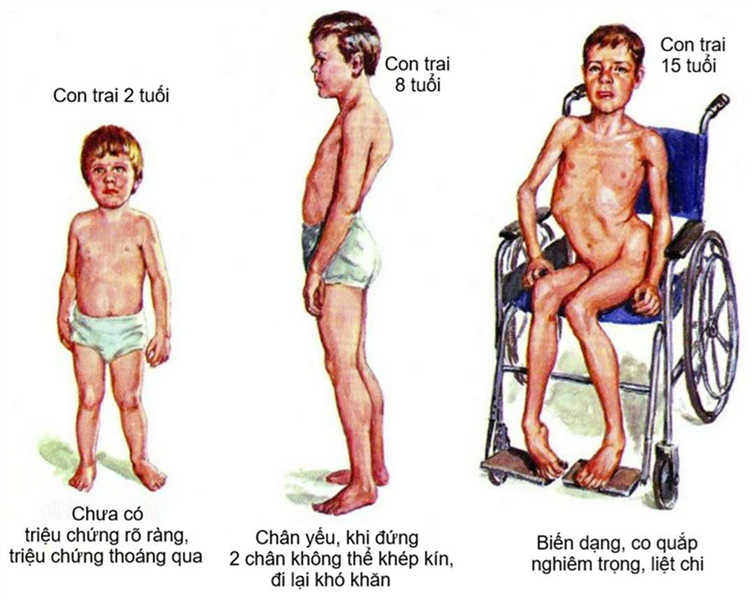
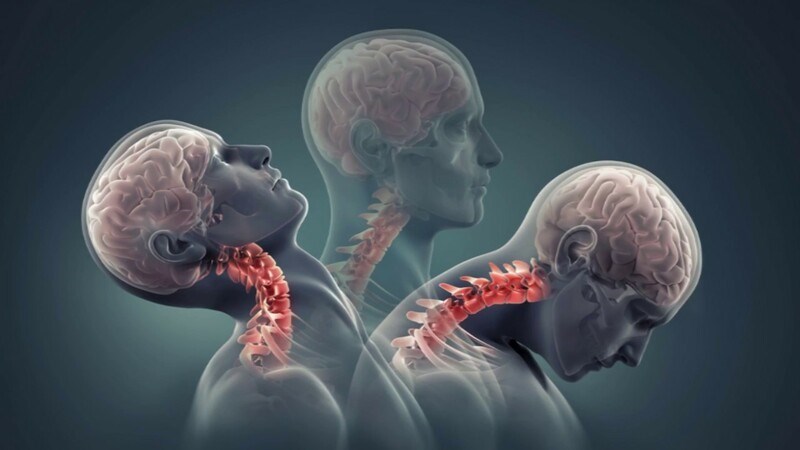
Bại não là một nhóm tình trạng bệnh lý do tổn thương não trước, trong và sau sinh cho đến dưới 5 tuổi. Các tổn thương não này không tiến triển theo thời gian, gây nên đa tàn tật về vận động, tinh thần, giác quan và hành vi, gây nên gánh nặng cho bản thân trẻ và gia đình, xã hội. Tỷ lệ bại não vào khoảng 2/1.000 trẻ mới sinh. Phương pháp điều trị tiêu chuẩn tập trung vào kiểm soát các triệu chứng thông qua vật lý trị liệu, thuốc men và các thiết bị hỗ trợ, tuy nhiên không có phương pháp điều trị nào trong số này có thể sửa chữa tổn thương não bộ.
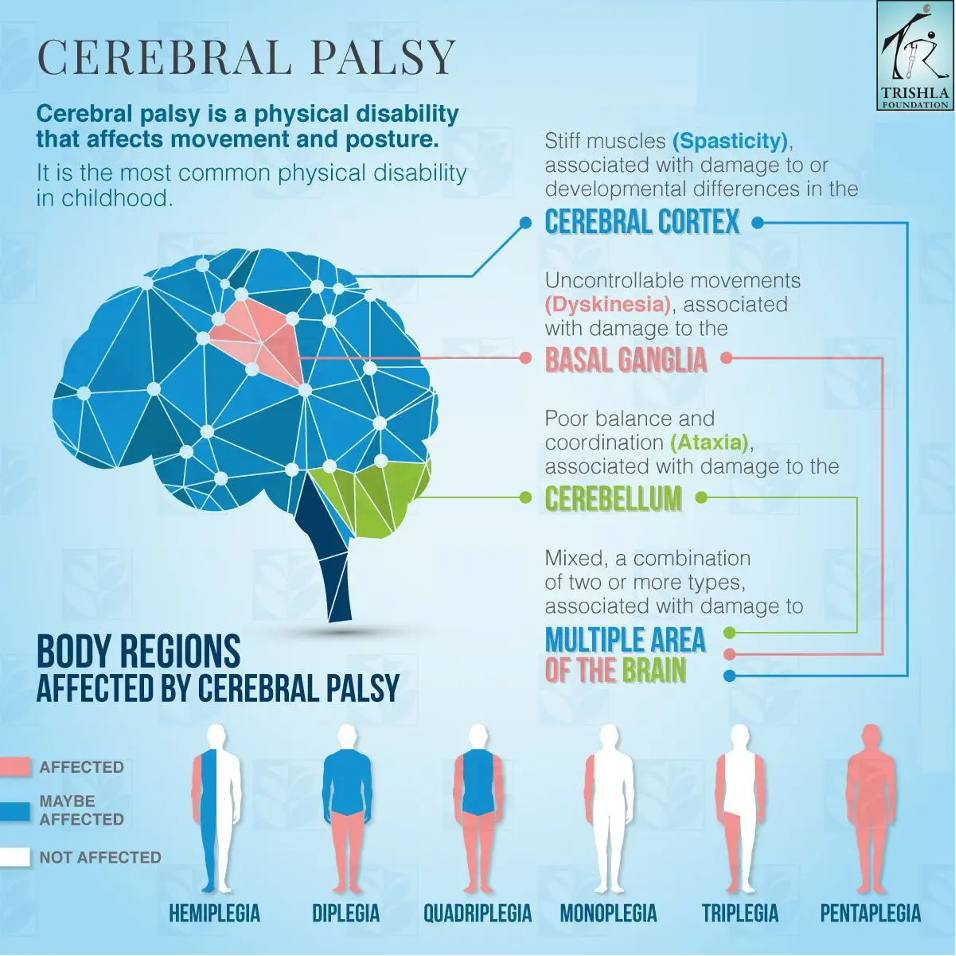
Nguồn: https://www.christopherreeve.org/todays-care/living-with-paralysis/health/causes-of-paralysis/cerebral-palsy/
Tháng 02/2026 tại Hoa Kỳ, sự ra đời của Kidswell USA (hợp tác giữa Treehill Partners và công ty Kidswell Bio đến từ Nhật Bản) đã mang đến sự quan tâm đặc biệt của các gia đình có trẻ em bại não. Kidswell Bio là một công ty sinh dược phẩm được thành lập tại Nhật Bản năm 2001 với tên gọi Gene Techno Science, hoạt động chủ yếu trong lĩnh vực nghiên cứu và phát triển các loại thuốc tương tự sinh học (biosimilar). Đến năm 2021, Gene Techno Science đổi tên thành như Kidswell Bio để tập trung vào các bệnh nhi và y học tái tạo, điển hình là phát triển các sản phẩm từ tế bào gốc tủy răng sữa. Họ đã hợp tác cùng Treehill Partners để thành lập nên công ty Kidswell USA tại Hoa Kỳ, nhờ đó có thể làm việc trực tiếp với Cục quản lý Thực phẩm và Dược phẩm (the U.S. Food and Drug Administration – FDA) để thiết kế các thử nghiệm lâm sàng, hợp tác với các viện nghiên cứu Hoa Kỳ và tuyển chọn bệnh nhân thông qua các kênh được quản lý chặt chẽ và hợp pháp. Mục tiêu trước mắt của họ là sớm phát triển một chương trình trị liệu tế bào mới cho bệnh bại não ở trẻ em, sử dụng các tế bào gốc từ tủy răng sữa.
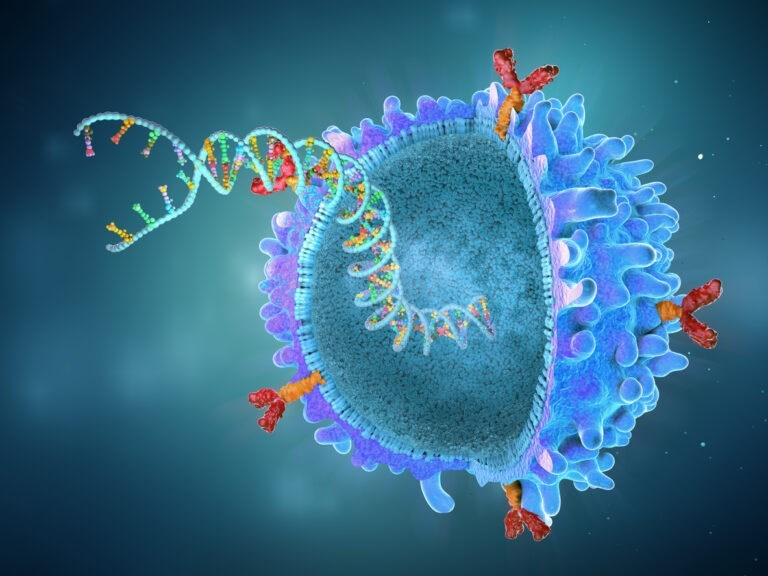
Tế bào gốc từ tủy răng sữa (Stem cells from human exfoliated deciduous teeth – SHED) được thu thập từ răng sữa rụng tự nhiên từ trẻ em, có thể được nuôi cấy tăng sinh trong phòng thí nghiệm để đạt số lượng lớn, đồng thời mang nhiều đặc điểm tương tự tế bào gốc trung mô (Mesenchymal stem/stromal cell – MSC) phân lập từ tủy xương, mô mỡ, dây rốn. Một số lý do khiến SHED thu hút sự chú ý là nguồn gốc mào thần kinh, đồng thời thể hiện những hoạt tính sinh học trong các mô hình thần kinh. Với mục tiêu điều trị bại não, SHED được kỳ vọng giải quyết các tác động thứ phát của tổn thương não sớm (như viêm mạn tính hay rối loạn tín hiệu thần kinh), hơn là tái tạo lại tổn thương đó. Lợi ích lâm sàng có đạt được hay không đòi hỏi các thử nghiệm trên người được thiết kế chặt chẽ và cẩn thận, quá trình đó đang được tiếp diễn. Để những liệu pháp như vậy trở thành một sản phẩm được cấp phép chính thức cần trải qua nhiều năm nghiên cứu bài bản, với rất nhiều giai đoạn như: thử nghiệm lâm sàng giai đoạn I/II đánh giá độ an toàn, thử nghiệm lâm sàng giai đoạn II/III đánh giá hiệu quả, xem xét và phê duyệt,…
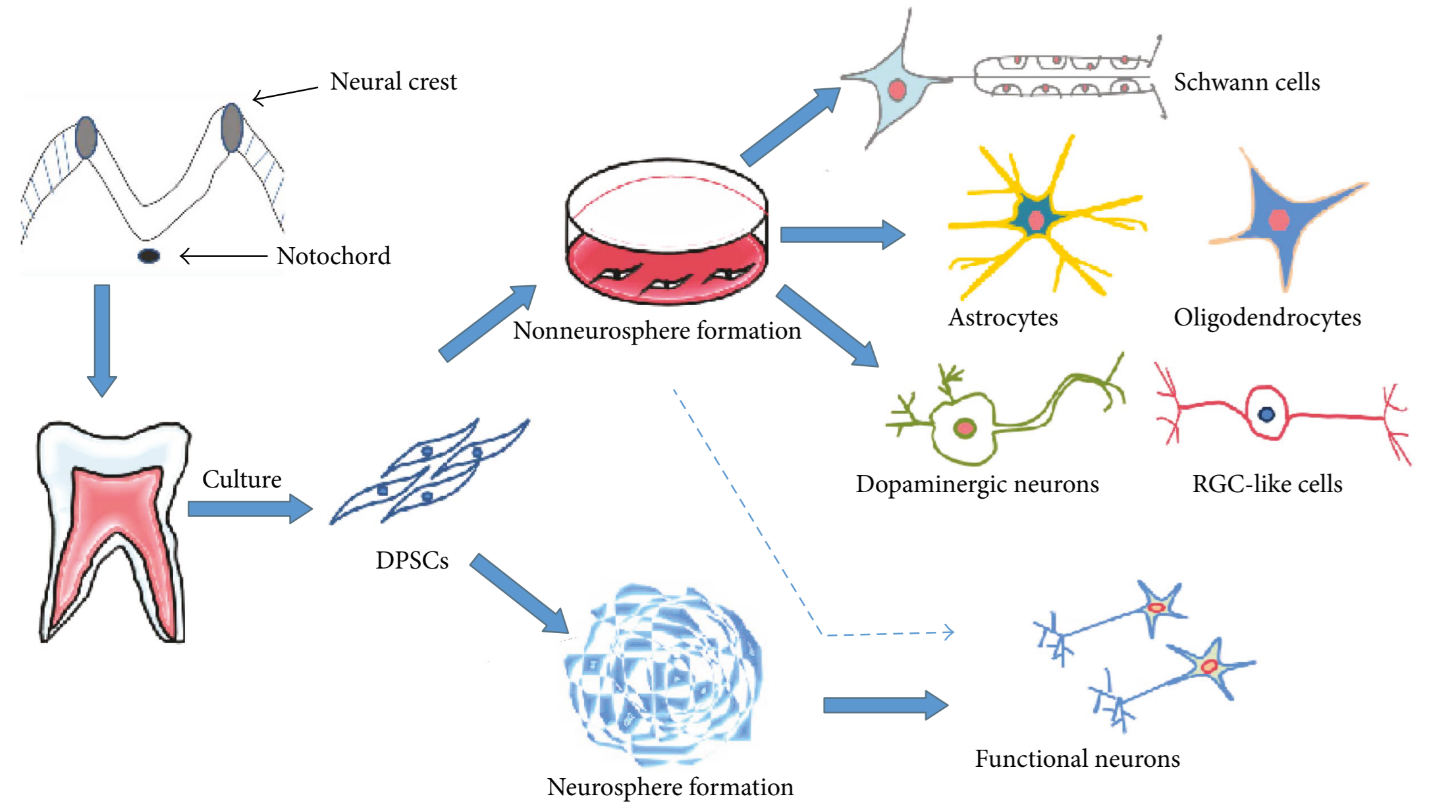
Nguồn: Luo L., et al. (2018). Potential roles of dental pulp stem cells in neural regeneration and repair. Stem cells international, 2018(1), 1731289. https://doi.org/10.1155/2018/1731289
Kidswell Bio không phải là đơn vị đầu tiên phát triển liệu pháp tế bào trong điều trị bại não ở Hoa Kỳ. Nhóm nghiên cứu tại Đại học Duke đã công bố các nghiên cứu đánh giá việc truyền tế bào gốc máu cuống rốn tự thân ở trẻ em bại não, với các dấu hiệu cải thiện vận động ở một số nhóm nhỏ. Các nhóm nghiên cứu khác cũng đã thử nghiệm với tế bào gốc trung mô tủy xương hoặc dây rốn.
Liệu pháp tế bào gốc để điều trị bại não vẫn đang phát triển. Mặc dù chưa có sản phẩm tế bào nào nhận được phê duyệt đầy đủ của FDA dành cho bệnh này, nhưng số lượng thử nghiệm lâm sàng ngày càng tăng cho thấy sự quan tâm ngày càng cao của cộng đồng khoa học.
TÀI LIỆU THAM KHẢO
Trang tin của Trung tâm Bệnh bại não Hoa Kỳ https://www.cerebralpalsycenter.com/news/kidswell-launches-effort-to-bring-cerebral-palsy-stem-cell-therapy-to-us/
Thông cáo báo chí ngày 16 tháng 2 năm 2026 của Kidswell Bio https://www.kidswellbio.com/Portals/0/resources/pdf/en/Topics/2026/20260216_01EN_8fgSyej9x.pdf