Liệu pháp tế bào Deramiocel làm chậm tiến triển bệnh loạn dưỡng cơ Duchenne
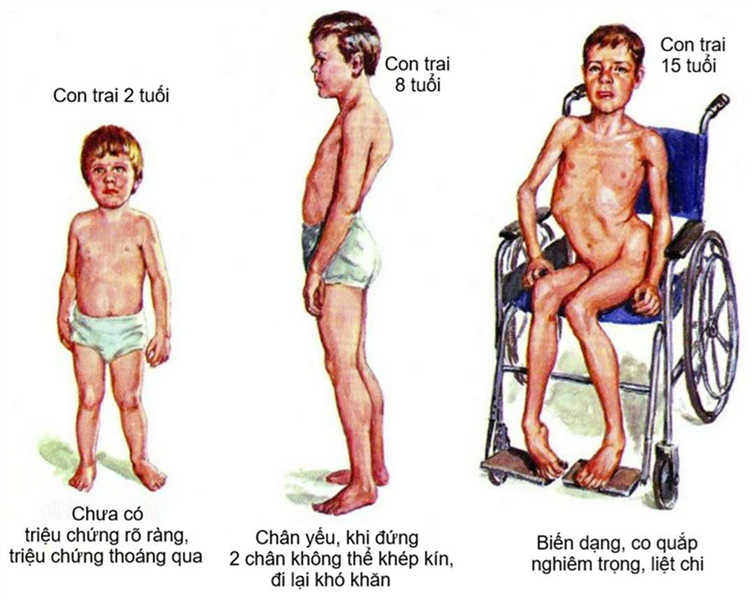
Loạn dưỡng cơ Duchenne là bệnh lý thần kinh cơ di truyền thường gặp nhất và để lại hậu quả nặng nề nhất. Đặc trưng của bệnh là các cơ teo dần, lâu ngày dẫn đến chức năng cơ suy giảm, cử động yếu dần, thậm chí có thể liệt ở nhóm cơ bị bệnh. Loạn dưỡng cơ Duchenne là một bệnh lý bẩm sinh, thường xuất hiện ngay sau sinh, thể hiện rõ nhất ở giai đoạn 2-5 tuổi, một số trường hợp đến tuổi thanh niên mới khởi phát.
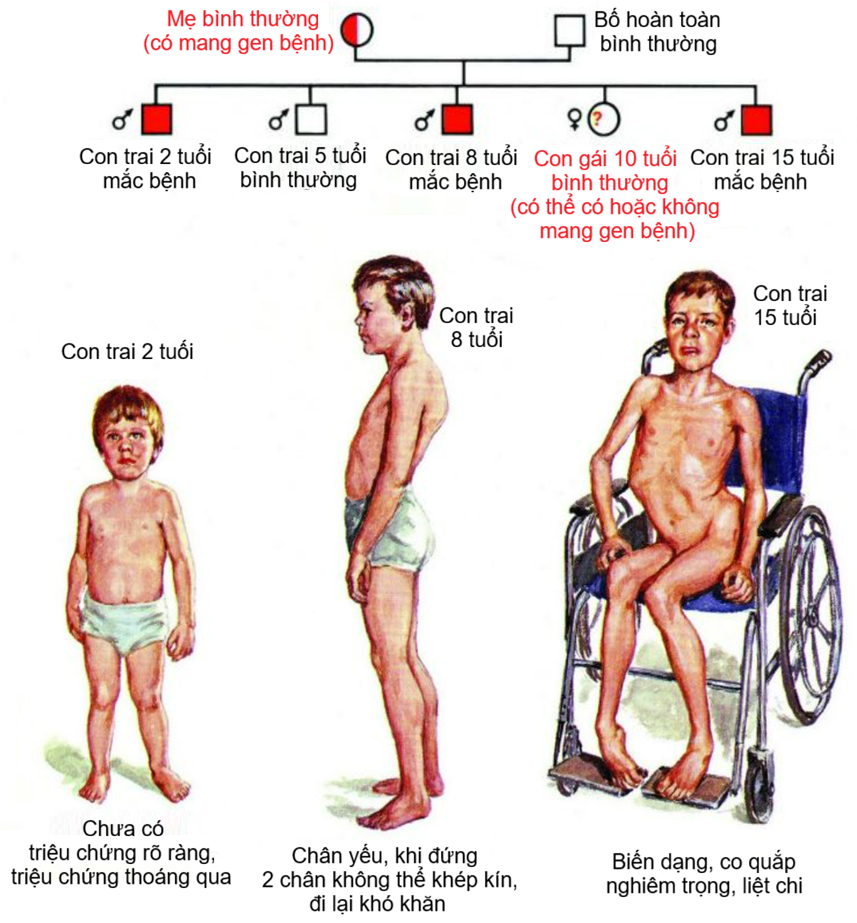
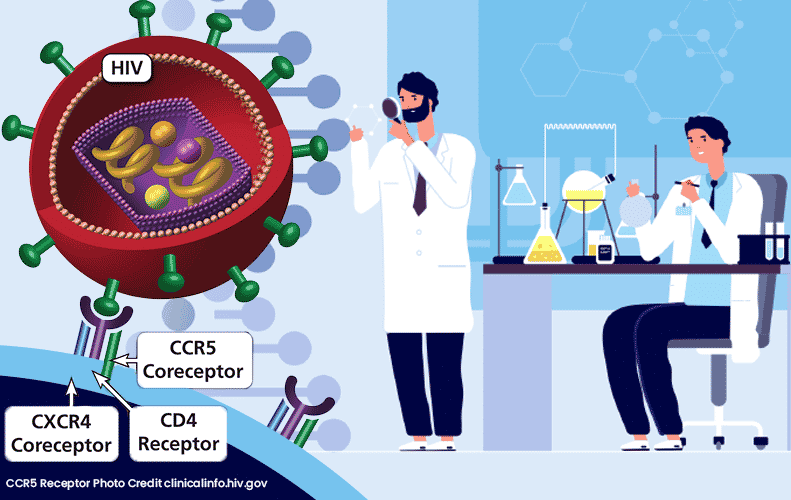
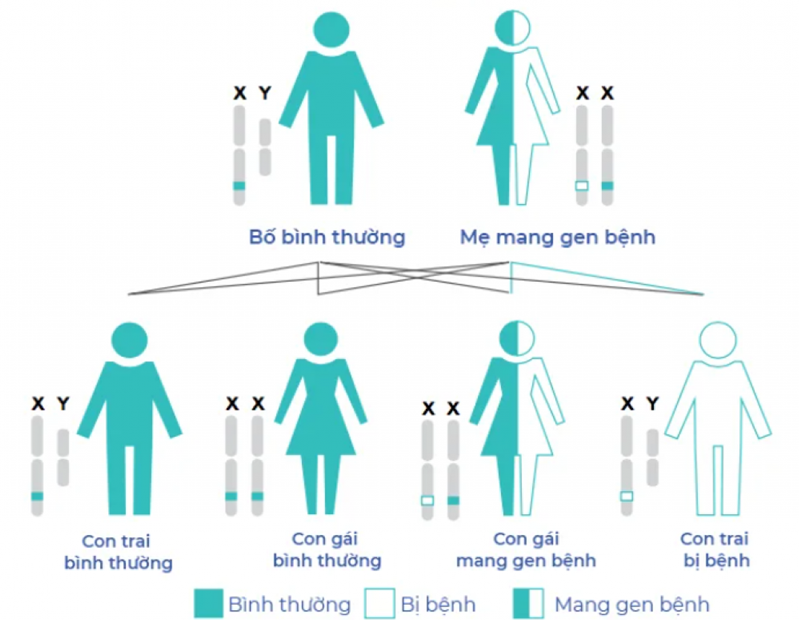
Nguyên nhân gây bệnh do đột biến gen DMD mã hóa dystrophin, một protein đảm bảo tính toàn vẹn của thoi cơ. Sự thiếu hụt protein dystrophin kích hoạt một loạt các tác động, bao gồm thoái hóa tiến triển cơ xương và cơ tim, phản ứng miễn dịch gây viêm và xơ hóa làm suy giảm khả năng phục hồi, từ đó sự suy giảm chức năng liên tục có thể dẫn đến các biến cố tim mạch đe dọa tính mạng. Do gen DMD nằm trên nhiễm sắc thể giới tính X và không có vùng tương đồng trên Y, bệnh chủ yếu xảy ra ở bé trai (tỷ lệ khoảng 1/3.500), có ghi nhận rải rác ở bé gái nhưng tỷ lệ rất thấp.
Hãng Capricor Therapeutics đã phát triển một liệu pháp tế bào có tên Deramiocel để điều trị cho những bệnh nhân loạn dưỡng cơ Duchenne giai đoạn nặng. Deramiocel (CAP-1002) là một liệu pháp dựa trên các tế bào cầu tim (cardiosphere-derived cell, CDCs) từ người hiến, hoạt động bằng cách tiết ra exosome (các túi ngoại bào) để điều chỉnh chức năng của đại thực bào, giúp giảm viêm và xơ hóa trong các mô cơ bị tổn thương. Tháng 7 năm 2025, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (The U.S. Food and Drug Administration – FDA) đã từ chối đơn xin cấp phép sản phẩm sinh học này, do bằng chứng lâm sàng chưa đầy đủ từ thử nghiệm HOPE-2 và yêu cầu thêm dữ liệu. Capricor Therapeutics đã tiếp tục gửi lên FDA kết quả thử nghiệm HOPE-3 vào cuối năm 2025, dự kiến FDA sẽ đưa ra quyết định xét duyệt trước ngày 22/08/2026.
Trong một phiên trình bày khoa học tại hội nghị thường niên của Học viện Thần kinh học Hoa Kỳ diễn ra vào ngày 18-22/04/2026, nhóm nghiên cứu thuộc Bệnh viện Nhi Arkansas và Đại học Khoa học Y tế Arkansas đã trình bày kết quả thử nghiệm HOPE-3. Đây là thử nghiệm lâm sàng giai đoạn III, đa trung tâm, phân nhóm ngẫu nhiên, mù đôi, có đối chứng giả dược (https://clinicaltrials.gov/study/NCT05126758), với 106 bệnh nhân nam mắc bệnh Duchenne giai muộn được phân nhóm ngẫu nhiên để truyền Deramiocel (54 người) và giả dược (52 người) với tần suất 3 tháng/lần trong 12 tháng (tổng 4 lần). Khi nhập viện, bệnh nhân có điểm chỉ số Hiệu suất chi trên phiên bản 2.0 (Performance of Upper Limb 2.0, PUL 2.0) ít nhất là 2, và phân suất tống máu thất trái (Left Ventricular Ejection Fraction, LVEF – phản ánh tỷ lệ phần trăm máu được tâm thất trái bơm ra nuôi cơ thể sau mỗi nhịp đập, ở người bình thường là 50-70%) ít nhất là 35%. Khoảng 90% bệnh nhân đang sử dụng thuốc tim mạch và hơn 75% được chẩn đoán lâm sàng mắc bệnh cơ tim. Tất cả bệnh nhân đều được dùng phác đồ corticosteroid ổn định trong suốt nghiên cứu.
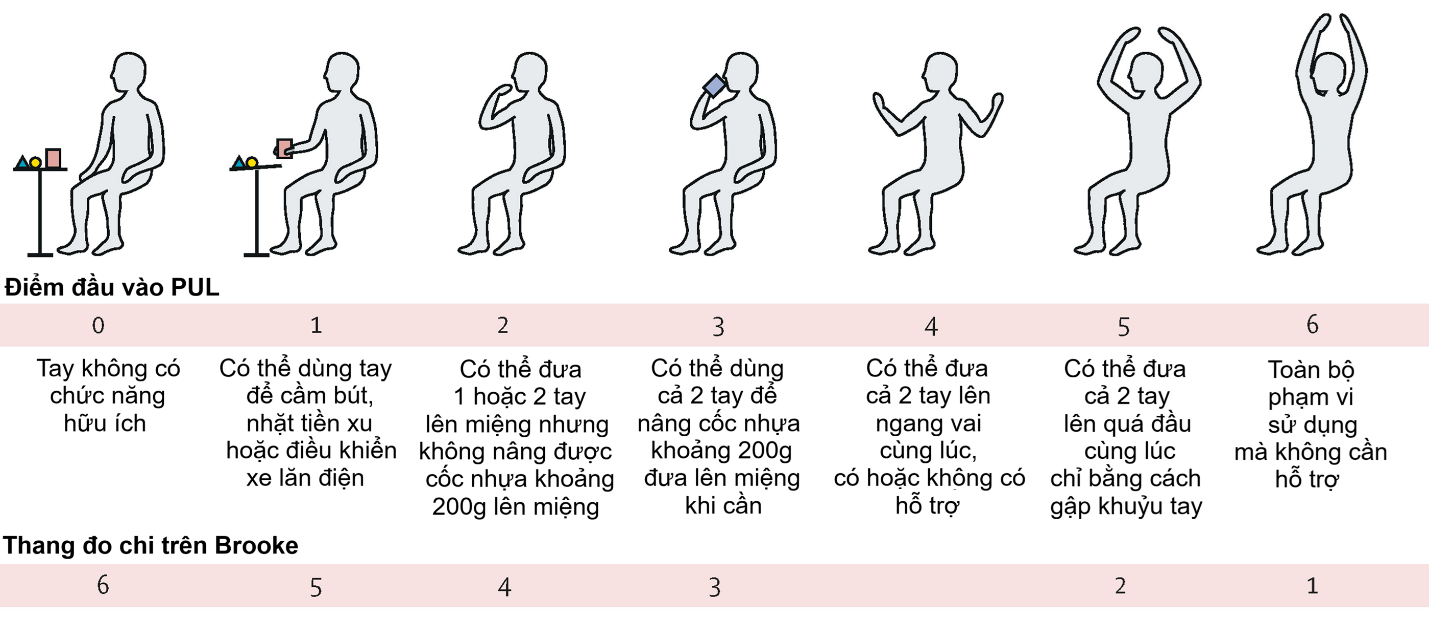
Kết quả cho thấy so với giả dược, điều trị bằng Deramiocel làm chậm quá trình suy giảm chức năng chi trên 54% (đo bằng thang PUL 2.0), và làm chậm quá trình suy giảm chức năng tim 91% (đo bằng LVEF). Những chỉ số phụ như khả năng tự ăn, điểm số “ăn 10 miếng” trong bài kiểm tra video đo lường khả năng ăn uống ổn định tại nhà cũng đều có sự cải thiện rõ rệt tới 65-83%. Đồng thời, hồ sơ an toàn tổng thể của Deramiocel tương đương với giả dược, các tác dụng phụ từ nhẹ đến trung bình bao gồm những triệu chứng giống cúm thoáng qua và tự khỏi trong vòng 24-48 giờ sau khi truyền thuốc.
Rõ ràng, liệu pháp tế bào này đã làm chậm tiến triển bệnh với lợi ích ở chi trên và bệnh tim mạch, cải thiện tính độc lập và chất lượng cuộc sống ở những bệnh nhân loạn dưỡng cơ Duchenne bị ảnh hưởng nặng. Những kết quả này mang lại hy vọng rất lớn cho các gia đình có người mắc bệnh này. Hãng Capricor Therapeutics cũng đã gửi các dữ liệu thử nghiệm đến FDA và hy vọng sẽ sớm được cấp phép cho liệu pháp này.
NGUỒN THÔNG TIN – TÀI LIỆU THAM KHẢO
- Tin tức MedPage Today https://www.medpagetoday.com/meetingcoverage/aan/120956
- Thông cáo báo chí của Capricor Therapeutics https://www.capricor.com/investors/news-events/press-releases/detail/338/capricor-therapeutics-announces-establishment-of-new-pdufa
- Tin tức y tế Cardiology Advisor https://www.thecardiologyadvisor.com/news/deramiocel-slows-dmd-progression-in-phase-3-trial/
- McDonald C., et al. (2022). Repeated intravenous cardiosphere-derived cell therapy in late-stage Duchenne muscular dystrophy (HOPE-2): a multicentre, randomised, double-blind, placebo-controlled, phase 2 trial. The Lancet, 399, 1049-1058. https://doi.org/10.1016/S0140-6736(22)00012-5