Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh (P2)
1. Tế bào giết tự nhiên (Natural killer cell – NK cell)
Tế bào NK là một nhóm nhỏ các tế bào lympho trong hệ miễn dịch bẩm sinh, chiếm khoảng 5-15% tổng số tế bào đơn nhân trong máu ngoại vi (peripheral blood mononuclear cell – PBMC). Khác với tế bào lympho T, NK không biểu hiện CD3 và không có thụ thể tế bào T (T cell receptor – TCR), nhưng biểu hiện CD56. Chúng tham gia vào việc tiêu diệt tế bào khối u, tế bào bị nhiễm trùng và ký sinh trùng. Chức năng của chúng được điều chỉnh bởi một loạt các thụ thể kích hoạt và ức chế phức tạp có thể phân biệt giữa các tế bào khỏe mạnh và các tế bào bất thường.
NK có các thụ thể với phạm vi rộng trong việc nhận biết các tế bào thiếu biểu hiện phức hợp tương thích mô chính (Major Histocompatibility Complex – MHC), khác với tế bào T chỉ có một TCR duy nhất và cần được kích hoạt bởi peptide liên kết với MHC do tế bào trình diện kháng nguyên (Antigen-Presenting Cell – APC) trình bày. Đồng thời, tế bào NK được kích hoạt để tạo ra hiệu quả chống ung thư toàn diện, tác động đến hầu hết mọi bước trong chu trình miễn dịch ung thư. Chúng tiết ra các hạt ly giải (chứa perforin và granzyme) để gây độc tế bào đích, quá trình đó cũng đồng thời giải phóng kháng nguyên tế bào ung thư và tạo điện kiện kích thích APC. NK tham gia vào hàng loạt các cơ chế thu hút, kích hoạt tế bào T, thậm chí đóng vai trò APC để trình diện một số kháng nguyên nhất định cho tế bào T CD8+. Bên cạnh đó, NK tiêu diệt tế bào u độc lập với sự biểu hiện MHC, tạo ra hiệu ứng bổ sung hoàn hảo cho tế bào T.
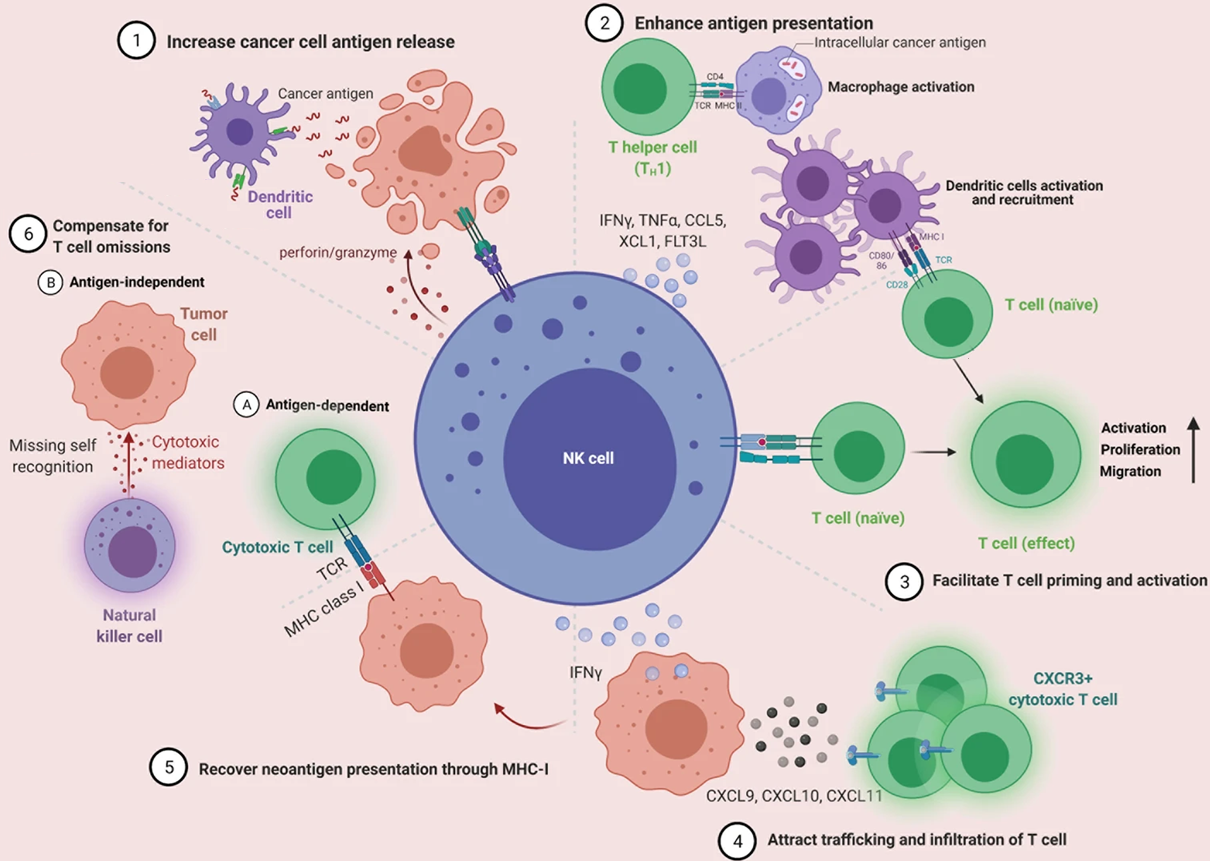
Các tế bào NK được hoạt hóa làm tăng sự giải phóng kháng nguyên của tế bào ung thư, tăng cường trình diện kháng nguyên, tạo điều kiện thuận lợi cho việc kích thích và hoạt hóa tế bào T, thu hút sự di chuyển và xâm nhập của tế bào T, phục hồi sự trình diện kháng nguyên mới và bù đắp cho sự thiếu hụt tế bào T.
Nguồn: Wang M., et al. (2022). Natural killer cell awakening: Unleash cancer-immunity cycle against glioblastoma. Cell Death & Disease, 13 (7), 588.
2. Giải pháp CAR-NK
Do các cơ chế kích hoạt đa dạng như trên, tế bào NK là mục tiêu hấp dẫn cho liệu pháp thụ thể kháng nguyên khảm (Chimeric Antigen Receptor – CAR), khắc phục một số hạn chế so với tế bào CAR-T.
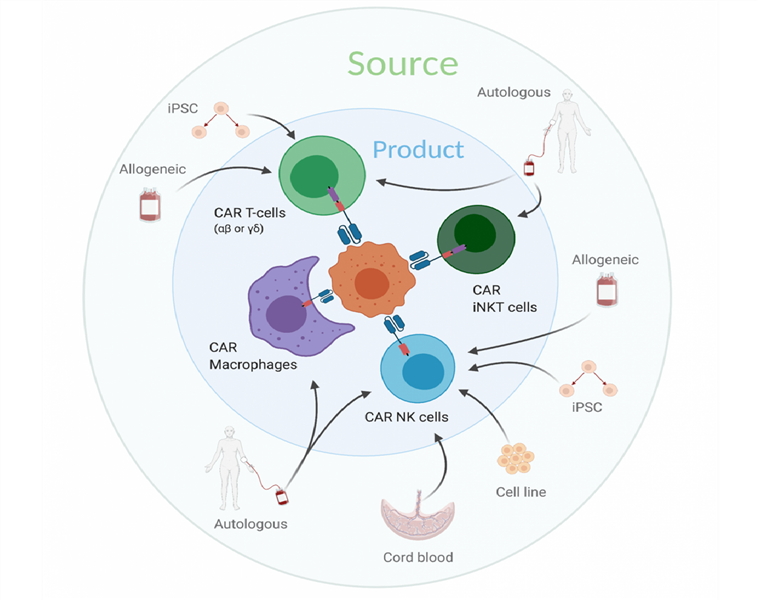
Trong thiết kế cấu trúc CAR, một số miền được cải biến khác với cấu trúc này ở CAR-T, giúp cho chúng phù hợp hơn trên tế bào NK và tăng cường các cơ chế hoạt hóa loại tế bào này. Việc chuyển gen CAR vào tế bào NK cũng đòi hỏi việc phát triển các hệ thống không sử dụng virus (do khả năng phá vỡ virus của chúng), ví dụ các polyme cation như dextran sulfat, hay các hạt nano lipid mRNA. Nguồn tế bào được sử dụng thường là PBMC tự thân, tuy nhiên gần đây các nỗ lực xây dựng CAR-NK đồng loại hướng đến PBMC từ người hiến, hoặc từ máu cuống rốn, từ tế bào gốc đa tiềm năng cảm ứng (Induced pluripotent stem cell – iPSC), hay từ dòng tế bào NK thương mại.
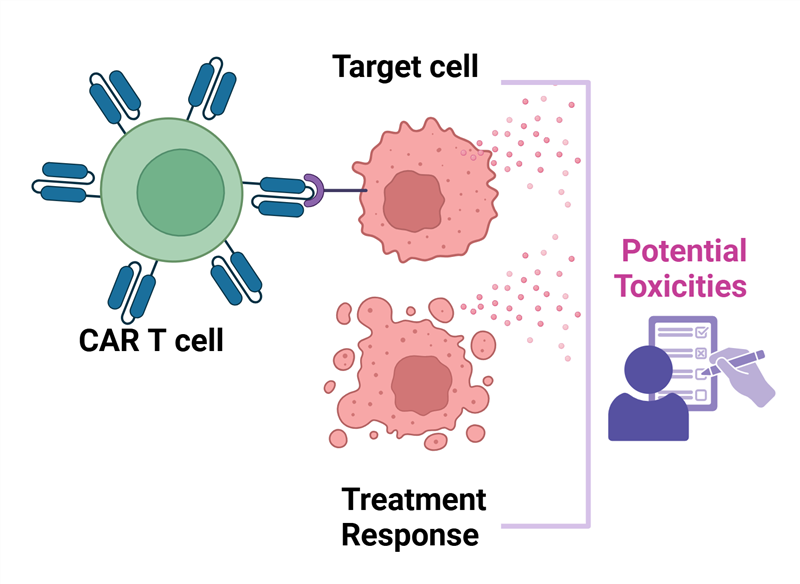
Tương tự CAR-T, các tế bào CAR-NK phát huy tác dụng kháng u thông qua độc tính tế bào phụ thuộc CAR sau khi nhận diện các kháng nguyên cụ thể của tế bào ung thư. Bên cạnh đó, CAR-NK có khả năng tạo ra độc tính tế bào không phụ thuộc vào CAR, cung cấp những cơ chế hoạt động bổ sung giúp khắc phục hiện tượng thoát kháng nguyên (khối u chọn lọc các quần thể tế bào ung thư không biểu hiện kháng nguyên mà cấu trúc CAR nhận diện để tránh được sự giám sát miễn dịch).
Liệu pháp CAR-NK thể hiện sự an toàn vượt trội so với CAR-T, do chúng sinh ra lượng cytokine gây viêm thấp hơn, nên ít gặp các phản ứng viêm nghiêm trọng, hội chứng giải phóng cytokine và độc tính thần kinh. NK biểu hiện các thụ thể ức chế như KIR và NKG2A liên kết với MHC-I tự thân và ức chế hoạt hóa tế bào NK, là nền tảng cho khả năng tự dung nạp của chúng và đóng vai trò quan trọng trong việc giảm độc tính trúng đích ở ngoài khối u, một mối lo ngại phổ biến khi các kháng nguyên liên quan đến khối u (tumor-associated antigen – TAA) cũng được biểu hiện trong các mô bình thường. Do đó, tế bào CAR-NK có thể phân biệt tế bào ác tính với tế bào khỏe mạnh hiệu quả hơn, giảm thiểu tổn thương cho các mô bình thường.
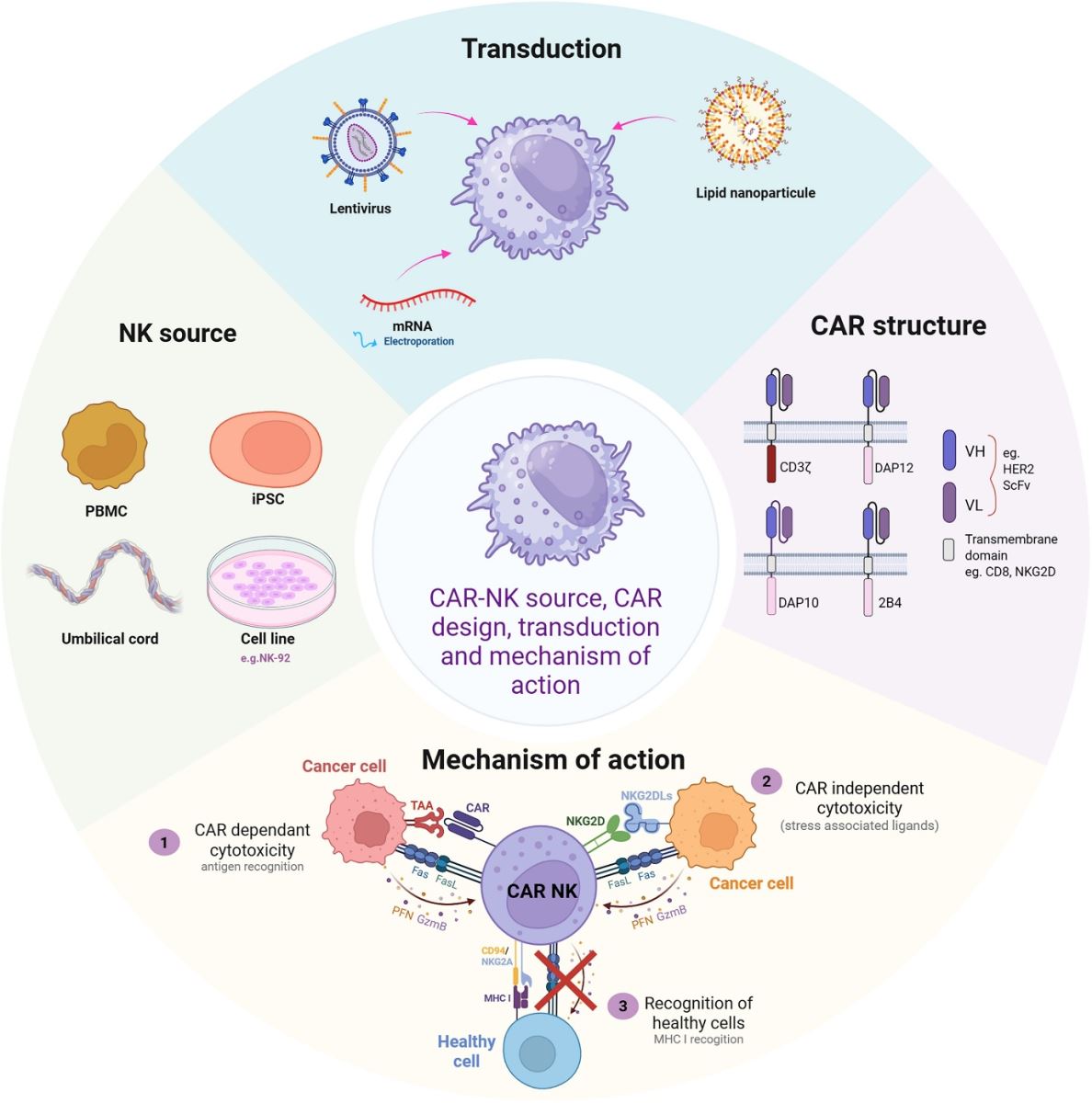
Nguồn: Jassaud M., et al. (2026). Innate immune cells in chimeric antigen receptor therapy. Molecular Therapy, 34 (1), 97-116.
3. Bức tranh lâm sàng về liệu pháp CAR-NK
Một bước quan trọng trong việc chuyển liệu pháp CAR-NK vào thực tiễn lâm sàng là phát triển các quy trình tuân thủ Thực hành Sản xuất Tốt (Good Manufacturing Practices – GMP). Tế bào CAR-NK có thể được sản xuất bằng các hệ thống khép kín tự động như thiết bị CliniMACS Prodigy, cho phép mở rộng và chuyển gen trong điều kiện GMP, đồng thời duy trì hoạt động chống khối u tương đương với sản xuất quy mô nhỏ. Một số quy trình khác cũng được xác nhận đạt tiêu chuẩn lâm sàng, sau khi trải qua các quá trình đánh giá nghiêm ngặt.
Trong ung thư huyết học, nhiều bệnh lý được thử nghiệm và ứng dụng liệu pháp CAR-T cũng đang được tiếp cận với CAR-NK, như u lympho tế bào B, bệnh bạch cầu dòng lympho mạn tính (CLL), bệnh bạch cầu dòng lympho cấp tính (ALL), bệnh bạch cầu tủy cấp tính (AML),… Nhiều thử nghiệm đã cho những kết quả đáng khích lệ, với hiệu quả tương tự CAR-T nhưng tính an toàn vượt trội, không có các tác dụng phụ nghiêm trọng như hội chứng giải phóng cytokine, độc tính thần kinh hoặc bệnh ghép chống chủ.
Trong các dạng ung thư u đặc, liệu pháp CAR-T gặp rất nhiều khó khăn do đặc điểm vi môi trường khối u, ngược lại CAR-NK có những ưu thế vượt trội giúp những tế bào này tiếp cận tế bào ung thư tốt hơn. Một số thử nghiệm lâm sàng đã được thực hiện cho ung thư tuyến tiền liệt, buồng trứng, u nguyên bào thần kinh đệm, ung thư biểu mô tuyến tụy,… Những tín hiệu lạc quan về hiệu quả của liệu pháp này đã được ghi nhận, bao gồm tác động trực tiếp của tế bào CAR-NK cũng như khả năng điều hòa miễn dịch của chúng.
Trong bệnh tự miễn, liệu pháp CAR-NK cũng được chú ý đến, sau những thành công bước đầu mà CAR-T đạt được trên các bệnh nhân lupus ban đỏ hệ thống. Những bệnh tự miễn đang được thử nghiệm lâm sàng với CAR-NK bao gồm lupus ban đỏ hệ thống, giảm tiểu cầu miễn dịch nguyên phát, bệnh thận liên quan đến miễn dịch và viêm thận do lupus, tất cả đều liên quan đến việc nhắm mục tiêu vào tế bào B thông qua CD19.
4. Những hạn chế của liệu pháp CAR-NK và phương hướng khắc phục
Liệu pháp CAR-NK cũng đối mặt với một số thách thức.
Vấn đề đầu tiên liên quan đến quy trình sản xuất. Các vector virus có khả năng chuyển gen tốt trên tế bào T nhưng hiệu suất khá thấp trên tế bào NK, và gặp những lo ngại về khả năng biến đổi di truyền tế bào đích. Các vector và phương pháp chuyển gen không dùng virus đang được phát triển, nhưng ảnh hưởng lớn đến sức sống của tế bào, và độ an toàn cần được nghiên cứu sâu hơn. Việc thu nhận và nuôi cấy tăng sinh tế bào NK cũng gặp khó khăn hơn tế bào T do chúng chiếm tỷ lệ thấp hơn nhiều.
Tiếp theo, các tế bào CAR-NK khi truyền vào cơ thể có thời gian tồn tại khá ngắn, làm giảm hiệu quả điều trị. Các chiến lược khắc phục đang được nghiên cứu, bao gồm thiết kế các gen thúc đẩy sự sống (ví dụ như chống apoptosis), các cơ chế giảm phản ứng miễn dịch của vật chủ chống tế bào lạ, cung cấp các cytokine để duy trì sự tăng sinh và hoạt động của tế bào NK,…
Bên cạnh đó, vi mô trường khối u (tumor microenvironment – TME) gây nên những rào cản để CAR-NK có thể tiếp cận các tế bào ung thư trong u đặc. Mặc dù có lợi thế hơn nhiều so với CAR-T, các tế bào CAR-NK vẫn cần được tăng cường khả năng thâm nhập mô và thích ứng với TME. Một số phương án khắc phục đang được thử nghiệm, bao gồm kết hợp CAR-NK với các chất ức chế điểm kiểm soát miễn dịch, sửa đổi gen để cải thiện khả năng thích ứng, những can thiệp trong quá trình điều trị để thay đổi TME như khắc phục tình trạng thiếu oxy và pH thấp,…
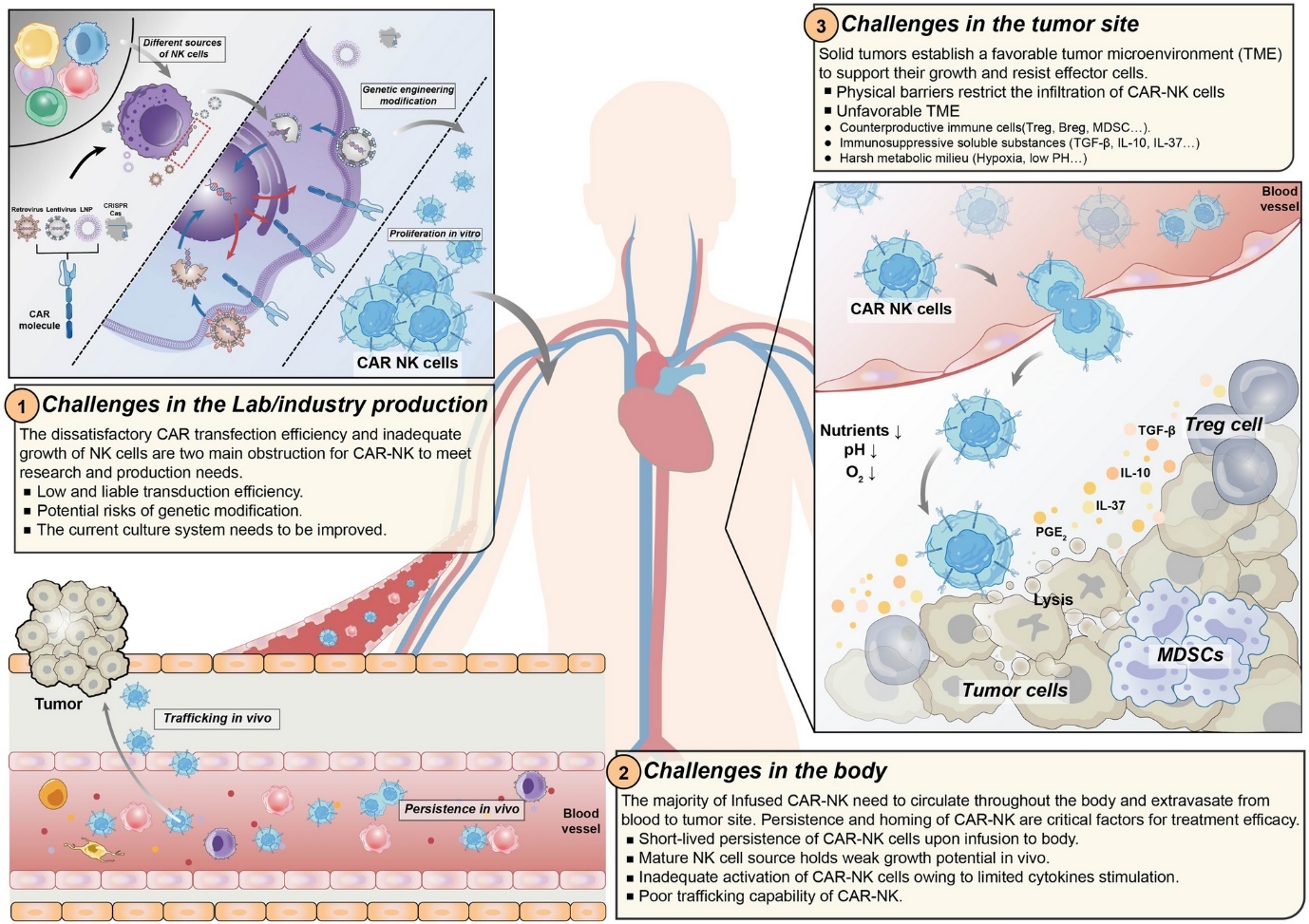
Nguồn: Zhang Y., et al. (2023). Chimeric antigen receptor engineered natural killer cells for cancer therapy. Experimental Hematology & Oncology, 12 (1), 70.
TÀI LIỆU THAM KHẢO
1. Jassaud M., et al. (2026). Innate immune cells in chimeric antigen receptor therapy. Molecular Therapy, 34 (1), 97-116. https://doi.org/10.1016/j.ymthe.2025.10.003
2. Jørgensen L. V., et al. (2025). The clinical landscape of CAR NK cells. Experimental Hematology & Oncology, 14 (1), 46. https://doi.org/10.1186/s40164-025-00633-8
3. Wang W., et al. (2024). Breakthrough of solid tumor treatment: CAR-NK immunotherapy. Cell Death Discovery, 10 (1), 40. https://doi.org/10.1038/s41420-024-01815-9
4. Yao P., et al. (2024). The development and application of chimeric antigen receptor natural killer (CAR-NK) cells for cancer therapy: current state, challenges and emerging therapeutic advances. Experimental Hematology & Oncology, 13 (1), 118. https://doi.org/10.1186/s40164-024-00583-7
5. Zhang Y., et al. (2023). Chimeric antigen receptor engineered natural killer cells for cancer therapy. Experimental Hematology & Oncology, 12 (1), 70. https://doi.org/10.1186/s40164-023-00431-0
6. Wang M., et al. (2022). Natural killer cell awakening: Unleash cancer-immunity cycle against glioblastoma. Cell Death & Disease, 13 (7), 588. https://doi.org/10.1038/s41419-022-05041-y
XEM THÊM
- Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh: Phần 1 - Các tế bào miễn dịch bẩm sinh và lợi thế trong điều trị ung thư u đặc https://ysinhtebao.com/lieu-phap-tb-mien-dich/car-innate-immune-cells-p1-introduction
- Liệu pháp miễn dịch trong điều trị ung thư https://ysinhtebao.com/ung-thu/lieu-phap-mien-dich-trong-dieu-tri-ung-thu
- Liệu pháp CAR-T, TCR-T https://ysinhtebao.com/lieu-phap-cart-tcrt