Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh (P3)
1. Đại thực bào
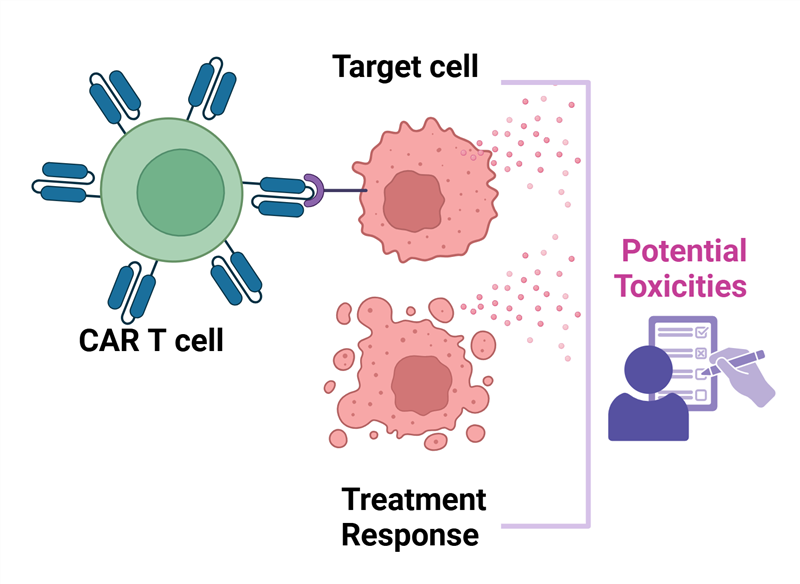
Đại thực bào là những tế bào miễn dịch bẩm sinh rất linh hoạt, đóng vai trò quan trọng trong cả đáp ứng miễn dịch bẩm sinh và thích ứng. Đa số đại thực bào tập trung ở các vị trí thường xảy ra sự xâm nhập của các tác nhân môi trường, như da (tế bào Langerhans), phổi (đại thực bào phế nang, hay tế bào bụi – dust cell), hệ thần kinh (vi bào đệm – microglia), gan (tế bào Kupffer), xương (hủy cốt bào – osteoclast),…
Vai trò chính của chúng là thực bào (nuốt và tiêu hóa các tác nhân gây bệnh như vi khuẩn, mảnh vụn tế bào, các tế bào bất thường), ngoài ra có thể trình diện kháng nguyên (đại thực bào là một trong những tế bào trình diện kháng nguyên chuyên nghiệp), và tiết ra nhiều loại cytokine khác nhau đề điều hòa đáp ứng miễn dịch.
Có một số dạng hoạt hóa của đại thực bào, với 2 nhóm chính là M1 và M2. Đại thực bào M1 có chức năng gây viêm, diệt khuẩn và thực bào. Ngược lại, đại thực bào M2 kháng viêm, tham gia chữa lành vết thương và sửa chữa mô, chúng cần thiết cho quá trình tái tạo mạch máu và tái tạo biểu mô.
Trong ung thư, đại thực bào liên quan đến khối u (Tumor-associated macrophage – TAM) cũng gồm các phân nhóm khác nhau và thể hiện chức năng kép. TAM dạng M1 thể hiện đặc tính kháng u, tiêu diệt tế bào ung thư thông qua thực bào và độc tính tế bào. Phân nhóm M2 (chiếm tỷ lệ lớn hơn trong vi môi trường khối u) thúc đẩy sự hình thành mạch máu khối u, tăng trưởng, di căn và ức chế điều hòa ức chế các tế bào miễn dịch kháng u. Các đại thực bào có thể xâm nhập vào một số khối u, sự tăng số lượng của chúng liên quan với tiên lượng xấu trong một số dạng ung thư. Những chiến lược điều trị ung thư tác động đến TAM đang hướng đến việc thay đổi kiểu hình của chúng từ dạng M1 sang M2, có thể gồm thay đổi con đường truyền tin tế bào, sử dụng các chất cảm ứng, hay ức chế hoạt tính của dạng M2,…
.png)
TAM dạng M2 (hình trên) có thể thúc đẩy sự tiến triển của ung thư. Các chiến lược để thúc đẩy chúng chuyển sang dạng M1 bao gồm tái lập trình dựa trên sự phân cực (tác động đến tín hiệu CSF1/CSF1-R là con đường truyền tin liên quan đến hoạt hóa TAM thành dạng M2, hoặc PI3K là con đường M2 thúc đẩy sự xâm lấn của khối u) hoặc dựa trên chức năng (như nhắm mục tiêu vào các phân tử tránh thực bào, hoặc các phân tử ức chế miễn dịch). Khi tái lập trình sang dạng M1 (hình dưới), TAM có khả năng tiêu diệt tế bào ung thư thông qua cơ chế thực bào, gây độc tế bào hoặc hoạt hóa các loại tế bào miễn dịch khác.
Nguồn: Lu J., et al. (2024). CAR Macrophages: a promising novel immunotherapy for solid tumors and beyond. Biomarker research, 12(1), 86. https://doi.org/10.1186/s40364-024-00637-2
Do khả năng thâm nhập khối u, và mang những đặc điểm lợi thế chung của các tế bào miễn dịch bẩm sinh so với tế bào T, CAR-M một phương pháp mới và đầy hứa hẹn thay thế CAR-T trong liệu pháp miễn dịch ung thư, đặc biệt là các loại u đặc.
Trong thiết kế cấu trúc CAR, vùng nội bào cần được điều chỉnh phù hợp với đại thực bào, cùng với việc kết hợp các tín hiệu tăng cường thực bào và tiết cytokine gây viêm, thúc đẩy các loại tế bào miễn dịch kháng u khác, chống lại sự chuyển hóa M2 và ức chế miễn dịch trong vi môi trường khối u. Những cải tiến này phản ánh sự phức tạp nhưng cũng cho thấy tiềm năng của liệu pháp CAR-M, không chỉ trực tiếp tiêu diệt tế bào ung thư mà còn kích hoạt miễn dịch rộng hơn và điều chỉnh vi môi trường khối u.
Việc chuyển gen mã hóa cấu trúc CAR vào đại thực bào cũng gặp những khó khăn tương tự như với tế bào NK, do chúng đều có hoạt tính tiêu diệt virus nên khó có thể áp dụng phương pháp chuyển gen bằng vector virus. Các phương án khắc phục bao gồm ức chế chất thể hiện đặc tính kháng virus, sử dụng adenovirus là vector biểu hiện ở tế bào chất, phát triển các phương pháp không dùng virus như các hạt nano lipid (Lipid nanoparticle – LNP), xung điện,…
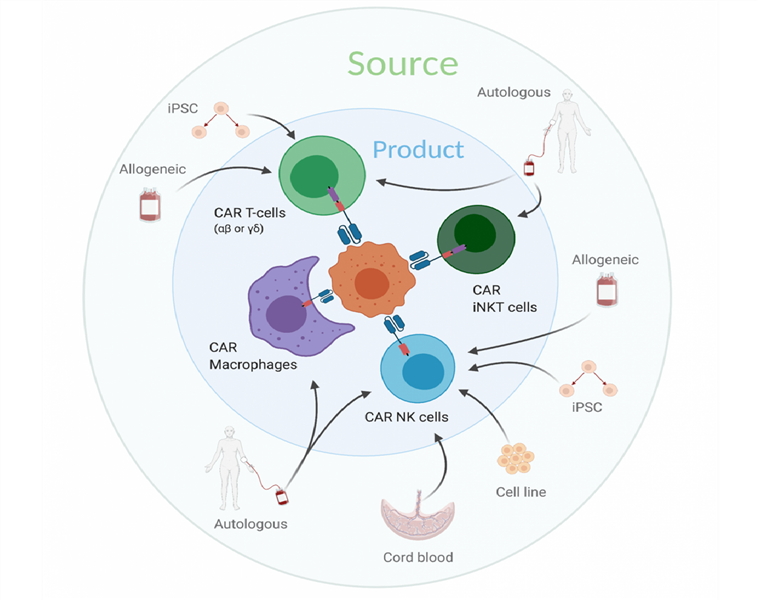
Nguồn đại thực bào có thể huy động theo nhiều cách khác nhau, bao gồm đại thực bào biệt hóa từ tế bào đơn nhân thu từ máu ngoại vi, các dòng tế bào bất tử giống đại thực bào (dòng tế bào đơn nhân THP-1), biệt hóa từ tế bào gốc đa tiềm năng như tế bào gốc phôi (ESC) hay tế bào gốc đa tiềm năng cảm ứng (iPSC),… Một chiến lược đầy hứa hẹn khác là biểu hiện CAR trên tế bào đơn nhân (là dạng tiền thân trước biệt hóa của đại thực bào), chúng có thể tồn tại lâu dài và biệt hóa thành CAR-M gây viêm với hoạt tính kháng u mạnh.
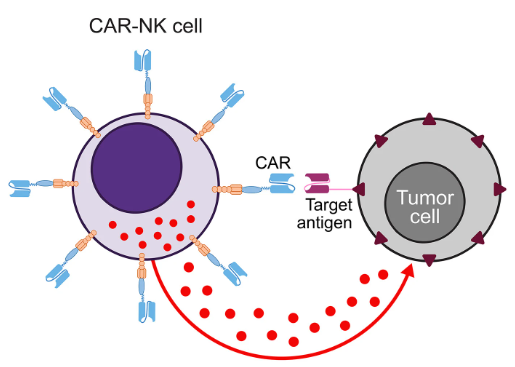
Các tế bào CAR-M có nhiều cơ chế chống ung thư khác nhau. CAR-M có thể thực bào tế bào ác tính khi nhận diện kháng nguyên đặc hiệu khối u, hoặc tiết các cytokine gây viêm. Ngoài ra, CAR-M còn tái cấu trúc vi môi trường khối u, làm thoái hóa chất nền ngoại bào để phá các rào cản vật lý bảo vệ khối u, tạo điều kiện cho các tế bào khác xâm nhập, trình diện kháng nguyên cho tế bào T, thu hút và kích hoạt tế bào T cùng nhiều loại tế bào miễn dịch khác,…
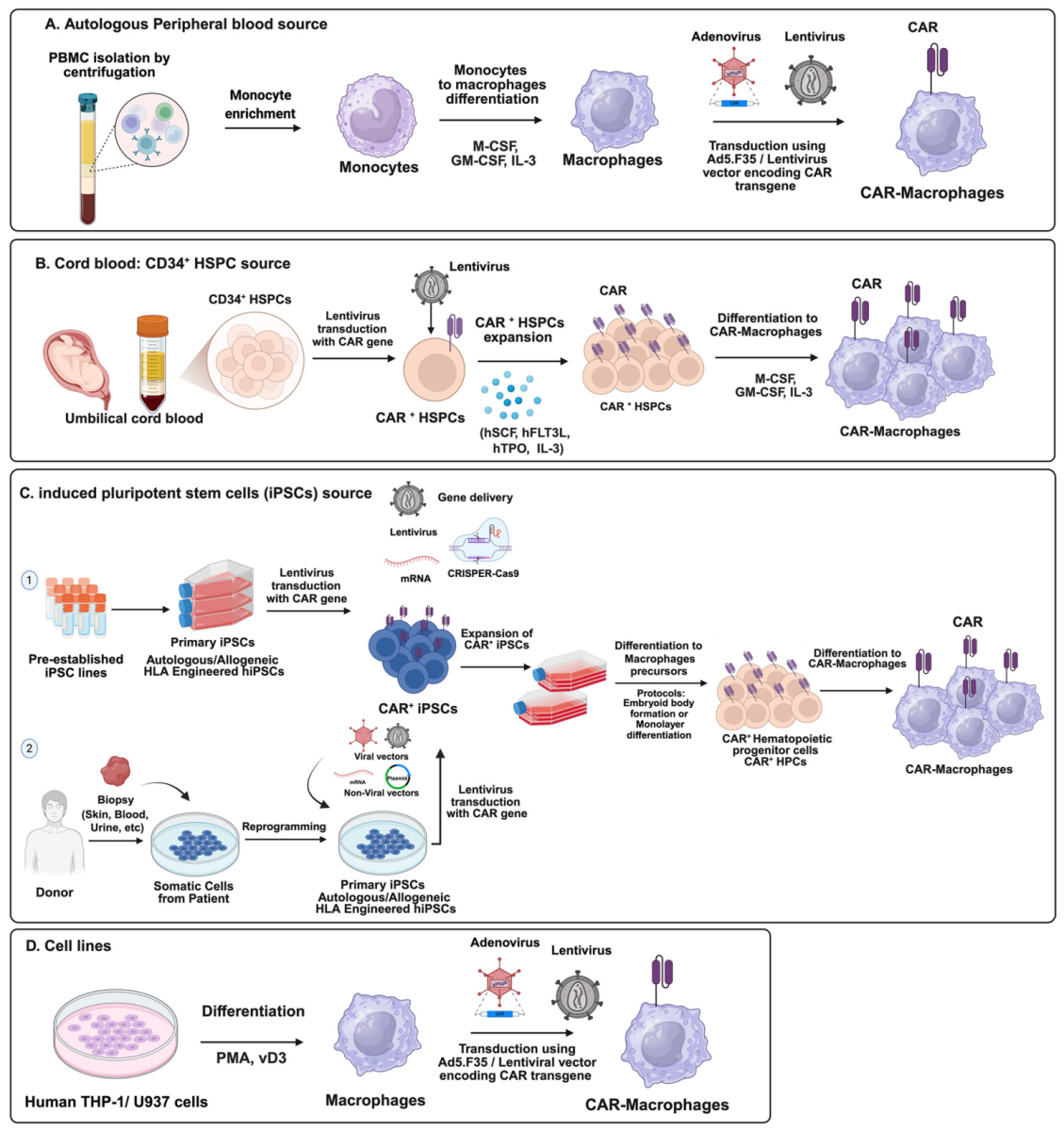
A. Tế bào đơn nhân được thu thập từ máu ngoại vi tự thân, biệt hóa thành đại thực bào, sau đó chuyển gen mã hóa cấu trúc CAR bằng lentivirus hoặc adenovirus. B. Tế bào gốc/tiền thân tạo máu (HSPC) từ máu dây rốn được chuyển gen CAR bằng lentivirus, tạo nên CAR-HSPC, sau đó biệt hóa thành CAR-M. C. Tế bào gốc đa tiềm năng cảm ứng (iPSC), có thể là dòng tế bào có sẵn hoặc được cảm ứng từ tế bào soma của người hiến, được chuyển gen CAR với nhiều cách thức khác nhau tạo nên CAR-iPSC, sau đó biệt hóa thành tế bào tiền thân tạo máu CAR-HPC, cuối cùng biệt hóa thành CAR-M. D. Các dòng tế bào thương mại từ tủy xương người được biệt hóa thành tế bào giống đại thực bào, sau đó chuyển gen CAR bằng lentivirus/adenovirus để tạo thành CAR-M.
Nguồn: 2. Alrehaili M., et al. (2025). CAR-macrophages in solid tumors: promise, progress, and prospects. npj Precision Oncology, 9(1), 382. https://doi.org/10.1038/s41698-025-01170-7
3. Bức tranh lâm sàng về liệu pháp CAR-M
Các thử nghiệm điều trị ung thư dạng u đặc là những nghiên cứu lâm sàng đầu tiên sử dụng CAR-M. Thử nghiệm lâm sàng giai đoạn I mã số NCT04660929 (khởi động năm 2021) của Carisma Therapeutics đã đánh giá CAR-M kháng HER2 ở bệnh nhân ung thư có biểu hiện thụ thể này. Kết quả cho thấy tính an toàn có thể kiểm soát, không có tác dụng phụ nghiệm trọng liên quan đến hội chứng giải phóng cytokine hoặc độc tính thần kinh. Các tế bào CAR-M xâm nhập thành công vào khối u, kéo theo sự gia tăng xâm nhập của tế bào T, hỗ trợ cho việc điều chỉnh vi môi trường khối u. Sau thử nghiệm này, một số nghiên cứu lâm sàng giai đoạn I/II tiếp tục được thực hiện trên ung thư dạ dày, buồng trứng, u trung mô phúc mạc, hiện đang thu thập dữ liệu về tính an toàn, khả năng dung nạp và hiệu quả điều trị.
Ngoài ung thư, CAR-M có tiềm năng ứng dụng trong một số bệnh lý nhiễm khuẩn – nhiễm virus, xơ hóa, xơ vữa động mạch. Các thử nghiệm tiền lâm sàng trên mô hình động vật đang được thực hiện với những kết quả đầy hy vọng. Những bệnh lý ngoài ung thư đang được thử nghiệm với CAR-M bao gồm nhiễm khuẩn huyết, nhiễm trùng quanh khớp nhân tạo (biến chứng nghiêm trọng sau thay khớp như khớp háng, khớp gối), xơ gan, Alzheimer, bệnh cơ tim, xơ vữa động mạch, COVID-19,…
.png)
Tế bào đơn nhân tự thân là một nguồn tế bào khả thi, sau đó được chuyển gen in vitro để tạo nên tế bào CAR-M (hình trên, bên trái). Một cách tiếp cận khác là sử dụng các yếu tố chuyển gen chính xác vào đại thực bào trong cơ thể tạo nên CAR-M in vivo (hình dưới, bên trái). Các tế bào CAR-M trong cơ thể có thể di chuyển theo mạch máu (1) đến vị trí mô tổn thương/khối u, thâm nhiễm mô/khối u (2) và hoạt động chức năng (3).
Nguồn: Nguồn: Chen Y., et al. (2025). Exploring CAR-macrophages in non-tumor diseases: therapeutic potential beyond cancer. Journal of advanced research, 77, 481-496. https://doi.org/10.1016/j.jare.2025.01.004
4. Hạn chế của liệu pháp CAR-M để c thể ứng dụng lâm sàng
Giống như liệu pháp CAR-NK, CAR-M cũng đối mặt với một số hạn chế. Việc chuyển gen vào đại thực bào còn gặp khó khăn, mặc dù các vector adenovirus hay các hệ thống mới không dùng virus đã cải thiện hiệu quả phần nào. Đại thực bào đã biệt hóa hoàn toàn nên không tăng sinh và thời gian tồn tại hạn chế, do đó làm giảm hiệu quả điều trị. Vi môi trường khối u có tính ức chế miễn dịch có thể tái lập trình lại chúng theo hướng kiểu hình giống M2, làm giảm hoạt động kháng u. Không giống như tế bào CAR-T hoặc CAR-NK, CAR-M thiếu khả năng gây độc tế bào trực tiếp mà thay vào đó dựa vào thực bào và huy động miễn dịch, điều này có thể không đủ đối với các khối u có khả năng sinh miễn dịch kém. Việc sản xuất đạt tiêu chuẩn lâm sàng cũng vẫn còn phức tạp, và tương đối ít liệu pháp CAR-M đã tiến đến giai đoạn thử nghiệm lâm sàng.
.png)
CAR-M có những chức năng loại bỏ những yếu tố bất thường trong cơ thể thông qua tấn công có định hướng một cách kiểm soát, phân cực thành M1/M2 để can thiệp vào vi môi trường của mô bệnh, điều hòa miễn dịch. Tuy nhiên liệu pháp CAR-M gặp một số thách thức, như tế bào biệt hóa cuối dòng và khó chuyển gen nên khó khăn trong việc sản xuất và duy trì thời gian tồn tại trong cơ thể, hiện tượng thoát kháng nguyên ảnh hưởng đến hiệu quả, cấu trúc CAR có thể kích hoạt phản ứng miễn dịch đối với CAR-M, và chưa có nhiều dữ liệu lâm sàng về tính an toàn.
Nguồn: Chen Y., et al. (2025). Exploring CAR-macrophages in non-tumor diseases: therapeutic potential beyond cancer. Journal of advanced research, 77, 481-496. https://doi.org/10.1016/j.jare.2025.01.004
TÀI LIỆU THAM KHẢO
1. Jassaud M., et al. (2026). Innate immune cells in chimeric antigen receptor therapy. Molecular Therapy, 34 (1), 97-116. https://doi.org/10.1016/j.ymthe.2025.10.003
2. Alrehaili M., et al. (2025). CAR-macrophages in solid tumors: promise, progress, and prospects. npj Precision Oncology, 9(1), 382. https://doi.org/10.1038/s41698-025-01170-7
3. Chen Y., et al. (2025). Exploring CAR-macrophages in non-tumor diseases: therapeutic potential beyond cancer. Journal of advanced research, 77, 481-496. https://doi.org/10.1016/j.jare.2025.01.004
4. Lu J., et al. (2024). CAR Macrophages: a promising novel immunotherapy for solid tumors and beyond. Biomarker research, 12(1), 86. https://doi.org/10.1186/s40364-024-00637-2
5. Look T., et al. (2025). CAR T cells, CAR NK cells, and CAR macrophages exhibit distinct traits in glioma models but are similarly enhanced when combined with cytokines. Cell Reports Medicine, 6(2), 101931. https://doi.org/10.1016/j.xcrm.2025.101931
XEM THÊM
- Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh: Phần 1 - Các tế bào miễn dịch bẩm sinh và lợi thế trong điều trị ung thư u đặc https://ysinhtebao.com/lieu-phap-tb-mien-dich/car-innate-immune-cells-p1-introduction
- Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh: Phần 2. Liệu pháp CAR-NK – hiện trạng, thách thức và triển vọng tương lai https://ysinhtebao.com/lieu-phap-tb-mien-dich/car-innate-immune-cells-p2-car-nk
- Liệu pháp miễn dịch trong điều trị ung thư https://ysinhtebao.com/ung-thu/lieu-phap-mien-dich-trong-dieu-tri-ung-thu
- Liệu pháp CAR-T, TCR-T https://ysinhtebao.com/lieu-phap-cart-tcrt
- Vai trò của tương tác giữa đại thực bào liên quan đến khối u và nguyên bào sợi liên quan đến ung thư trong môi trường vi mô của sarcoma mô mềm https://ysinhtebao.com/tb-md/tuong-tac-tam-va-caf-trong-tme-sarcoma