Liệu pháp CAR-NKT mang lại hiệu quả vượt trội khi điều trị ung thư nội mạc tử cung trong nghiên cứu tiền lâm sàng
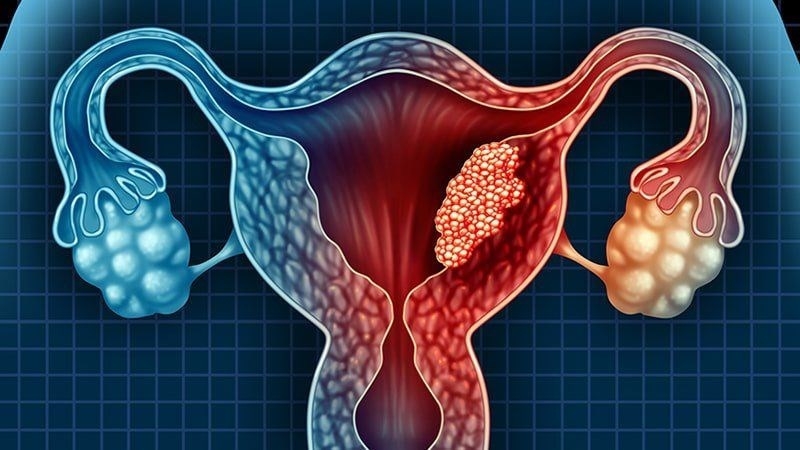
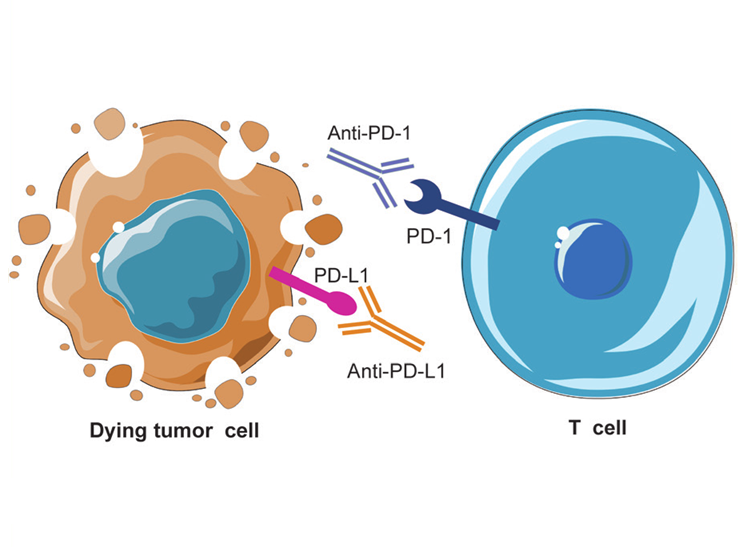
Ung thư nội mạc tử cung là bệnh ung thư phụ khoa ảnh hưởng chủ yếu đến phụ nữ sau mãn kinh. Bệnh có thể xảy ra ở bất kỳ độ tuổi nào, nhưng hầu hết được chẩn đoán ở phụ nữ 55-64 tuổi, với tuổi trung vị khi chẩn đoán là 63 tuổi. Bệnh thường gặp hơn ở những người thừa cân, béo phì, mắc tiểu đường, hay dùng các sản phẩm có chứa hormone estrogen. Các phương pháp điều trị chính bao gồm phẫu thuật cắt bỏ tử cung toàn phần, cắt hai buồng trứng và vòi trứng; hóa – xạ trị sau phẫu thuật để diệt tế bào ung thư còn sót hoặc khi ung thư di căn; liệu pháp nội tiết với hormone đối kháng để ức chế khối u; các thuốc điều trị đích như Lenvatinib (Lenvima) hay Bevacizumab (Avastin) ức chế hình thành mạch máu; liệu pháp miễn dịch với các thuốc ức chế điểm kiểm soát PD-1/PD-L1 như Pembrolizumab (Keytruda) và Dostarlimab (Jemperli), giúp hệ miễn dịch phát hiện và tiêu diệt tế bào ung thư.
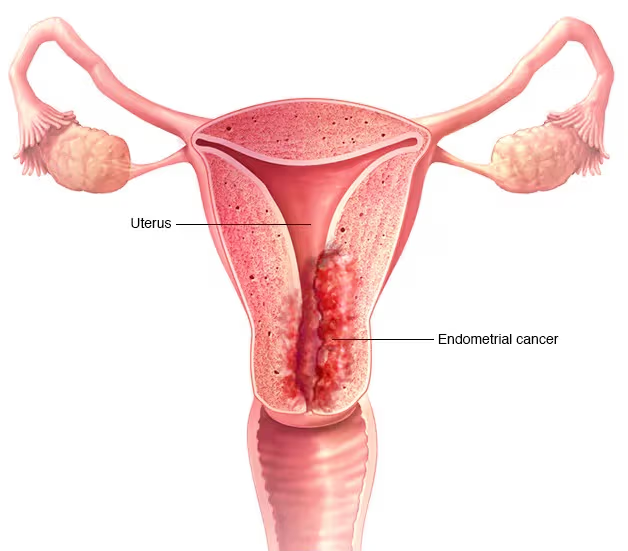
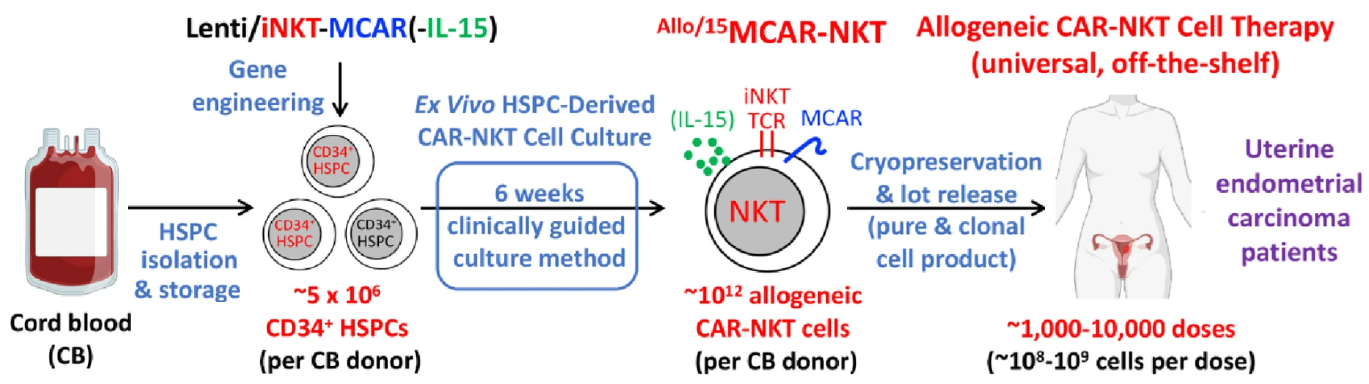
Trong một nghiên cứu mới công bố trên tạp chí Experimental Hematology & Oncology, các nhà khoa học tại Đại học California (Los Angeles, Hoa Kỳ) đã phát triển một liệu pháp tế bào miễn dịch có khả năng điều trị hiệu quả ung thư nội mạc tử cung. Nhóm nghiên cứu đã chuyển gen mã hóa thụ thể kháng nguyên khảm (Chimeric Antigen Receptor – CAR) hướng đích mesothelin (một loại protein được tìm thấy trên các tế bào ung thư nội mạc tử cung) vào tế bào gốc máu cuống rốn, sau đó biệt hóa các tế bào này thành tế bào T giết tự nhiên bất biến (invariant Natural Killer T cell – NKT). Những tế bào CAR-NKT này có thể phát hiện và tiêu diệt tế bào ác tính một cách chính xác, đồng thời có thể điều chỉnh vi môi trường khối u, giúp tăng hiệu quả điều trị. Nhóm nghiên cứu cũng đã tạo nên các tế bào CAR-T và CAR-NK để so sánh, kết quả cho thấy CAR-NKT thể hiện ưu thế vượt trội. Trên mô hình chuột mắc ung thư nội mạc tử cung, CAR-NKT đã loại bỏ hoàn toàn khối u và kéo dài thời gian sống, trong khi CAR-T chỉ kiểm soát được khối u một phần và tạm thời, trước khi khối u tái phát. Việc thử nghiệm rộng rãi hơn trên mẫu khối u của bệnh nhân và các dòng tế bào ung thư đã khẳng định khả năng kháng u vượt trội của liệu pháp này, ngay cả đối với các phân nhóm ung thư nội mạc tử cung có độ ác tính cao.
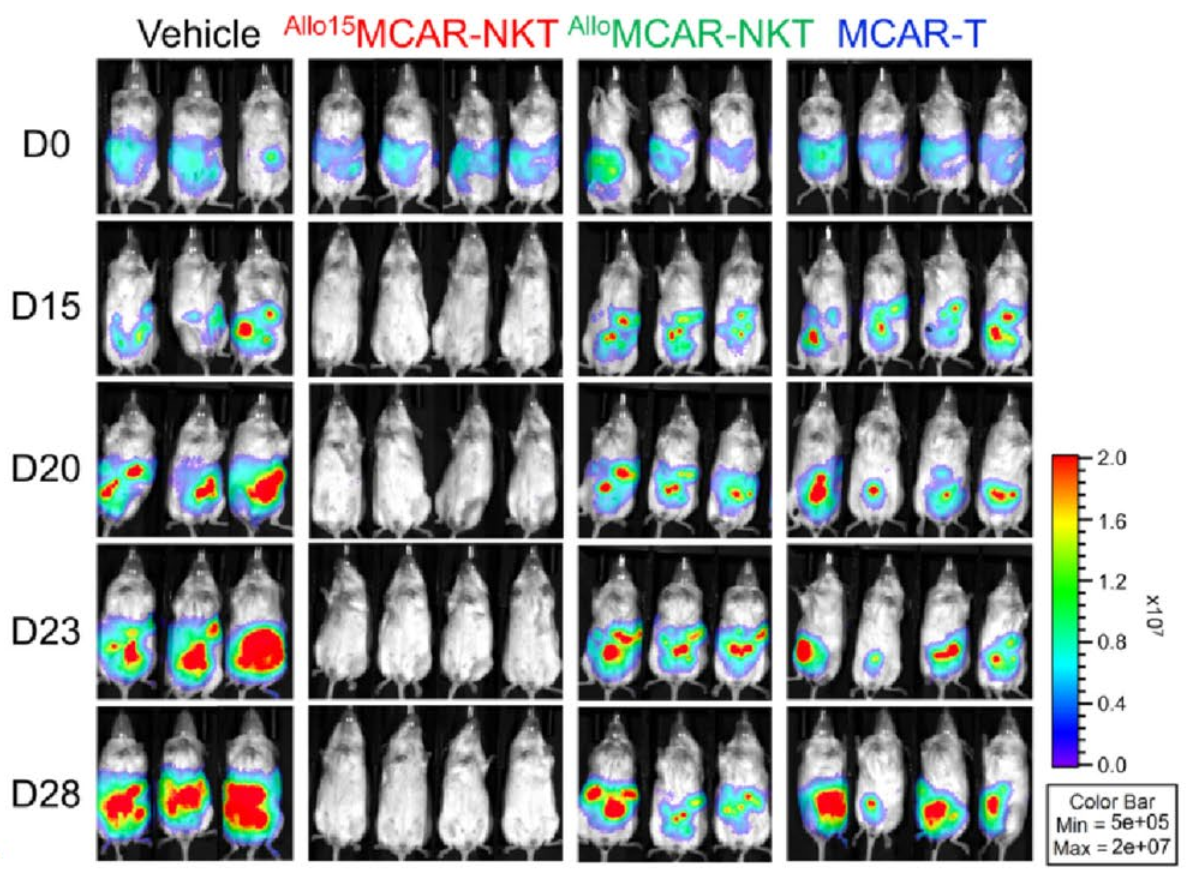
Hình ảnh phát quang sinh học cho thấy sự hiện diện của tế bào khối u ở chuột thí nghiệm theo thời gian, chứng minh hiệu quả kháng u trên mô hình chuột NSG (NOD scid gamma mouse) cấy ghép khối u biểu mô nội mạc tử cung người HEC1B-MSLN-FG. Ba loại tế bào điều trị được sử dụng: AlloMCAR-NKT (CAR-NKT đồng loại hướng đích mesothelin), Allo15MCAR-NKT (CAR-NKT đồng loại hướng đích mesothelin, có IL-15 kích hoạt) và tế bào MCAR-T thông thường (CAR-T hướng đích mesothelin). Liều tiêm phúc mạc là 3 × 106 tế bào.
Đồng thời, liệu pháp CAR-NKT chứng minh được sự an toàn khi sử dụng. Chúng không gây ra bệnh ghép chống chủ (Graft Versus Host Disease – GvHD), một tình trạng nguy hiểm trong đó các tế bào của người hiến tấn công các mô khỏe mạnh, khá phổ biến khi sử dụng CAR-T. Chúng cũng có nguy cơ gặp hội chứng giải phóng cytokine (cytokine release syndrome – CRS) thấp hơn so với liệu pháp CAR-T thông thường. Ngoài ra, CAR-NKT tương thích tự nhiên với bệnh nhân, nên có thể được sản xuất hàng loạt với nguồn nguyên liệu là máu cuống rốn, sau đó nuôi cấy tăng sinh lên số lượng lớn và bảo quản lạnh, sẵn sàng sử dụng cho nhiều người ngay khi có nhu cầu. Quy trình sản xuất này giúp việc điều trị có thể dễ tiếp cận hơn và chi phí thấp hơn khá nhiều, so với liệu pháp CAR-T tự thân hiện tại.
Những kết quả trên cũng mở ra tiềm năng điều trị ung thư vú, buồng trứng, phổi và tuyến tụy – những loại ung thư đều có sự biểu hiện mesothelin ở tế bào ác tính. Nhờ đó, một sản phẩm CAR-NKT hướng đích mesothelin có thể sử dụng cho nhiều bệnh nhân mắc các loại ung thư khác nhau. Nhóm nghiên cứu đang thúc đẩy phát triển một nền tảng CAR-NKT đồng loại tuân thủ GMP, đồng thời hướng đến các thử nghiệm lâm sàng đối với sản phẩm này.
TÀI LIỆU THAM KHẢO
Li Y. R., et al. (2026). Stem cell engineering for the generation of allogeneic CAR-directed natural killer T cells targeting endometrial carcinoma. Experimental Hematology & Oncology, 15(1), 14. https://doi.org/10.1186/s40164-026-00746-8