Triển vọng mới trong điều trị bệnh bạch cầu bằng cách hướng đến tế bào gốc của nó
Khó khăn lớn nhất khi điều trị AML là sự tồn tại của những “tế bào gốc ung thư bạch cầu”, chúng thường ở dạng không hoạt động và kháng hóa trị. Sau mỗi đợt điều trị có vẻ thành công, những tế bào này “tỉnh dậy” và kích hoạt trở lại để tăng sản tế bào, tạo nên đợt tiến triển mới của bệnh. Do vậy, việc phát triển các liệu pháp nhắm vào những tế bào gốc ung thư này là một thách thức nghiên cứu.
Theo một nghiên cứu đăng trên tạp chí Science Translational Medicine mới phát hành ngày 31/07/2024, một nhóm các nhà khoa học đã cung cấp những hiểu biết mới về đặc điểm di truyền và trao đổi chất của những tế bào này, từ đó mở ra hướng đi mới trong điều trị AML.
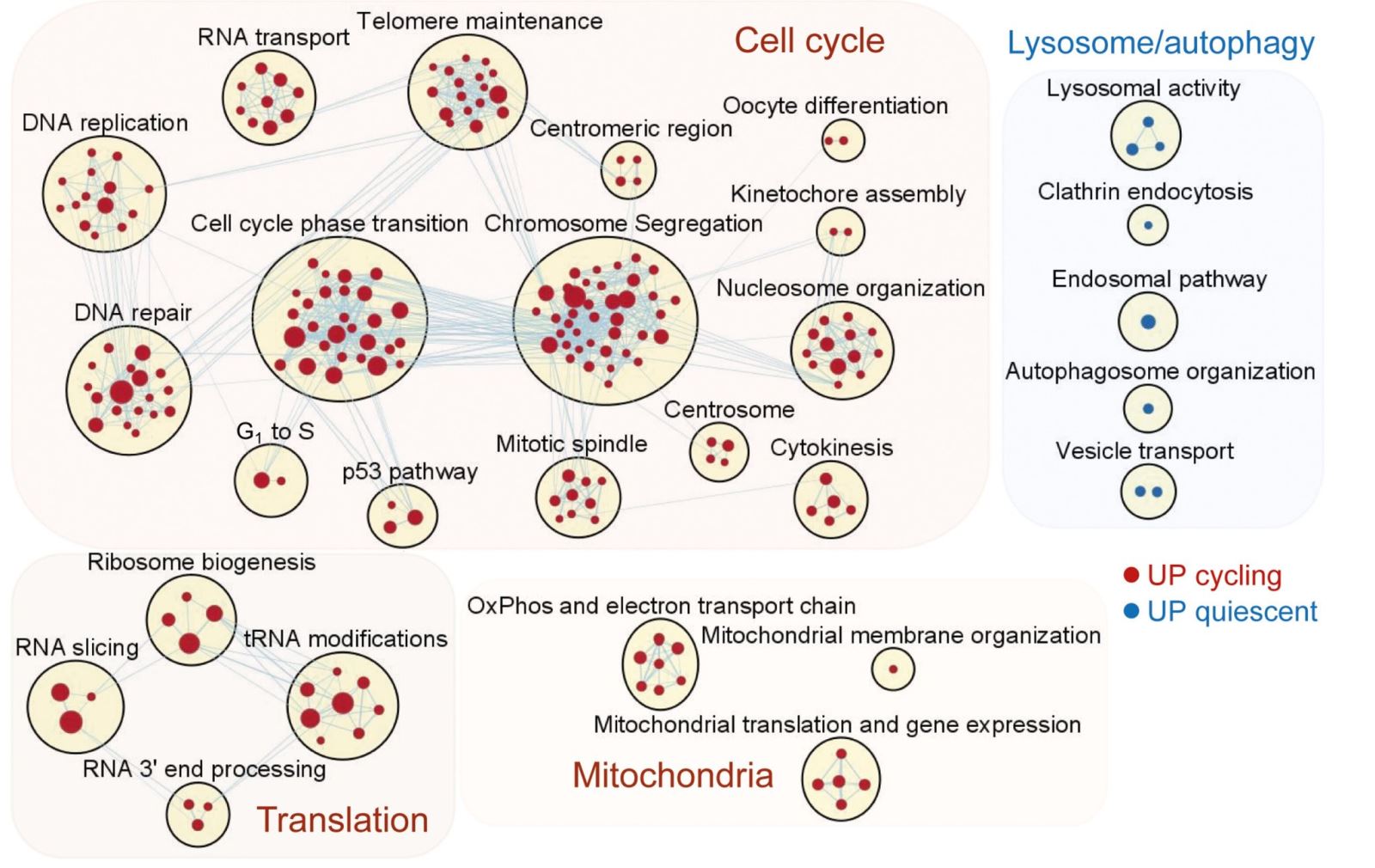
Những tế bào gốc ung thư trong AML chứa một dấu hiệu di truyền đặc trưng bao gồm 35 gen, có mối liên hệ chặt chẽ với tiên lượng bệnh. Đồng thời, cơ chế trao đổi chất của những tế bào bạch cầu không hoạt động cũng được chỉ rõ, liên quan đến cơ chế “tự thực bào” – “autophagy” (quá trình mà các tế bào tái chế những thành phần của nó để tạo ra những thành phần mới và cung cấp năng lượng trong trường hợp thiếu chất dinh dưỡng bên ngoài). Những tế bào này tồn tại phụ thuộc vào “ferritinophagy” – dạng tự thực nhắm vào ferritin (phân tử lưu trữ sắt chính trong cơ thể) – được trung gian bởi protein NCOA4. Bằng cách ức chế NCOA4, những tế bào ung thư bạch cầu (đặc biệt là các tế bào gốc không hoạt động) có khả năng chết cao hơn, trong khi các tế bào gốc máu khỏe mạnh vẫn được bảo tồn.
Do đó, thuốc nhắm mục tiêu ferritinophagy có thể là một chiến lược điều trị đầy hứa hẹn cho AML. Hợp chất được sử dụng để ngăn chặn NCOA4 đang ở giai đoạn phát triển ban đầu cho các thử nghiệm lâm sàng trong tương lai.
TÀI LIỆU THAM KHẢO
Larrue C., et al. (2024).Targeting ferritinophagy impairs quiescent cancer stem cells in acute myeloid leukemia in vitro and in vivo models. Science Translational Medicine 16 (757). DOI: 10.1126/scitranslmed.adk1731