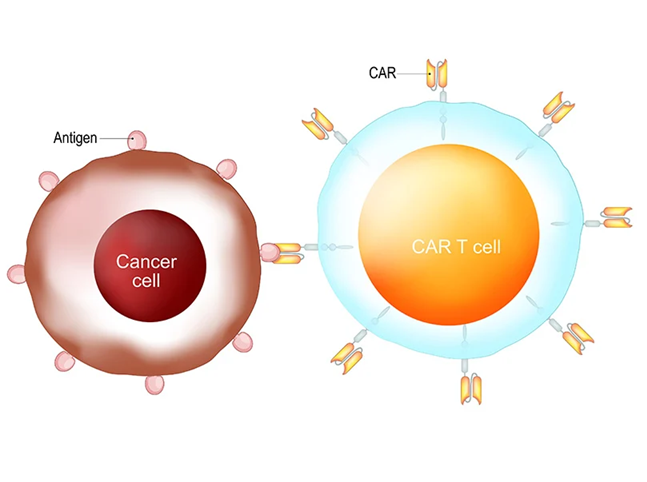
FDA trì hoãn việc phê duyệt liệu pháp tế bào và gen do các vấn đề về quy trình sản xuất và kiểm soát sản phẩm
FDA đã công bố hơn 200 Thư Phản hồi Đầy đủ (Complete Response Letter – CRL) cho các công ty sản xuất, trong đó 74% CRL trong giai đoạn 2020–2024 nêu rõ để khắc phục các vấn đề về hóa chất, sản xuất và kiểm soát (chemical, manufacturing and control – CMC). Ví dụ, liệu pháp gen của Ultragenyx cho hội chứng Sanflilippo loại A được yêu cầu bổ sung thông tin và cải tiến liên quan đến sản xuất sau quá trình kiểm tra cơ sở sản xuất. Liệu pháp tế bào của Capricor để điều trị bệnh cơ tim liên quan đến loạn dưỡng cơ Duchenne cũng bị từ chối, do cần bổ sung dữ liệu lâm sàng và các mục chưa được giải quyết trong phần CMC của đơn đăng ký.
Hiện tại, quá trình sản xuất liệu pháp tế bào và gen đang gặp nhiều thách thức để có thể được phê duyệt. Những liệu pháp này thường sử dụng các lộ trình lâm sàng tăng tốc để đẩy nhanh quá trình xin cấp phép, áp dụng quy định của FDA cho phép sản phẩm điều trị bệnh nghiêm trọng và đe dọa tính mạng được phê duyệt dựa trên một tiêu chí thay thế hoặc tiêu chí trung gian, dựa trên dự đoán lợi ích lâm sàng. Sự rút ngắn thời gian này dẫn đến những rủi ro lớn về CMC. Ngoài ra, trong những pha sớm của thử nghiệm sản phẩm, các lựa chọn ban đầu (như nguồn tế bào hay lựa chọn vector) có thể dẫn đến những hậu quả sâu rộng, ảnh hưởng đến hiệu suất sản phẩm, khả năng sản xuất và mở rộng quy mô.
Các nhà phát triển cần triển khai một chiến lược CMC mạnh mẽ ngay từ đầu, cân nhắc đến những yêu cầu cho giai đoạn sau của quá trình chuyển giao sản xuất và thương mại. Việc lựa chọn đối tác sản xuất và các chuyên gia CMC có năng lực đóng vai trò quan trọng trong việc định hướng này. Những yêu cầu pháp lý đối với quy trình sản xuất liệu pháp tế bào và gen đang ngày càng tăng, tuy nhiên tương lai cho các nhà phát triển không hoàn toàn ảm đạm. Việc chuẩn hóa quy trình và những tiến bộ trong sản xuất, cũng như nền tảng kỹ thuật số đang giúp họ định hướng chiến lược thích nghi trong bối cảnh pháp lý CMC đang thay đổi.
Thông điệp từ FDA rất rõ ràng, việc lập kế hoạch CMC sớm và thực hiện quyết liệt giờ đây không còn là tùy chọn, mà đã trở thành yêu cầu bắt buộc đối với các nhà phát triển liệu pháp tế bào và gen.
NGUỒN