LIỆU PHÁP CAR-T, TCR-T
Biểu hiện TCR trên tế bào CAR-T giúp cải thiện tính an toàn và hiệu quả trong điều trị ung thư
Liệu pháp tế bào T đã mang lại những cải thiện đáng kể về khả năng điều trị ung thư, đặc biệt với sự phát triển của công nghệ chỉnh sửa gen giúp cải biến đặc tính vốn có của tế bào miễn dịch. Đối với liệu pháp CAR-T, tế bào T biểu hiệu thụ thể kháng nguyên khảm (chimeric antigen receptor – CAR) được thiết kế để nhận diện và tiêu diệt tế bào ung thư. CAR-T cho những kết quả đầy hứa hẹn trong điều trị ung thư máu, nhưng gặp nhiều cản trở ở u đặc bởi nhiều nguyên nhân, trong đó có việc tấn công cả tế bào khỏe mạnh có cùng protein đích với tế bào ung thư. Ngược lại, liệu pháp TCR-T sử dụng các thụ thể tế bào T (T cell receptor – TCR) có nguồn gốc tự nhiên, khả năng phân biệt tốt hơn giữa tế bào khối u và tế bào bình thường, nhưng hiệu quả có nhiều hạn chế. Một nhóm nghiên cứu tại Đại học Oxford và Viện Ung thư Quốc gia (Hoa Kỳ), hợp tác với Đại học Montréal (Canada) đã tìm giải pháp khắc phục các nhược điểm trên bằng cách tạo ra các tế bào biểu hiện cả CAR và TCR. Họ đã kiểm chứng trên nền tảng robot IMMUNOtron thông lượng cao và mô hình động vật, kết quả cho thấy tín hiệu TCR hoạt động như một cái phanh để giảm thiểu phản ứng quá mức của CAR, thay vì kích hoạt chúng. Mô hình toán học lý thuyết đã xác định việc điều chỉnh phản ứng miễn dịch bằng cách sử dụng các TCR tự nhiên, và chứng minh được sự điều hòa phản ứng miễn dịch với khả năng cân bằng giữa “bàn đạp phanh” và “bàn đạp ga” của tế bào T. Từ đó, nhóm nghiên cứu phát triển sản phẩm CAR-T mới với Hệ thống phanh chống đối kháng (Antagonism-Enforced Braking System – AEBS), bằng cách thêm một TCR có nhiệm vụ ức chế CAR-T hoạt động trên mô khỏe mạnh bởi các protein trên tế bào bình thường, nhưng khi gặp phiên bản đột biến của các protein này trên tế bào ung thư thì kích thích hoạt động mạnh mẽ. Chiến lược này giúp AEBS CAR-T ít gây hại với tế bào khỏe mạnh, đồng thời tăng hiệu quả kháng u. Thành công này đã mở đường cho một chiến lược mới trong liệu pháp miễn dịch điều trị ung thư. Định hướng tiếp theo của nhóm nghiên cứu là tập trung vào việc tăng cường tương tác giữa các thụ thể và tế bào AEBS CAR-T, nhằm tạo ra sản phẩm miễn dịch chống ung thư an toàn hơn, hiệu quả hơn trong những năm tới trên nhiều loại bệnh ung thư. TÀI LIỆU THAM KHẢO Kondo T., et al. (2025). Engineering TCR-controlled fuzzy logic into CAR T cells enhances therapeutic specificity. Cell, 188(9), 2372-2389. DOI: https://doi.org/10.1016/j.cell.2025.03.017
23/01/2026
FDA loại bỏ các chiến lược đánh giá và giảm thiểu rủi ro cho liệu pháp CAR-T tự thân trong điều trị ung thư
Ngày 27 tháng 6 năm 2025, Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (The U.S. Food and Drug Administration – US FDA) đã ra thông báo chính thức xác định: tính an toàn và hiệu quả của các liệu pháp CAR-T tự thân đã được chấp thuận có thể được đảm bảo mà không cần các chiến lược đánh giá và giảm thiểu rủi ro (Risk Evaluation and Mitigation Strategies – REMS). Liệu pháp CAR-T sử dụng các tế bào T mang thụ thể kháng nguyên khảm (Chimeric Antigen Receptor – CAR) được thiết kế nhân tạo để phát hiện đặc hiệu và tiêu diệt các tế bào ung thư. Liệu pháp CAR-T đã đạt nhiều thành tựu trong điều trị các bệnh lý huyết học ác tính, ngoài ra cũng cho thấy những tín hiệu lạc quan với ung thư u đặc, các bệnh tự miễn. Mặc dù vậy, liệu pháp này cũng có những rủi ro đáng kể cho bệnh nhân, bao gồm hội chứng giải phóng cytokine, hội chứng độc tính thần kinh liên quan đến tế bào miễn dịch, nhiễm trùng, nguy cơ mắc ung thư thứ phát,… REMS là chương trình an toàn mà FDA có thể yêu cầu đối với một số loại thuốc có vấn đề nghiêm trọng về độ an toàn, giúp đảm bảo lợi ích của thuốc lớn hơn rủi ro. FDA quyết định rằng REMS không còn cần thiết và cần bị loại bỏ khỏi các sản phẩm CAR-T tự thân sau (đã được FDA cấp phép trong điều trị các bệnh huyết học ác tính): - Abecma (idecabtagene vicleucel) - Breyanzi (lisocabtagene maraleucel) - Carvykti (ciltacabtagene autoleucel) - Kymriah (tisagenlecleucel) - Tecartus (brexucabtagene autoleucel) - Yescarta (axicabtagene ciloleucel) Việc loại bỏ REMS với các sản phẩm trên đồng nghĩa với việc tháo gỡ các yêu cầu những bệnh viện/phòng khám sử dụng chúng phải được chứng nhận đặc biệt và có sẵn thuốc tocilizumab (kháng thể đơn dòng điều trị một số bệnh viêm và tự miễn). Thông tin về các rủi ro được thể hiện đầy đủ trên nhãn sản phẩm, bao gồm hội chứng giải phóng cytokine và độc tính thần kinh. Các bác sỹ và các tổ chức hiện có nhiều kinh nghiệm hơn trong kiểm soát độc tính của những sản phẩm CAR-T đã được chấp thuận. Việc loại bỏ REMS giúp đẩy nhanh việc cung cấp liệu pháp cho người bệnh và giảm gánh nặng cho các nhà cung cấp. Các sản phẩm vẫn phải tuân theo quy định về giám sát an toàn, thông qua các yêu cầu báo cáo tác dụng phụ theo quy định. FDA tiếp tục yêu cầu các nhà sản xuất tiến hành các nghiên cứu quan sát đánh giá độ an toàn trong quá trình sử dụng (bao gồm cả nguy cơ mắc ung thư thứ phát) với việc theo dõi bệnh nhân trong 15 năm sau khi sử dụng, và cam kết thông báo cho công chúng khi có thông tin mới về tác dụng phụ nghiêm trọng của các sản phẩm này. TÀI LIỆU THAM KHẢO Thông cáo báo chí của FDA ngày 27 tháng 06 năm 2025 về việc loại bỏ các chiến lược đánh giá và giảm thiểu rủi ro (REMS) cho liệu pháp miễn dịch tế bào CAR-T tự thân https://www.fda.gov/news-events/press-announcements/fda-eliminates-risk-evaluation-and-mitigation-strategies-rems-autologous-chimeric-antigen-receptor
23/01/2026
Liệu pháp TCR-T trong điều trị ung thư
1. Liệu pháp TCR-T là gì Thụ thể tế bào T (T-cell receptor, TCR) là phức hợp protein trên tế bào T, có chức năng nhận diện các mảnh kháng nguyên dưới dạng peptide liên kết với các phân tử phức hợp phù hợp mô chính (Major Histocompatibility Complex – MHC), hay kháng nguyên bạch cầu người (Human leukocyte antigen – HLA). Sự liên kết giữa TCR và phức hợp MHC-kháng nguyên dẫn đến hoạt hóa tế bào T để bắt đầu phản ứng miễn dịch. Trong liệu pháp tế bào T với TCR sửa đổi (TCR-engineered T cell, TCR-T), tế bào T được chỉnh sửa để biểu hiện các TCR nhất định có khả năng nhận biết đặc hiệu với kháng nguyên cụ thể nào đó trên tế bào ung thư, giúp tế bào T nhắm mục tiêu và tiêu diệt tế bào ung thư. Ví dụ: TECELRA (Afamitresgene autoleucel), là sản phẩm TCR-T đầu tiên và duy nhất hiện nay được FDA phê duyệt (tháng 08/2024), dùng trong điều trị sarcoma hoạt dịch, với các tế bào T biểu hiện TCR hướng đến kháng nguyên MAGE-A4 được biểu hiện mạnh ở các tế bào sarcoma hoạt dịch. Một phương pháp cải biến phổ biến khác để tăng tính đặc hiệu của tế bào T là chuyển gen biểu hiện thụ thể kháng nguyên khảm (Chimeric Antigen Receptor – CAR, xem bài viết về CAR-T tại https://www.facebook.com/share/p/1Epva8XNKz/). Liệu pháp TCR-T khác CAR-T ở 2 điểm chính: TCR-T sửa đổi một thụ thể tự nhiên trong khi CAR-T sử dụng thụ thể tổng hợp nhân tạo, TCR-T liên kết với các protein bất thường thường thấy bên trong tế bào ung thư nhưng được MHC di truyển đến bề mặt tế bào còn CAR-T nhắm vào các protein bất thường trên bề mặt tế bào ung thư. 2. Quy trình thực hiện liệu pháp TCR-T - Sàng lọc bệnh nhân, phân loại HLA - Sinh thiết khối u, sàng lọc mô khối u để tìm kháng nguyên mục tiêu - Phân lập tế bào T của bệnh nhân từ máu ngoại vi hoặc từ khối u (TIL) - Phân lập TCR đặc hiệu đích từ người hiến khỏe mạnh, được biến đổi và chuyển vào tế bào T của bệnh nhân - Nuôi cấy tăng sinh tế bào TCR-T - Truyền cho bệnh nhân (đã được điều trị điều hóa để làm suy giảm lympho) kết hợp truyền interleukin 2 (IL-2) để duy trì TCR-T trong cơ thể bệnh nhân 3. Dữ liệu lâm sàng về liệu pháp TCR-T Đến thời điểm hiện tại, có 1 liệu pháp TCR-T được FDA phê duyệt, đó là TECELRA (Afamitresgene autoleucel) dùng trong điều trị sarcoma hoạt dịch, với đích là kháng nguyên A4 liên quan đến ung thư hắc tố (MAGE-A4). Quyết định này dựa trên kết quả thử nghiệm lâm sàng nhãn mở, đa trung tâm, giai đoạn II có tên gọi SPEARHEAD-1, với 52 bệnh nhân bị sarcoma hoạt dịch không thể cắt bỏ hoặc di căn đã được hóa trị trước đó, với 44 bệnh nhân đủ điều kiện sử dụng liệu pháp. Kết quả cho thấy 43,2% bệnh nhân được điều trị đáp ứng với afami-cel, thời gian bắt đầu đáp ứng trung bình là 4,9 tuần, thời gian đáp ứng trung bình 6 tháng. Trong số này, 45,6% và 39,0% số bệnh nhân đáp ứng điều trị có thời gian đáp ứng kéo dài ít nhất 6 tháng và 12 tháng. Ngoài ra, liệu pháp TCR-T đã được thử nghiệm trên nhiều loại ung thư khác nhau, hầu hết là u rắn, như u hắc tố di căn, ung thư vòng họng, ung thư cổ tử cung, ung thư liên quan đến virus HPV,… Rất nhiều trong số đó đã thu được những kết quả khả quan. 4. Những ưu điểm và thách thức của liệu pháp TCR-T TCR-T có những ưu điểm khiến các nhà ung thư học quan tâm như phạm vi nhận diện kháng nguyên rộng hơn CAR-T (đặc biệt là kháng nguyên nội bào), phù hợp với nhiều loại ung thư (gồm cả u đặc và ung thư máu, trong đó u đặc chưa có nhiều kết quả tốt với CAR-T), ít tác dụng phụ liên quan đến cytokine hơn. Mặc dù vậy, TCR-T gặp những hạn chế dẫn đến chưa có nhiều sản phẩm được chấp thuận, chưa mang lại lợi ích lâm sàng rõ rệt cho bệnh nhân: khó khăn trong việc lựa chọn kháng nguyên đích và TCR tiềm năng, sự thoát khỏi miễn dịch của khối u, nhận diện kém và tấn công tế bào lành gây nên bệnh lý thứ phát nguy hiểm, không phản ứng hoặc nhanh chóng suy giảm sau khi đưa vào cơ thể người bệnh,… --------- TÀI LIỆU THAM KHẢO 1. Tsimberidou A. M., et al. (2021). T-cell receptor-based therapy: an innovative therapeutic approach for solid tumors. Journal of Hematology & Oncology, 14, 1-22. DOI: 10.1186/s13045-021-01115-0 2. Shafer P., et al. (2022). Cancer therapy with TCR-engineered T cells: current strategies, challenges, and prospects. Frontiers in immunology, 13, 835762. DOI: 10.3389/fimmu.2022.835762 3. Liu Y., et al. (2022). TCR-T immunotherapy: the challenges and solutions. Frontiers in oncology, 11, 794183. DOI: 10.3389/fonc.2021.794183 4. Baulu E., et al. (2023). TCR-engineered T cell therapy in solid tumors: State of the art and perspectives. Science Advances, 9(7), eadf3700. DOI: 10.1126/sciadv.adf370 5. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-accelerated-approval-afamitresgene-autoleucel-unresectable-or-metastatic-synovial-sarcoma
23/01/2026
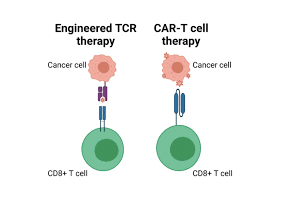
Cải biến di truyền giúp tăng cường hiệu quả liệu pháp tế bào miễn dịch trong điều trị ung thư: TCR-T và CAR-T
1. Liệu pháp miễn dịch tế bào T Các liệu pháp miễn dịch tế bào T khác nhau tùy thuộc vào nguồn gốc tế bào, cách thức xử lý ngoài cơ thể và phương thức tế bào T nhận diện mục tiêu khi được truyền cho bệnh nhân. Các chiến lược khai thác liệu pháp miễn dịch tế bào T bao gồm: - Liệu pháp tế bào lympho thâm nhiễm khối u (Tumor-Infiltrating Lymphocyte, TIL): sử dụng các tế bào T trong khối u, với thụ thể tế bào T tự nhiên nhận diện các mục tiêu trên tế bào ung thư (xem bài viết về liệu pháp TIL tại https://ysinhtebao.com/lieu-phap-tb-mien-dich-khac/lieu-phap-til-trong-dieu-tri-u-dac-trien-vong-va-thach-thuc). - Liệu pháp thụ thể tế bào T (T Cell Receptor-Engineered T Cell, TCR-T): Sử dụng các kỹ thuật di truyền để thiết kế các thụ thể tế bào T, bổ sung cho tế bào T giúp chúng nhận diện mục tiêu trên tế bào ung thư. - Liệu pháp tế bào T với thụ thể kháng nguyên khảm (Chimeric Antigen Receptor T cell, CAR-T): sử dụng kỹ thuật di truyền để tạo ra các thụ thể nhân tạo, cung cấp cho tế bào T giúp chúng phát hiện các mục tiêu trên tế bào ung thư mà thụ thể tự nhiên không nhận diện được. 2. Liệu pháp TCR-T: biến đổi di truyền thụ thể tế bào T Nhờ thụ thể tế bào T (T Cell Receptor – TCR), tế bào T có khả năng nhận biết tự nhiên đối với các mục tiêu như vi khuẩn, virus, tế bào ung thư,... và tiêu diệt chúng. Đối với liệu pháp TCR-T, các nhà nghiên cứu ung thư đã xác định một dấu hiệu trên các tế bào ung thư, thiết kế một TCR nhận dạng được dấu hiệu đó, sau đó tách tế bào T từ bệnh nhân và thêm vào đó gen mã hóa TCR đã thiết kế để tạo nên TCR-T phát hiện tốt các tế bào ung thư. Liệu pháp TCR-T đã được thử nghiệm lâm sàng để điều trị nhiều loại ung thư khác nhau, trong đó thu được những tín hiệu tích cực đối với u đặc. Tháng 08/2024, Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (US FDA) đã chấp thuận sản phẩm TECELRA (Afamitresgene autoleucel), là sản phẩm TCR-T tự thân hướng đến kháng nguyên A4 liên quan đến ung thư hắc tố (MAGE-A4) dùng trong điều trị sarcoma hoạt dịch. Các chiến lược hiện nay về TCR-T đang hướng đến khắc phục những nhược điểm khiến bệnh nhận hưởng những lợi ích hạn chế lâm sàng, bao gồm giảm độc tính trên bệnh nhân, tăng cường các dấu hiệu nhận diện khối u – đặc biệt là các tân kháng nguyên – để cải thiện hiệu quả và ngăn ngừa tổn thương cho các tế bào và mô khỏe mạnh. 3. Liệu pháp CAR-T: thụ thể nhân tạo nhận diện tế bào ung thư CAR-T là liệu pháp tế bào miễn dịch trong đó tế bào T được biến đối với một thụ thể nhân tạo, được gọi là thụ thể kháng nguyên khảm (Chimeric Antigen Receptor – CAR), để nhận diện tế bào ung thư. Tế bào T tự nhiên có TCR cho phép chúng phát hiện nhiều phân tử mà chúng xác định là tế bào ung thư, nhưng không phải tất cả các kháng nguyên, do đó các nhà nghiên cứu thiết kế nên CAR để phát hiện những thụ thể bề mặt mà TCR không nhận diện được. Liệu pháp CAR-T đã chứng minh hiệu quả trong điều trị các bệnh lý ác tính huyết học. Hiện tại đã có 7 sản phẩm được US FDA cấp phép: 5 sản phẩm nhận diện CD19 trong điều trị u lympho và bệnh bạch cầu, gồm KYMRIAH (Tisagenlecleucel, được cấp phép tháng 08/2017), YESCARTA (Axicabtagene ciloleucel, 10/2017), TECARTUS (Brexucabtagene autoleucel, 07/2020), BREYANZI (Lisocabtagene maraleucel, 02/2021), AUCATZYL (Obecabtagene autoleucel, 11/2024); 2 sản phẩm nhận diện kháng nguyên trưởng thành tế bào B trong điều trị đa u tủy xương, gồm ABECMA (Idecabtagene vicleucel, được cấp phép tháng 03/2021), CARVYKTI (Ciltacabtagene autoleucel, 02/2022). 4. Những khác biệt giữa liệu pháp TCR-T và CAR-T Cả hai liệu pháp này đều sử dụng các kỹ thuật di truyền để biến đổi tế bào T, khai thác sức mạnh của hệ thống miễn dịch nhằm điều trị ung thư, nhưng có một số khác biệt chính. Về mặt cấu trúc: TCR là các thụ thể tự nhiên hoặc được biến đổi hạn chế để nhận diện các kháng nguyên khối u. CAR được thiết kế nhân tạo để nhận diện kháng nguyên cụ thể, đồng thời người ta có thể bổ sung trên cấu trúc CAR các vùng giúp tăng cường hoạt động cũng như duy trì sự hoạt hóa và sống còn của tế bào T. Về khả năng nhận diện kháng nguyên: TCR nhận diện các kháng nguyên có trên bề mặt và bên trong tế bào, được trình diện trên bề mặt qua kháng nguyên bạch cầu người (HLA), cần có sự tương thích HLA giữa bệnh nhân và TCR. CAR nhận diện các kháng nguyên trên bề mặt tế bào và không phụ thuộc HLA. Vì thế, TCR có thể nhận diện kháng nguyên phổ rộng hơn CAR. Về ứng dụng lâm sàng: TCR-T có nhiều hứa hẹn với các dạng ung thư u đặc như u hắc tố, ung thư phổi, ung thư cổ tử cung,… CAR-T chủ yếu điều trị các bệnh lý ác tính về máu như bệnh bạch cầu cấp/mạn dòng lympho (ALL/CLL), u lympho tế bào B lớn (LBCLu lympho tế bào B lớn (LBCL), u lympho dòng lympho nhỏ (SLL), u lympho nang (FL), u lympho tế bào màng ngoài (MCL), đa u tủy xương,… và khó hiệu quả với u đặc do hàng rào mô, môi trường vi mô ức chế. TÀI LIỆU THAM KHẢO 1. Shafer P., et al. (2022). Cancer therapy with TCR-engineered T cells: current strategies, challenges, and prospects. Frontiers in immunology, 13, 835762. DOI: 10.3389/fimmu.2022.835762 2. Baulu E., et al. (2023). TCR-engineered T cell therapy in solid tumors: State of the art and perspectives. Science Advances, 9(7), eadf3700. DOI: 10.1126/sciadv.adf3700 3. Sterner R. C., et al. (2021). CAR-T cell therapy: current limitations and potential strategies. Blood cancer journal, 11(4), 69. DOI: 10.1038/s41408-021-00459-7 4. Chen Y. J., et al. (2023). CAR-T: what is next?. Cancers, 15(3), 663. DOI: 10.3390/cancers15030663 5. Haanen J., et al. (2024). Adoptive cell therapy for solid tumors: current status in melanoma and next-generation therapies. American Society of Clinical Oncology Educational Book, 44(3), e431608. DOI: 10.1200/EDBK_431608 6. https://www.fda.gov/vaccines-blood-biologics/cellular-gene-therapy-products/approved-cellular-and-gene-therapy-products
23/01/2026
Nguy cơ ung thư thứ phát sau điều trị bằng liệu pháp CAR-T: kết luận của Cơ quan Dược phẩm Châu Âu (EMA) dựa trên đánh giá 38 trường hợp nghi ngờ
Liệu pháp tế bào T mang thụ thể kháng nguyên khảm (chimeric antigen receptor T-cell, CAR-T) là liệu pháp điều trị ung thư và một số bệnh lý khác, sử dụng các tế bào T chứa thụ thể có khả năng nhận diện một yếu tố nhất định trên tế bào đích để tiêu diệt chúng. Tính đến nay, Cơ quan Dược phẩm Châu Âu (the European Medicines Agency, EMA) đã khuyến cáo lưu hành 6 sản phẩm CAR-T để điều trị các bệnh lý ung thư huyết học, bao gồm tisagenlecleucel (Kymriah), lisocabtagene maraleucel (Breyanzi), axicabtagene ciloleucel (Yescarta), brexucabtagene autoleucel (Tecartus), idecabtagene vicleucel (Abecma) và ciltacabtagene autoleucel (Carvykti). Quy trình sản xuất CAR-T thường sử dụng vector lentivirus để chuyển gen vào tế bào T, mang đến những lo ngại về việc chèn trình tự DNA vào gen hoạt động, có thể góp phần gây ung thư. Rủi ro này được nêu rõ trong thông tin sản phẩm và khuyến nghị cần theo dõi bệnh nhân suốt đời, kết hợp đánh giá chặt chẽ những phản ứng bất lợi sau khi sử dụng sản phẩm. Cuối năm 2023, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (the United States Food and Drug Administration, US FDA) đã thông báo ghi nhận nhiều trường hợp bệnh nhân được phát hiện bệnh lý ác tính tế bào T sau khi sử dụng liệu pháp CAR-T. Trong nghiên cứu này, các nhà nghiên cứu của EMA kết hợp nhiều đơn vị trên toàn châu Âu đã phân tích các trường hợp mắc bệnh ác tính tế bào T sau sử dụng liệu pháp CAR-T, nhằm đánh giá sự rủi ro của liệu pháp này trong khía cạnh gây ung thư thứ phát. Tính đến ngày 11/04/2024, đã có 38 trường hợp bệnh nhân 29-80 tuổi mắc bệnh ác tính tế bào T (trong tổng số khoảng 42.500 bệnh nhân sử dụng) sau khi điều trị với 1 trong 6 sản phẩm CAR-T được EMA khuyến nghị cấp phép (tỷ lệ khoảng 1/1.000). Hầu hết các trường hợp này được chẩn đoán trong vòng 12 tháng sau điều trị. Trong 38 bệnh nhân này, 19 bệnh nhân được xét nghiệm sự hiện diện của gen chuyển CAR trong mẫu khối u, và phát hiện ở 7 trường hợp, số lượng bản sao thấp ở 5 trường hợp, và 7 trường hợp còn lại âm tính. Không có dữ liệu cho thấy bất kỳ trường hợp nào có dòng tế bào CAR chiếm ưu thế ở thời điểm đánh giá, chưa phát hiện loại virus nào liên quan đến vector chuyển gen có khả năng nhân lên ở bất cứ thời điểm nào được khảo sát. Nhóm nghiên cứu nhận định: nguy cơ mắc bệnh ác tính thứ phát có nguồn gốc từ tế bào T dường như thấp (tỷ lệ khoảng 1/1.000), và "có khả năng" các bệnh này có liên quan đến liệu pháp CAR-T. Dựa trên những dữ liệu hiện có, kết hợp xem xét cơ chế và tác dụng của liệu pháp CAR-T, EMA kết luận rằng đây là tác dụng chung của nhóm sản phẩm, ngay cả khi không phải tất cả các sản phẩm đều có trường hợp mắc bệnh lý ác tính tế bào T được báo cáo. Kết luận này đã dẫn đến các hành động quản lý tập trung vào các biện pháp giảm thiểu rủi ro, bao gồm cập nhật thông tin sản phẩm, kế hoạch quản lý rủi ro, tài liệu giáo dục, tăng cường xét nghiệm di truyền trên các mẫu khối u còn lại sau điều trị,… Các cơ chế cơ bản dẫn đến sự phát triển của các bệnh ung thư thứ phát có nguồn gốc từ tế bào T ở bệnh nhân sau sử dụng CAR-T vẫn chưa được làm rõ. Những khía cạnh được cân nhắc đến bao gồm nguy cơ đột biến chèn khi chuyển gen, quá trình sản xuất ảnh hưởng đến điều hòa biểu hiện gen, điều trị điều kiện hóa trước truyền CAR-T làm suy yếu khả năng loại bỏ các tế bào tiền ác tính,… Mắc dù vậy, vẫn cần có những quan sát tích lũy trong quá trình thử nghiệm và lưu hành sản phẩm CAR-T để theo dõi được số lượng bệnh nhân lớn hơn để đưa ra được những kết luận chính xác. TÀI LIỆU THAM KHẢO Berg P., et al. (2025). Secondary malignancy of T-cell origin after CAR T-cell therapy: EMA’s conclusions from the evaluation of 38 suspected cases. Gene Therapy, 1-6. DOI: https://doi.org/10.1038/s41434-025-00586-x
23/01/2026
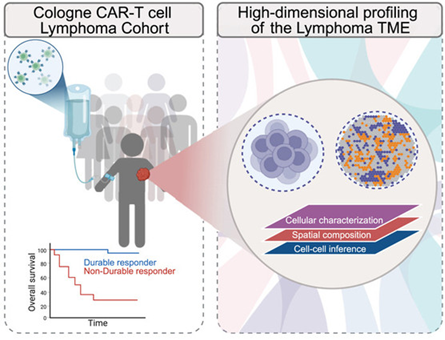
Phát hiện “hàng rào” tế bào làm giảm hiệu quả điều trị của liệu pháp CAR-T trong bệnh u lympho
Liệu pháp CAR-T sử dụng các tế bào T mang thụ thể kháng nguyên khảm (Chimeric Antigen Receptor – CAR) được thiết kế nhân tạo, nhờ đó chúng có thể phát hiện đặc hiệu và tiêu diệt các tế bào ung thư. CAR-T đã tạo nên bước đột phá trong điều trị nhiều bệnh lý huyết học ác tính, trong đó có u lympho tế bào B tái phát hoặc kháng trị - loại u lympho không Hodgkin phổ biến nhất. Tuy nhiên, có đến 50% số bệnh nhân được điều trị bằng liệu pháp này không duy trì khả năng đáp ứng ban đầu, hoặc tái phát sau điều trị, thậm chí tử vong. Cơ chế kháng CAR-T của bệnh này vẫn chưa được hiểu rõ hoàn toàn. Trong một nghiên cứu mới đăng trên tạp chí Cancer Cell tháng 5 năm 2025, các nhà khoa học đã phân tích sự khác biệt giữa những bệnh nhân có đáp ứng lâu dài so với nhóm kém đáp ứng với liệu pháp CAR-T. Nhóm tác giả đã phân tích mẫu u lympho của các bệnh nhân: giải trình tự RNA số lượng lớn để phân tích hoạt đột gen tổng thể của toàn bộ mẫu, giải trình tự RNA tế bào đơn để kiểm tra hoạt động gen của từng tế bào, tạo bản đồ vị trí các loại tế bào khác nhau và sự tương tác giữa chúng,… Mục tiêu cuối cùng là xác định các mục tiêu cụ thể trong môi trường vi mô của khối u có thể được điều chỉnh để cải thiện liệu pháp tế bào CAR-T. Nhóm nghiên cứu đã xác định được các tế bào đơn dòng tủy dương tính với CSF1R (một loại thụ thể có mặt trên bề mặt của các tế bào như microglia và đại thực bào, đóng vai trò quan trọng trong sự phát triển, sống sót và duy trì của microglia), còn gọi là tế bào LAMM, tăng đáng kể ở những bệnh nhân đáp ứng kém. Họ phát hiện ra rằng tế bào LAMM ức chế CAR-T thông qua con đường liên quan đến tín hiệu prostaglandin E2 (PGE2), sự tương tác giữa LAMM và một số thụ thể trên tế bào T làm vô hiệu hóa khả năng tăng sinh và tiêu diệt tế bào ung thư của CAR-T. Kết quả này cho thấy các tế bào LAMM hoạt động như một rào cản, bảo vệ khối u khỏi tế bào CAR-T. Tuy nhiên, hiện tại đã có thuốc được phê duyệt với tác dụng ức chế CSF1R (Sotuletinib hay BLZ-945), có thể phá vỡ hàng rào này, khi kết hợp với CAR-T trên mô hình chuột đã cải thiện hiệu quả điều trị một cách đáng kể. Đây có thể là bước đột phá trong chiến lược điều trị cho hàng nghìn bệnh nhân u lympho tế bào B kháng trị với liệu pháp CAR-T. TÀI LIỆU THAM KHẢO Stahl D., et al. (2025). CSF1R+ myeloid-monocytic cells drive CAR-T cell resistance in aggressive B cell lymphoma. Cancer cell. DOI: https://doi.org/10.1016/j.ccell.2025.05.013
22/01/2026
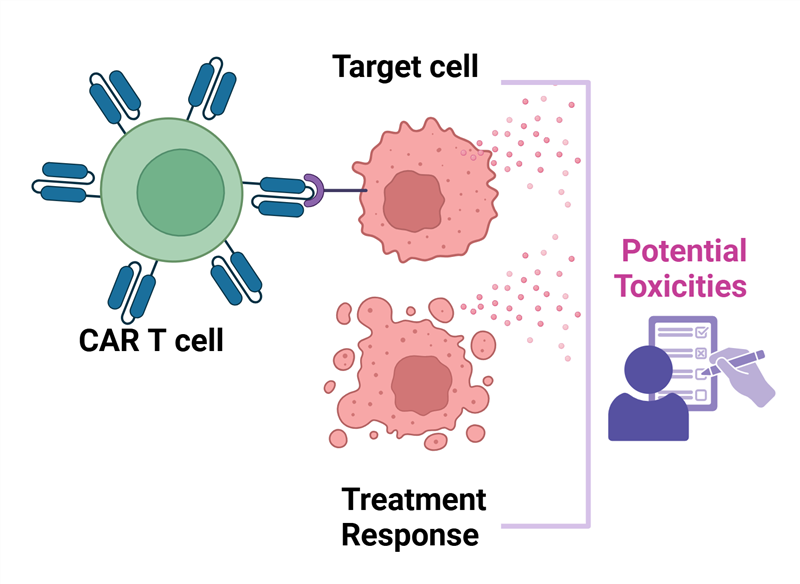
Liệu pháp CAR-T: bước đột phá của liệu pháp tế bào trong điều trị ung thư
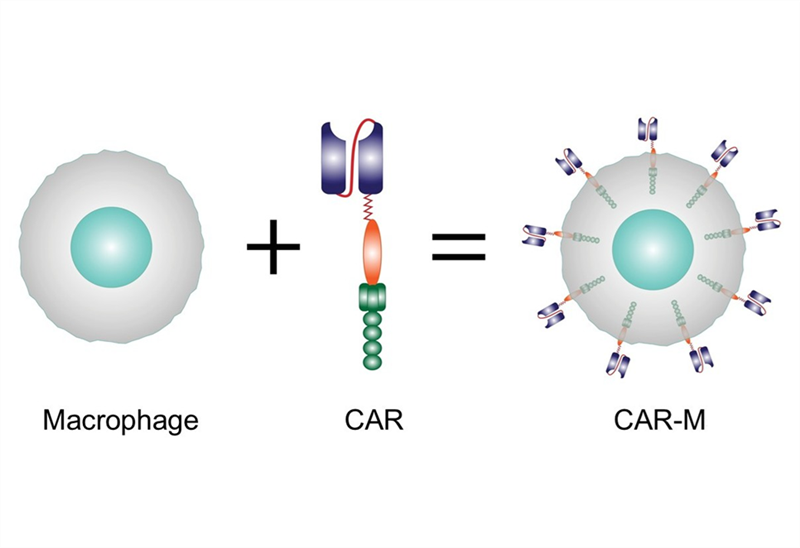
Thụ thể kháng nguyên khảm (Chimeric Antigen Receptor, CAR) là các protein thụ thể được thiết kế bao gồm cả chức năng liên kết với kháng nguyên đặc hiệu và chức năng kích hoạt tế bào miễn dịch. Các tế bào T mang cấu trúc CAR (CAR-T) có khả năng phát hiện đặc hiệu các tế bào ung thư, điều mà tế bào T bình thường không làm được hoặc nhận diện kém. Khi được truyền vào cơ thể bệnh nhân, tế bào CAR-T đi tìm và tiêu diệt tế bào ác tính, đồng thời có khả năng nhân lên để duy trì nguồn “thuốc sống” này trong cơ thế, ức chế ung thư.
22/01/2026