Liệu pháp TCR-T trong điều trị ung thư
1. Liệu pháp TCR-T là gì
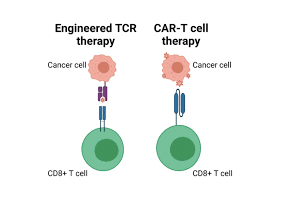
Thụ thể tế bào T (T-cell receptor, TCR) là phức hợp protein trên tế bào T, có chức năng nhận diện các mảnh kháng nguyên dưới dạng peptide liên kết với các phân tử phức hợp phù hợp mô chính (Major Histocompatibility Complex – MHC), hay kháng nguyên bạch cầu người (Human leukocyte antigen – HLA). Sự liên kết giữa TCR và phức hợp MHC-kháng nguyên dẫn đến hoạt hóa tế bào T để bắt đầu phản ứng miễn dịch.
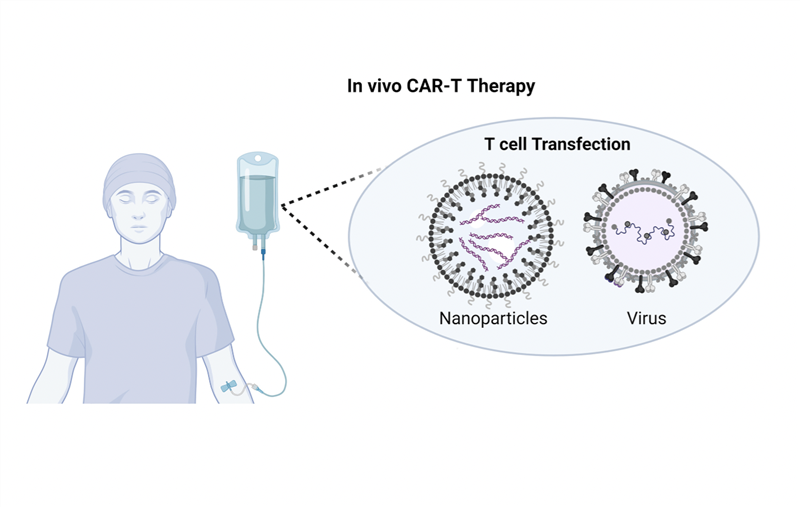
Trong liệu pháp tế bào T với TCR sửa đổi (TCR-engineered T cell, TCR-T), tế bào T được chỉnh sửa để biểu hiện các TCR nhất định có khả năng nhận biết đặc hiệu với kháng nguyên cụ thể nào đó trên tế bào ung thư, giúp tế bào T nhắm mục tiêu và tiêu diệt tế bào ung thư. Ví dụ: TECELRA (Afamitresgene autoleucel), là sản phẩm TCR-T đầu tiên và duy nhất hiện nay được FDA phê duyệt (tháng 08/2024), dùng trong điều trị sarcoma hoạt dịch, với các tế bào T biểu hiện TCR hướng đến kháng nguyên MAGE-A4 được biểu hiện mạnh ở các tế bào sarcoma hoạt dịch.
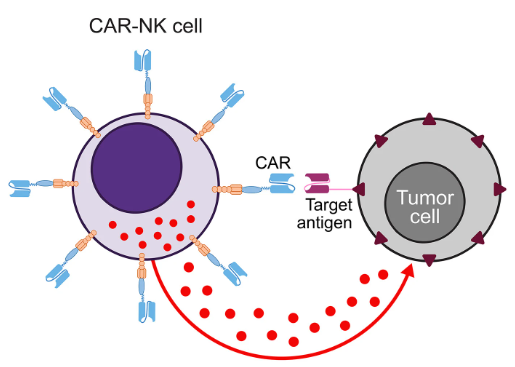
Một phương pháp cải biến phổ biến khác để tăng tính đặc hiệu của tế bào T là chuyển gen biểu hiện thụ thể kháng nguyên khảm (Chimeric Antigen Receptor – CAR, xem bài viết về CAR-T tại https://www.facebook.com/share/p/1Epva8XNKz/). Liệu pháp TCR-T khác CAR-T ở 2 điểm chính: TCR-T sửa đổi một thụ thể tự nhiên trong khi CAR-T sử dụng thụ thể tổng hợp nhân tạo, TCR-T liên kết với các protein bất thường thường thấy bên trong tế bào ung thư nhưng được MHC di truyển đến bề mặt tế bào còn CAR-T nhắm vào các protein bất thường trên bề mặt tế bào ung thư.
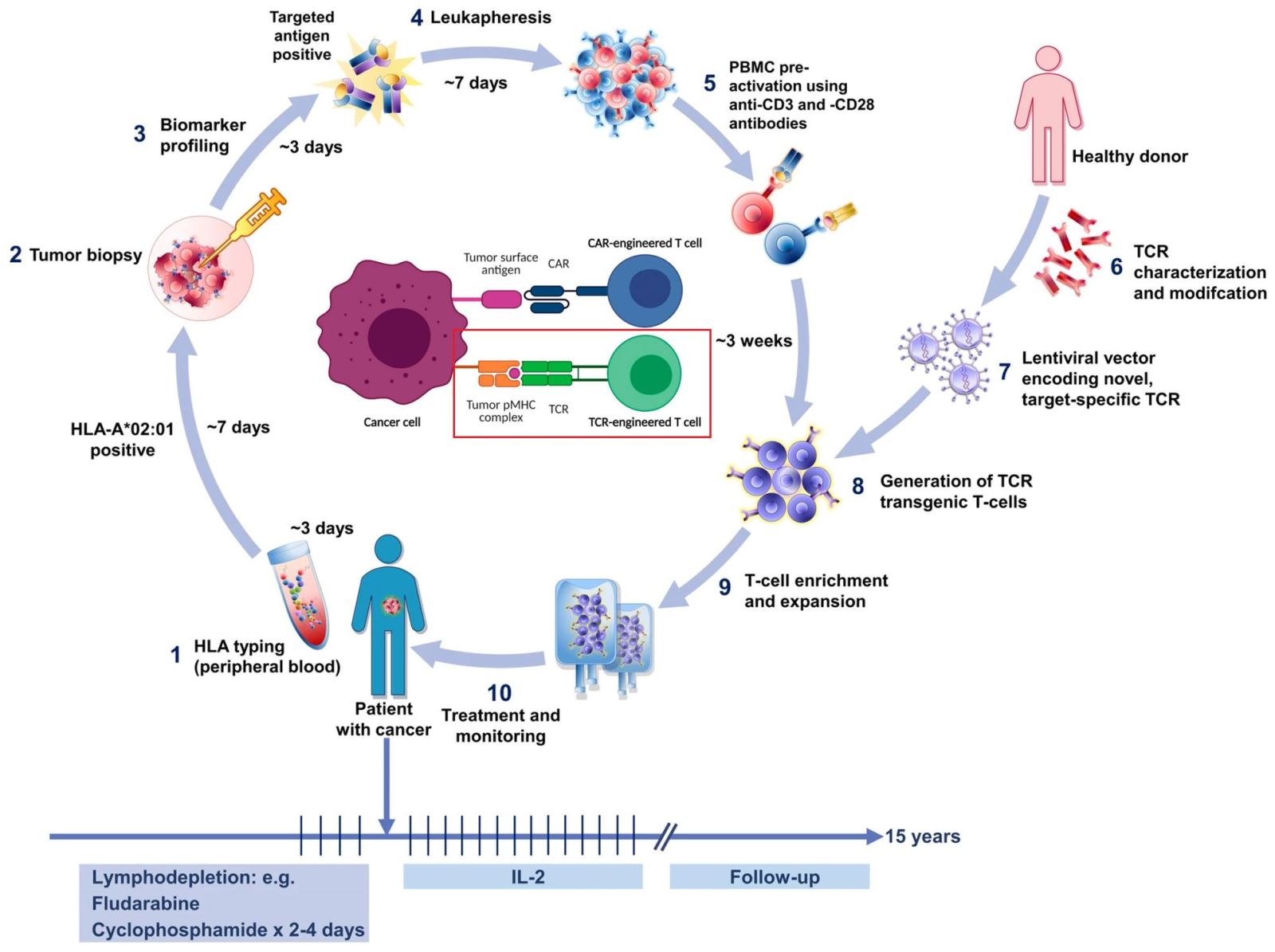
2. Quy trình thực hiện liệu pháp TCR-T
- Sàng lọc bệnh nhân, phân loại HLA
- Sinh thiết khối u, sàng lọc mô khối u để tìm kháng nguyên mục tiêu
- Phân lập tế bào T của bệnh nhân từ máu ngoại vi hoặc từ khối u (TIL)
- Phân lập TCR đặc hiệu đích từ người hiến khỏe mạnh, được biến đổi và chuyển vào tế bào T của bệnh nhân
- Nuôi cấy tăng sinh tế bào TCR-T
- Truyền cho bệnh nhân (đã được điều trị điều hóa để làm suy giảm lympho) kết hợp truyền interleukin 2 (IL-2) để duy trì TCR-T trong cơ thể bệnh nhân
3. Dữ liệu lâm sàng về liệu pháp TCR-T
Đến thời điểm hiện tại, có 1 liệu pháp TCR-T được FDA phê duyệt, đó là TECELRA (Afamitresgene autoleucel) dùng trong điều trị sarcoma hoạt dịch, với đích là kháng nguyên A4 liên quan đến ung thư hắc tố (MAGE-A4). Quyết định này dựa trên kết quả thử nghiệm lâm sàng nhãn mở, đa trung tâm, giai đoạn II có tên gọi SPEARHEAD-1, với 52 bệnh nhân bị sarcoma hoạt dịch không thể cắt bỏ hoặc di căn đã được hóa trị trước đó, với 44 bệnh nhân đủ điều kiện sử dụng liệu pháp. Kết quả cho thấy 43,2% bệnh nhân được điều trị đáp ứng với afami-cel, thời gian bắt đầu đáp ứng trung bình là 4,9 tuần, thời gian đáp ứng trung bình 6 tháng. Trong số này, 45,6% và 39,0% số bệnh nhân đáp ứng điều trị có thời gian đáp ứng kéo dài ít nhất 6 tháng và 12 tháng.
Ngoài ra, liệu pháp TCR-T đã được thử nghiệm trên nhiều loại ung thư khác nhau, hầu hết là u rắn, như u hắc tố di căn, ung thư vòng họng, ung thư cổ tử cung, ung thư liên quan đến virus HPV,… Rất nhiều trong số đó đã thu được những kết quả khả quan.
4. Những ưu điểm và thách thức của liệu pháp TCR-T
TCR-T có những ưu điểm khiến các nhà ung thư học quan tâm như phạm vi nhận diện kháng nguyên rộng hơn CAR-T (đặc biệt là kháng nguyên nội bào), phù hợp với nhiều loại ung thư (gồm cả u đặc và ung thư máu, trong đó u đặc chưa có nhiều kết quả tốt với CAR-T), ít tác dụng phụ liên quan đến cytokine hơn.
Mặc dù vậy, TCR-T gặp những hạn chế dẫn đến chưa có nhiều sản phẩm được chấp thuận, chưa mang lại lợi ích lâm sàng rõ rệt cho bệnh nhân: khó khăn trong việc lựa chọn kháng nguyên đích và TCR tiềm năng, sự thoát khỏi miễn dịch của khối u, nhận diện kém và tấn công tế bào lành gây nên bệnh lý thứ phát nguy hiểm, không phản ứng hoặc nhanh chóng suy giảm sau khi đưa vào cơ thể người bệnh,…
---------
TÀI LIỆU THAM KHẢO
1. Tsimberidou A. M., et al. (2021). T-cell receptor-based therapy: an innovative therapeutic approach for solid tumors. Journal of Hematology & Oncology, 14, 1-22. DOI: 10.1186/s13045-021-01115-0
2. Shafer P., et al. (2022). Cancer therapy with TCR-engineered T cells: current strategies, challenges, and prospects. Frontiers in immunology, 13, 835762. DOI: 10.3389/fimmu.2022.835762
3. Liu Y., et al. (2022). TCR-T immunotherapy: the challenges and solutions. Frontiers in oncology, 11, 794183. DOI: 10.3389/fonc.2021.794183
4. Baulu E., et al. (2023). TCR-engineered T cell therapy in solid tumors: State of the art and perspectives. Science Advances, 9(7), eadf3700. DOI: 10.1126/sciadv.adf370