Liệu pháp CAR-T và sự liên quan đến ung thư thứ phát – kết quả phân tích trên 783 bệnh nhân
1. CAR-T – bước đột phá của liệu pháp tế bào trong điều trị ung thư
Các tế bào T mang thụ thể kháng nguyên khảm (Chimeric Antigen Receptor T Cell – CAR-T) mang đến một giải pháp đầy hứa hẹn để điều trị một số bệnh ung thư máu, và các thử nghiệm lâm sàng hiện tại chủ yếu tập trung CAR-T đến các bệnh lý huyết học ác tính. Tính đến hết tháng 6 năm 2025, đã có 7 sản phẩm CAR-T được FDA Hoa Kỳ phê duyệt, bao gồm 5 sản phẩm trong điều trị u lympho và bệnh bạch cầu, 2 sản phẩm trong điều trị đa u tủy xương.
Ngược lại với những tiến bộ của CAR-T trong điều trị các bệnh lý huyết học ác tính, việc nghiên cứu và thử nghiệm liệu pháp này trên u đặc gặp rất nhiều hạn chế. Nguyên nhân có thể do tính không đồng nhất của kháng nguyên, vi môi trường khối u đặc ức chế miễn dịch nên ức chế hoặc bất hoạt CAR-T, rào cản vật lý và mô đệm ngăn cản tế bào CAR-T xâm nhập,… Tuy nhiên hiện nay, nhiều thử nghiệm đã có những chiến lược khắc phục hiện tượng trên, và cho thấy những tín hiệu tích cực về liệu pháp này trong điều trị u thần kinh đệm, sarcoma, ung thư biểu mô tế bào thận,…
2. Quy trình thực hiện liệu pháp CAR-T và những nghi ngại về khả năng gây ung thư thứ phát
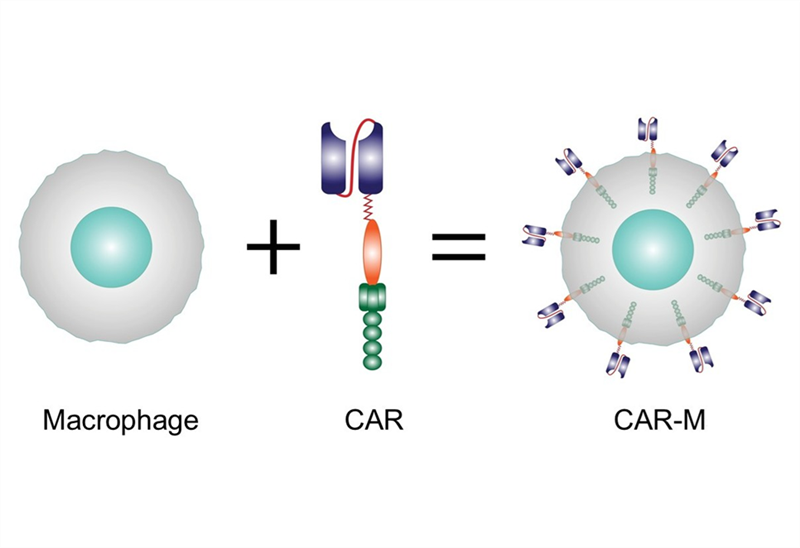
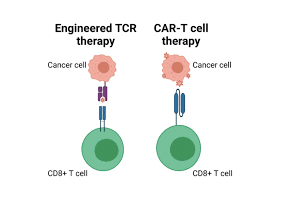
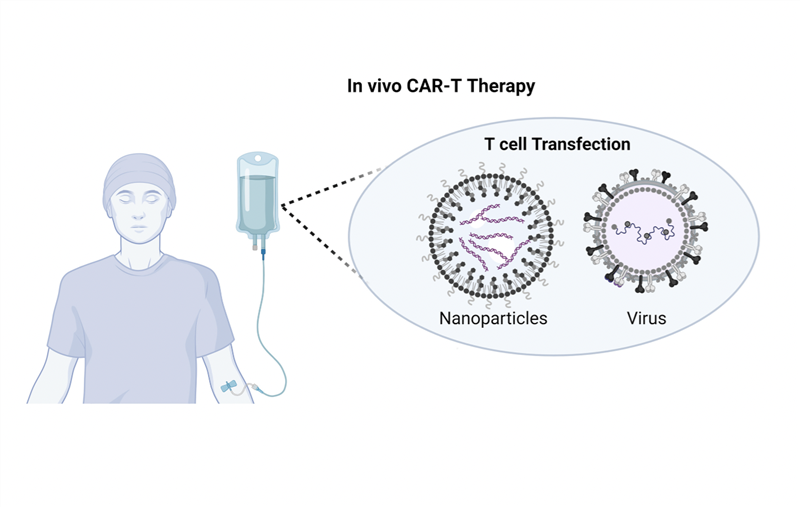
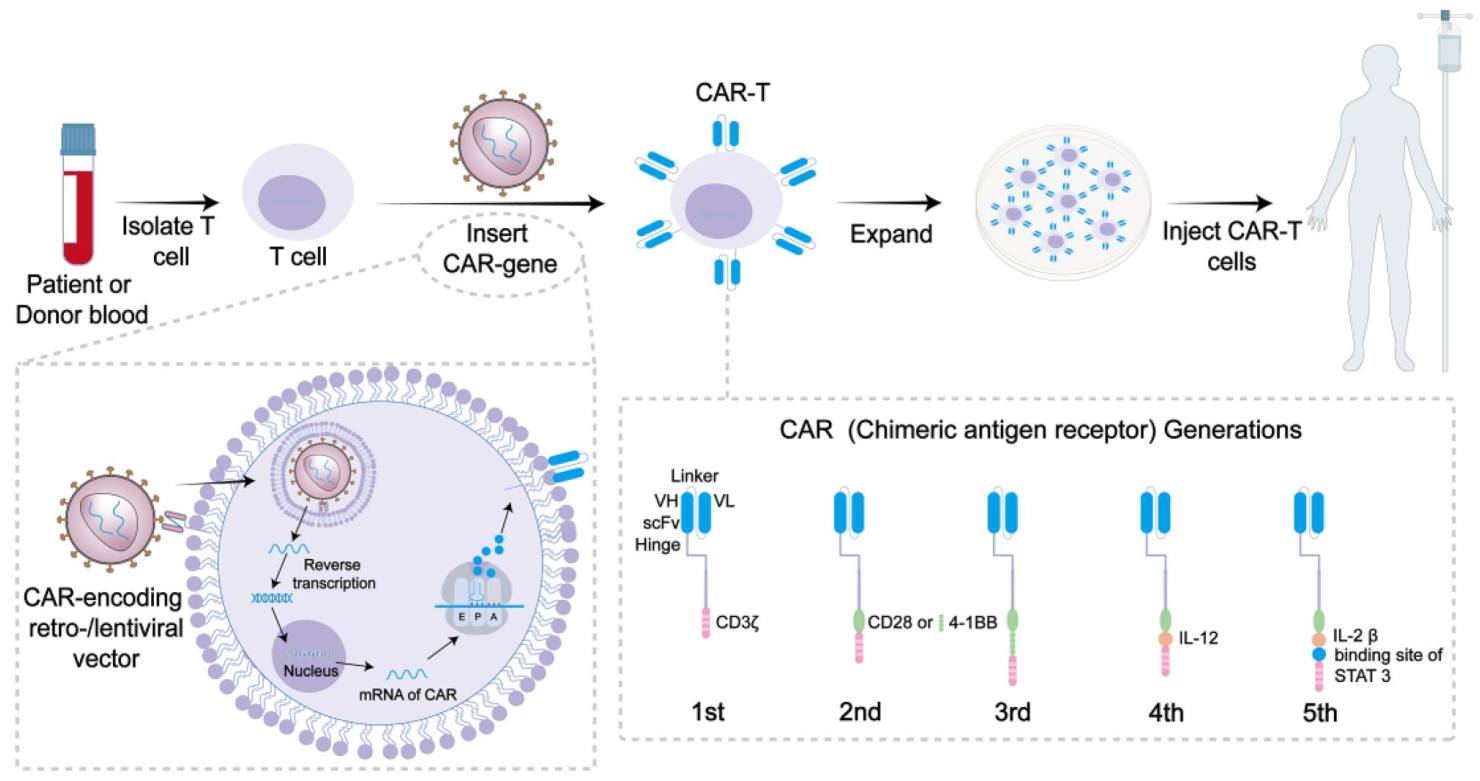
Quy trình thực hiện liệu pháp tế bào CAR-T thường bao gồm các bước chính: (1) thu thập tế bào T từ máu của chính bệnh nhân, (2) chuyển gen mã hóa thụ thể kháng nguyên khảm (CAR) để tế bào T có thể sản xuất cấu trúc CAR trên bề mặt của nó, cấu trúc này cho phép tế bào T nhận diện các protein đặc hiệu trên tế bào ung thư, (3) nuôi cấy tăng sinh tế bào CAR-T để nhân lên đủ số lượng cần thiết, (4) điều trị điều kiện hóa bệnh nhân bằng hóa/xạ trị để giảm số lượng tế bào T hiện có, tạo chỗ trống và chuẩn bị cho hệ miễn dịch tiếp nhận tế bào CAR-T, (5) truyền sản phẩm CAR-T cho bệnh nhân, các tế bào này đi khắp cơ thể và tìm những tế bào ác tính biểu hiện kháng nguyên mà CAR nhận diện để tiêu diệt chúng, (6) theo dõi bệnh nhân sau điều trị để đánh giá, kiểm soát tính an toàn và hiệu quả của liệu pháp.
Trong quy trình trên, giai đoạn thiết kế gen mã hóa CAR và chuyển gen này vào tế bào T đóng vai trò chìa khóa. Các nhà khoa học cần xác định dấu hiệu (kháng nguyên) đặc hiệu trên tế bào ung thư (ví dụ CD19 đối với bệnh bạch cầu/u lympho, hay BCMA đối với tế bào đa u tủy xương), sau đó thiết kế cấu trúc CAR nhận diện được kháng nguyên này. Đoạn ADN mã hóa cấu trúc đó được đưa vào tế bào T của bệnh nhân, thường bằng vector virus, là công cụ chuyển gen dựa trên cơ chế xâm nhập vào tế bào của một số loại virus. Vì các vector virus chèn ADN ngẫu nhiên chứ không nhắm trúng đích vào một vùng xác định của bộ gen, nên về lý thuyết sẽ có nguy cơ việc chèn ngẫu nhiên đó có thể phá vỡ các gen kiềm chế khối u chính, dẫn đến bệnh nhân mắc loại ung thư khác sau khi sử dụng liệu pháp CAR-T.
Những nghi vấn này càng trở nên đáng lo ngại khi đầu năm 2024, Verdun và cộng sự công bố: tính đến 31/12/2023, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (US-FDA) đã ghi nhận 22 trường hợp phát hiện các tế bào T ác tính ở những bệnh nhân trước đây được điều trị bằng tế bào T biến đổi gen, dường như đây là tác dụng phụ hiếm gặp do chính liệu pháp CAR-T gây nên. FDA khi phê duyệt các liệu pháp CAR-T đều áp dụng các chiến lược đánh giá và giảm thiểu rủi ro (Risk Evaluation and Mitigation Strategies – REMS), mặc dù chính sách này mới được gỡ bỏ cuối tháng 06/2025, nhưng FDA tiếp tục yêu cầu các nhà sản xuất tiến hành các nghiên cứu quan sát đánh giá độ an toàn trong quá trình sử dụng (bao gồm cả nguy cơ mắc ung thư thứ phát) với việc theo dõi bệnh nhân trong 15 năm sau khi điều trị.
3. Nghiên cứu hồi cứu chứng minh CAR-T không liên quan đến ung thư thứ phát
Để đánh giá những rủi ro này, một nhóm nghiên cứu Hoa Kỳ đã phân tích dữ liệu từ 783 bệnh nhân trong 38 thử nghiệm lâm sàng khác nhau sử dụng liệu pháp tế bào T diễn ra từ nă 2001 đến 2023. Theo kết quả đánh giá với thời gian theo dõi trung bình 1,56 năm, họ chỉ xác định được 1 trường hợp có tế bào T ác tính – một tỷ lệ rất hiếm. Điều quan trọng là khi giải trình tự ADN từ u lympho tế bào T này, chúng không chứa trình tự gen được sử dụng trong liệu pháp CAR-T, cho thấy đó không phải là nguyên nhân gây nên tình trạng ung thư thứ phát đó.
Theo nhóm nghiên cứu, nguyên nhân gây nên ung thư thứ phát khả năng cao nhất đến từ các liệu pháp hóa trị gây độc tế bào, gây tổn thương ADN. Những bệnh nhân sau khi trải qua các đợt hóa trị và được sử dụng liệu pháp CAR-T một cách hiệu quả, các tế bào ung thư bị tiêu diệt, tình trạng bệnh được cải thiện, tuy nhiên những tế bào T mang tổn thương ADN trong cơ thể bệnh nhân không được loại bỏ, khiến họ có khả năng bị ung thư tế bào T thứ phát trong những năm tiếp theo.
Trong 783 bệnh nhân được hồi cứu, 176 bệnh nhân vẫn còn mẫu máu lưu trữ trong quá trình thử nghiệm lâm sàng. Nhóm nghiên cứu đã giải trình tự ADN từ những mẫu này, kết quả cho thấy trong một số tế bào (đặc biệt là những tế bào tồn tại trong máu vài tháng sau điều trị) có phát hiện vị trí tích hợp nằm trong hoặc gần các gen liên quan đến ung thư, tuy nhiên ngay cả khi đó các tế bào không có dấu hiệu ác tính. Để những tế bào này trở thành tế bào ung thư cần có nhiều sự kiện phức tạp, rất khó để một sự kiện chuyển gen bằng vector virus có thể biến một tế bào T bình thường thành tế bào T ác tính.
Kết quả phân tích này đặc biệt quan trọng, giúp đẩy lùi những lo ngại về nguy cơ ung thư thứ phát xảy ra do liệu pháp CAR-T, đặc biệt khi hiện tại các nhà khoa học đang mở rộng thử nghiệm CAR-T trong nhiều bệnh lý khác, bao gồm cả các bệnh ung thư u đặc và các bệnh tự miễn. Đồng thời, những chiến lược chuyển gen an toàn hơn trong quá trình sản xuất CAR-T cũng đang được nghiên cứu rộng rãi trong thời gian gần đây.
TÀI LIỆU THAM KHẢO
1. Jadlowsky J. K., et al. (2025). Long-term safety of lentiviral or gammaretroviral gene-modified T cell therapies. Nature Medicine, 31(4), 1134-1144. DOI https://doi.org/10.1038/s41591-024-03478-6
2. Verdun N., and Marks P. (2024). Secondary cancers after chimeric antigen receptor T-cell therapy. New England Journal of Medicine, 390(7), 584-586. DOI https://doi.org/10.1056/NEJMp2400209
3. Xiao K., et al. (2024). mRNA‐based chimeric antigen receptor T cell therapy: Basic principles, recent advances and future directions. Interdisciplinary Medicine, 2(1), e20230036. DOI https://doi.org/10.1002/INMD.20230036
XEM THÊM
- Cải biến di truyền giúp tăng cường hiệu quả liệu pháp tế bào miễn dịch trong điều trị ung thư: TCR-T và CAR-T https://www.facebook.com/share/p/18mRyiUvJb/
- Liệu pháp CAR-T – bước đột phá của liệu pháp tế bào trong điều trị ung thư https://www.facebook.com/share/p/1ACHF2K2wY/
- FDA loại bỏ các chiến lược đánh giá và giảm thiểu rủi ro cho liệu pháp CAR-T tự thân trong điều trị ung thư https://www.facebook.com/share/p/171ZGTP5uq/
- CAR-T in vivo: chiến lược mới với tế bào CAR-T được sản xuất ngay trong cơ thể bệnh nhân https://www.facebook.com/share/p/19Yrq5KFJ2/
- CAR-E: Giải pháp tăng cường hiệu quả và tạo trí nhớ miễn dịch cho liệu pháp CAR-T, giúp ngăn ngừa khả năng tái phát ung thư sau điều trị bằng phương pháp này https://www.facebook.com/share/p/1BJvL3gP4L/