Một số giải pháp giảm chi phí cho liệu pháp CAR-T
Liệu pháp CAR-T được coi là bước đột phá của liệu pháp tế bào trong điều trị ung thư, mang đến giải pháp điều trị hiệu quả cho một số bệnh ung thư máu, ngoài ra cũng có những tiến bộ tích cực đối với u đặc và các bệnh tự miễn. Tính đến thời điểm hiện tại, đã có 7 sản phẩm được Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (The U. S. Food And Drug Administration – US FDA) và Cơ quan Dược phẩm Châu Âu (European Medicines Agency – EMA) phê duyệt, bao gồm Kymriah, Yescarta, Tecartus, Breyanzi, Aucatzyl, Abecma, Carvykti. Ngoài ra, một số sản phẩm khác được cấp phép ở Trung Quốc (Relma-cel, Yuanruida, Fucaso, Zevor-cell), Ấn Độ (NexCAR19, Qartemi),… đều thuộc các công ty ở quốc gia sở tại. Tuy nhiên, chi phí của phương pháp điều trị này khá cao, chỉ riêng quy trình điều chế CAR-T tại Hoa Kỳ đã tiêu tốn khoảng 300.000 USD trở lên và tăng theo từng năm theo giá nguyên liệu, nếu tính thêm các chi phí khác trong suốt quá trình nằm viện và theo dõi bệnh nhân thì sức ép kinh tế trở nên rất nặng nề.
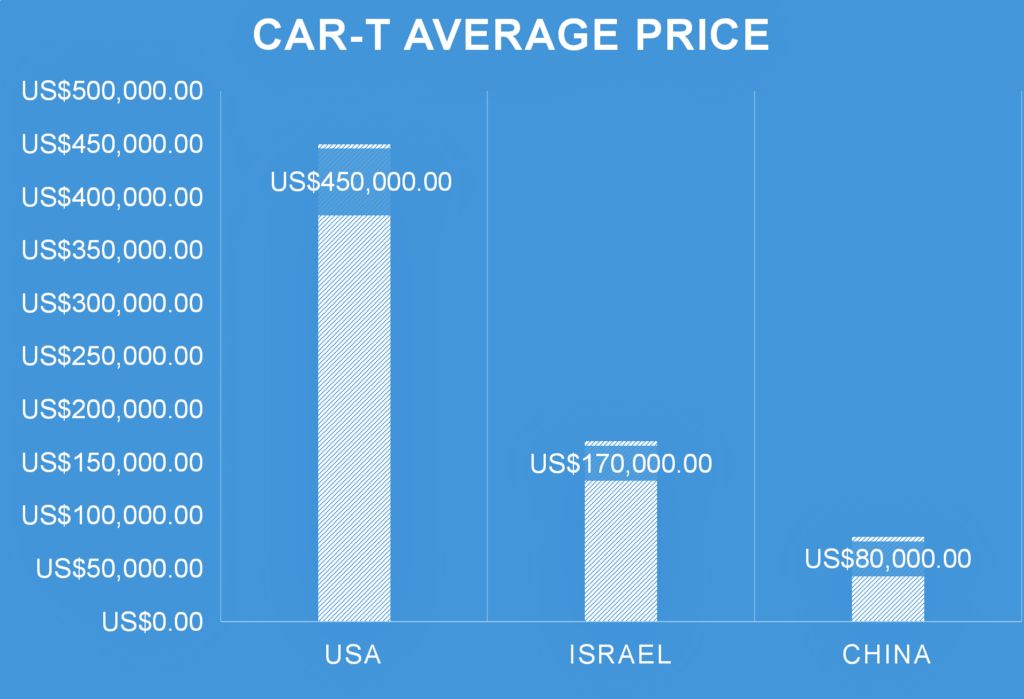
Để giải quyết vấn đề này, nhiều chiến lược đã được đề ra, sau đây là một số giải pháp chính.
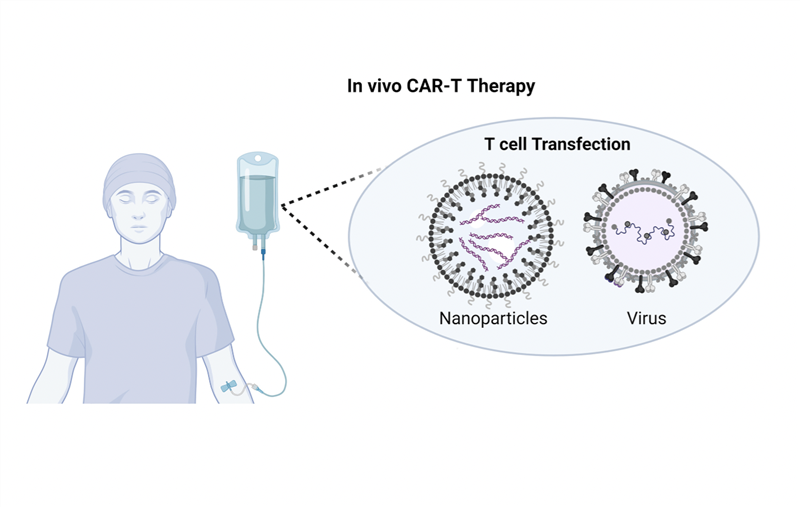
1. Phát triển liệu pháp CAR-T in vivo
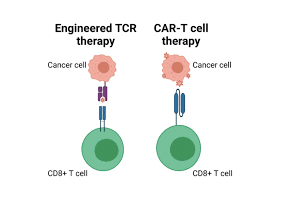
Quy trình CAR-T thông thường (ex vivo) được thực hiện qua nhiều bước phức tạp: thu thập tế bào T từ bệnh nhân, biến đổi gen của chúng để biểu hiện cấu trúc CAR, nuôi cấy tăng sinh tế bào CAR-T, kiểm tra chất lượng và truyền sản phẩm trở lại bệnh nhân. Tổng thời gian thường mất 2–4 tuần, đòi hỏi những yêu cầu đặc biệt về cơ sở vật chất và trang thiết bị, dẫn đến chi phí khá lớn.
Đối với CAR-T in vivo, các tế bào CAR-T được tạo ra trực tiếp trong cơ thể bệnh nhân, bằng cách đưa vào trong người bệnh các hạt nano hoặc vector virus nhắm trúng đích tế bào T, chúng sẽ chuyển gen và biểu hiện cấu trúc CAR, tạo nên tế bào CAR-T có thể nhân lên tự nhiên trong cơ thể. Phương pháp này có thể làm giảm chi phí và độ phức tạp so với CAR-T ex vivo, đồng thời có những ưu thế tiềm năng như tránh nguy cơ nhiễm trùng cơ hội và độc tính toàn thân cho người bệnh.
2. Phát triển các liệu pháp CAR-T đồng loại
Tất cả các liệu pháp CAR-T được phê duyệt hiện tại đều là tự thân (nghĩa là tế bào T được lấy từ bệnh nhân để sau đó điều trị cho chính họ), đa số các sản phẩm thử nghiệm cũng đều như vậy. Vì thế, mỗi lô sản xuất CAR-T mang một đặc điểm riêng được cá nhân hóa cho từng bệnh nhân, và chỉ sử dụng được cho chính người bệnh đó, làm tăng chi phí sản xuất.
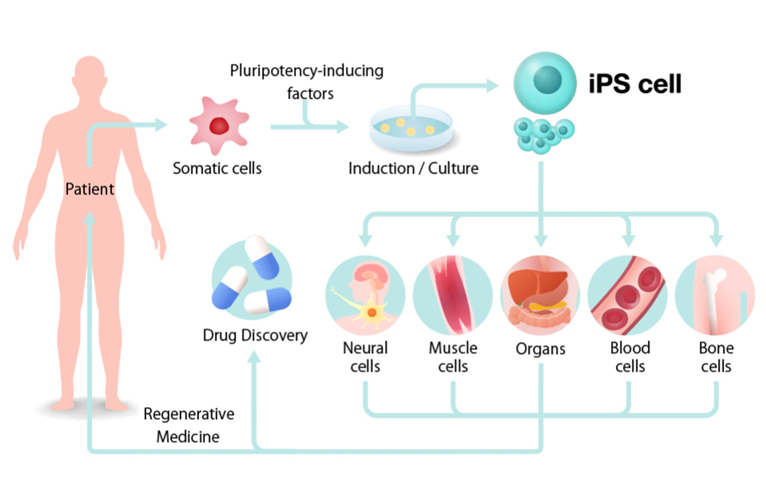
Các nhà khoa học đã và đang thực hiện những chiến lược để sản xuất CAR-T đồng loại (“off-the-shelf” allogeneic CAR-T), trong đó tế bào T được lấy từ người hiến khỏe mạnh, hoặc từ máu cuống rốn, hoặc được biệt hóa từ tế bào gốc, sau đó cải biến và nuôi cấy tăng sinh và lưu trữ đông lạnh, sẵn sàng truyền cho bệnh nhân khi cần. Quá trình sản xuất hàng loạt với số lượng lớn giúp giảm chi phí đáng kể, đồng thời mang đến những lợi thế khác như chất lượng đồng nhất, sẵn sàng sử dụng ngay cho bệnh nhân khi có chỉ định mà không cần chờ đợi quá trình cải biến trong phòng thí nghiệm.
3. Sản xuất CAR-T tại các quốc gia có chi phí thấp
Trong các sản phẩm CAR-T được cấp phép trên thế giới, 7 sản phẩm được phê duyệt tại Hoa Kỳ và Châu Âu có chi phí khá cao, ngược lại những sản phẩm tại Ấn Độ và Trung Quốc ở mức giá được coi là thấp hơn nhiều. Ví dụ, Relma-cel khoảng 1 triệu Nhân dân tệ (khoảng 140.000 USD), Zevor-cel khoảng 160.000 USD, NexCAR19 khoảng 50.000 USD. Mức chi phí thấp do nhiều nguyên nhân, bao gồm chi phí xây dựng cơ sở sản xuất, trang thiết bị, nguyên liệu, và đặc biệt là chi phí nhân công cũng như công nghệ tạo vector chuyển gen của từng công ty.
4. Chuyển giao công nghệ và sản xuất tại chỗ
Đây là giải pháp đầy hứa hẹn, cho phép các bệnh viện có thể sản xuất liệu pháp CAR-T tại chỗ để sử dụng cho bệnh nhân, tránh việc phải vận chuyển mẫu đến phòng thí nghiệm sản xuất, hoặc vận chuyển bệnh nhân đến cơ sở y tế thuận tiện (thường các phòng thí nghiệm hoặc cơ sở y tế này ở nước ngoài) làm tăng chi phí cho quá trình điều trị. Ví dụ, hãng Miltenyi Biotec có trụ sở tại Đức đã triển khai nhà máy và chuyển giao công nghệ (gồm hệ thống sản xuất CAR-T là CliniMACS Prodigy và hệ thống vector chuyển gen) đến nhiều quốc gia như Áo, Anh, Ireland, Hàn Quốc, Ấn Độ,… (tại Việt Nam, Hệ thống Y tế Vinmec cũng tiếp nhận chuyển giao công nghệ này).
Về lâu dài, việc sản xuất tại chỗ sẽ giúp giảm đáng kể chi phí sản xuất CAR-T, khi lượng bệnh nhân đủ lớn. Tuy nhiên ở thời điểm ban đầu, chiến lược này còn gặp nhiều thách thức, bao gồm quy định triển khai liệu pháp ở quốc gia sở tại, thử nghiệm đánh giá hiệu quả trên bệnh nhân của từng công nghệ/giải pháp (ngược lại với các sản phẩm CAR-T thương mại đã có dữ liệu lâm sàng đủ tin cậy trước khi được cấp phép), chi phí nguyên liệu và nhân công tại quốc gia sở tại,…
5. Một số giải pháp khác
Một số giải pháp chuyên sâu khác vẫn đang được các nhà khoa học nghiên cứu, bao gồm cải tiến quy trình (tìm vector thay thế vector virus, tăng hiệu suất để giảm thời gian nuôi cấy tế bào), chuyên môn hóa quá trình sản xuất đến nhiều công ty thay vì tập trung như hiện tại, tìm các dấu ấn sinh học để nâng cao hiệu quả của CAR-T,…