FDA loại bỏ các chiến lược đánh giá và giảm thiểu rủi ro cho liệu pháp CAR-T tự thân trong điều trị ung thư
Ngày 27 tháng 6 năm 2025, Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (The U.S. Food and Drug Administration – US FDA) đã ra thông báo chính thức xác định: tính an toàn và hiệu quả của các liệu pháp CAR-T tự thân đã được chấp thuận có thể được đảm bảo mà không cần các chiến lược đánh giá và giảm thiểu rủi ro (Risk Evaluation and Mitigation Strategies – REMS).
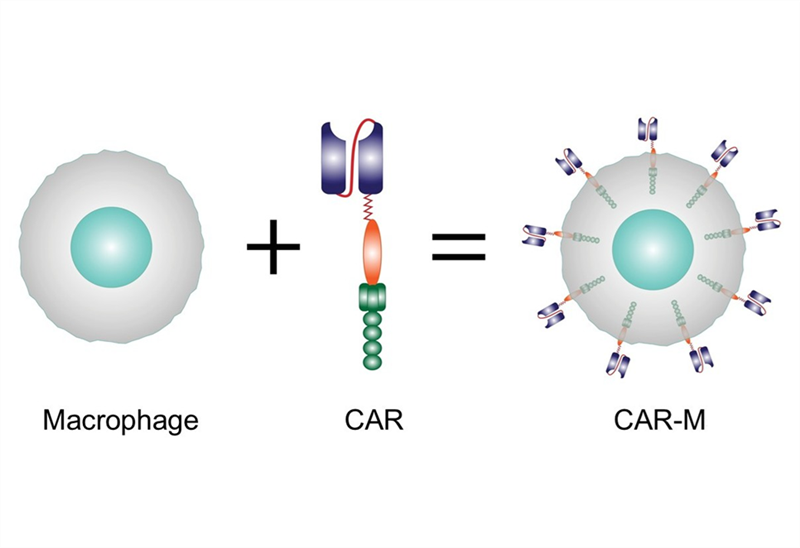
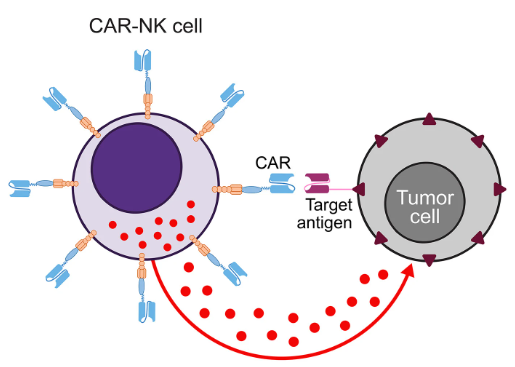
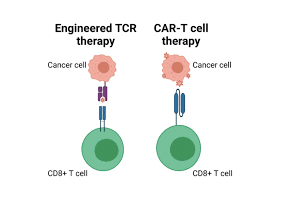
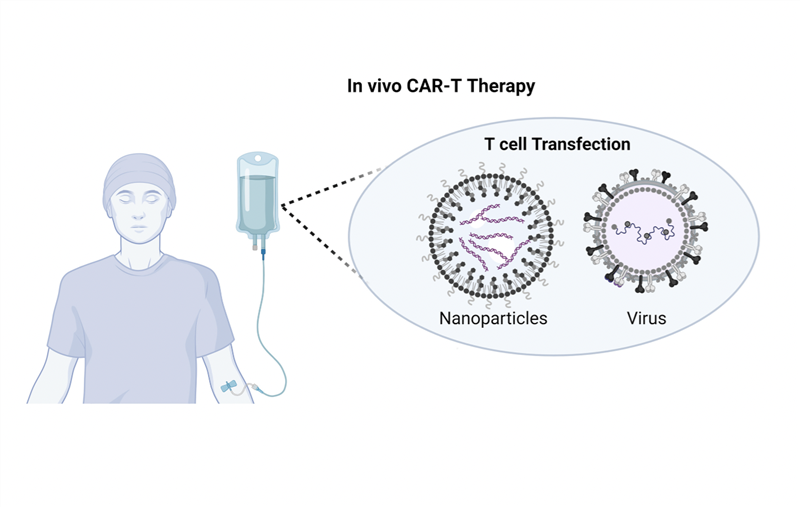
Liệu pháp CAR-T sử dụng các tế bào T mang thụ thể kháng nguyên khảm (Chimeric Antigen Receptor – CAR) được thiết kế nhân tạo để phát hiện đặc hiệu và tiêu diệt các tế bào ung thư. Liệu pháp CAR-T đã đạt nhiều thành tựu trong điều trị các bệnh lý huyết học ác tính, ngoài ra cũng cho thấy những tín hiệu lạc quan với ung thư u đặc, các bệnh tự miễn. Mặc dù vậy, liệu pháp này cũng có những rủi ro đáng kể cho bệnh nhân, bao gồm hội chứng giải phóng cytokine, hội chứng độc tính thần kinh liên quan đến tế bào miễn dịch, nhiễm trùng, nguy cơ mắc ung thư thứ phát,…
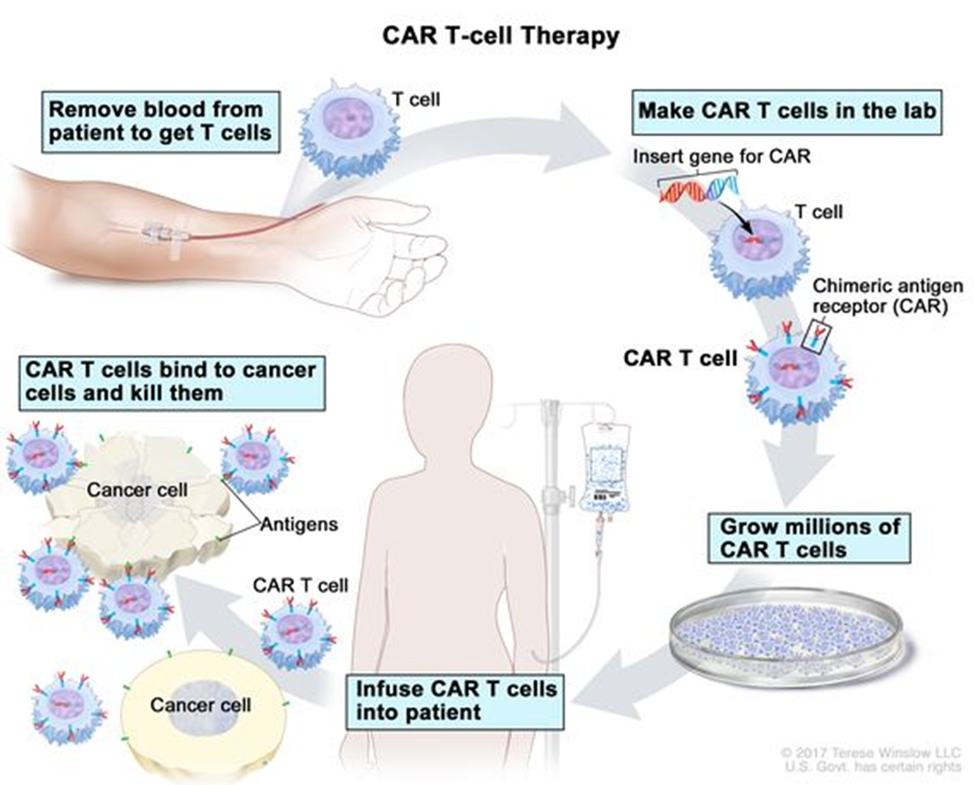
REMS là chương trình an toàn mà FDA có thể yêu cầu đối với một số loại thuốc có vấn đề nghiêm trọng về độ an toàn, giúp đảm bảo lợi ích của thuốc lớn hơn rủi ro. FDA quyết định rằng REMS không còn cần thiết và cần bị loại bỏ khỏi các sản phẩm CAR-T tự thân sau (đã được FDA cấp phép trong điều trị các bệnh huyết học ác tính):
- Abecma (idecabtagene vicleucel)
- Breyanzi (lisocabtagene maraleucel)
- Carvykti (ciltacabtagene autoleucel)
- Kymriah (tisagenlecleucel)
- Tecartus (brexucabtagene autoleucel)
- Yescarta (axicabtagene ciloleucel)
Việc loại bỏ REMS với các sản phẩm trên đồng nghĩa với việc tháo gỡ các yêu cầu những bệnh viện/phòng khám sử dụng chúng phải được chứng nhận đặc biệt và có sẵn thuốc tocilizumab (kháng thể đơn dòng điều trị một số bệnh viêm và tự miễn). Thông tin về các rủi ro được thể hiện đầy đủ trên nhãn sản phẩm, bao gồm hội chứng giải phóng cytokine và độc tính thần kinh. Các bác sỹ và các tổ chức hiện có nhiều kinh nghiệm hơn trong kiểm soát độc tính của những sản phẩm CAR-T đã được chấp thuận. Việc loại bỏ REMS giúp đẩy nhanh việc cung cấp liệu pháp cho người bệnh và giảm gánh nặng cho các nhà cung cấp.
Các sản phẩm vẫn phải tuân theo quy định về giám sát an toàn, thông qua các yêu cầu báo cáo tác dụng phụ theo quy định. FDA tiếp tục yêu cầu các nhà sản xuất tiến hành các nghiên cứu quan sát đánh giá độ an toàn trong quá trình sử dụng (bao gồm cả nguy cơ mắc ung thư thứ phát) với việc theo dõi bệnh nhân trong 15 năm sau khi sử dụng, và cam kết thông báo cho công chúng khi có thông tin mới về tác dụng phụ nghiêm trọng của các sản phẩm này.
TÀI LIỆU THAM KHẢO
Thông cáo báo chí của FDA ngày 27 tháng 06 năm 2025 về việc loại bỏ các chiến lược đánh giá và giảm thiểu rủi ro (REMS) cho liệu pháp miễn dịch tế bào CAR-T tự thân https://www.fda.gov/news-events/press-announcements/fda-eliminates-risk-evaluation-and-mitigation-strategies-rems-autologous-chimeric-antigen-receptor