Liệu pháp CAR-T đồng loại cho thấy tính an toàn và hiệu quả trong điều trị ung thư huyết học
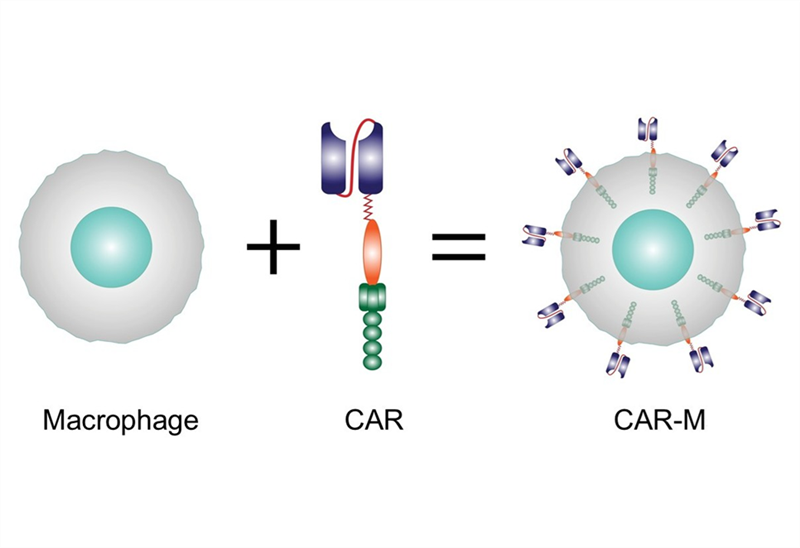
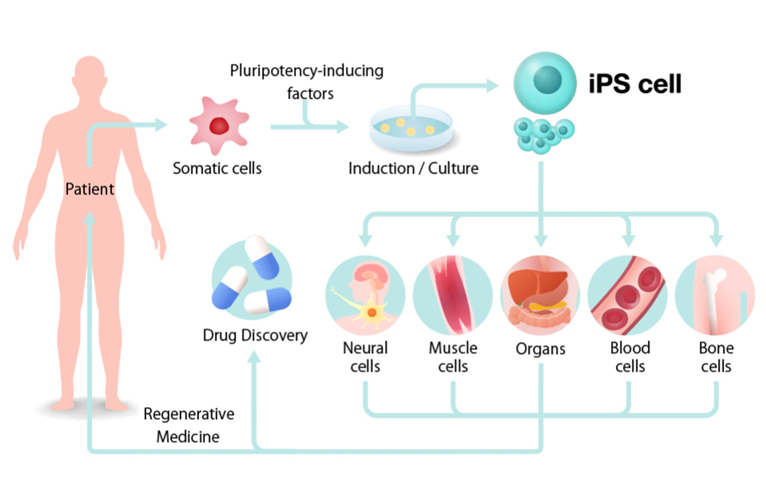
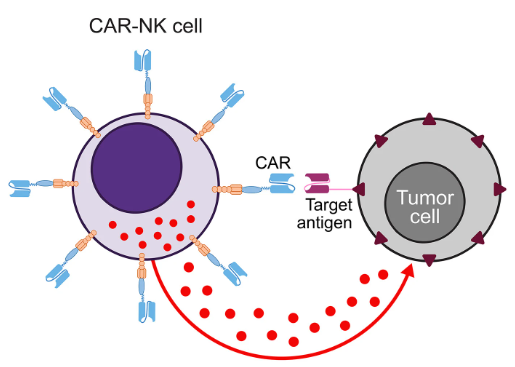
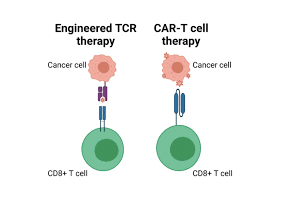
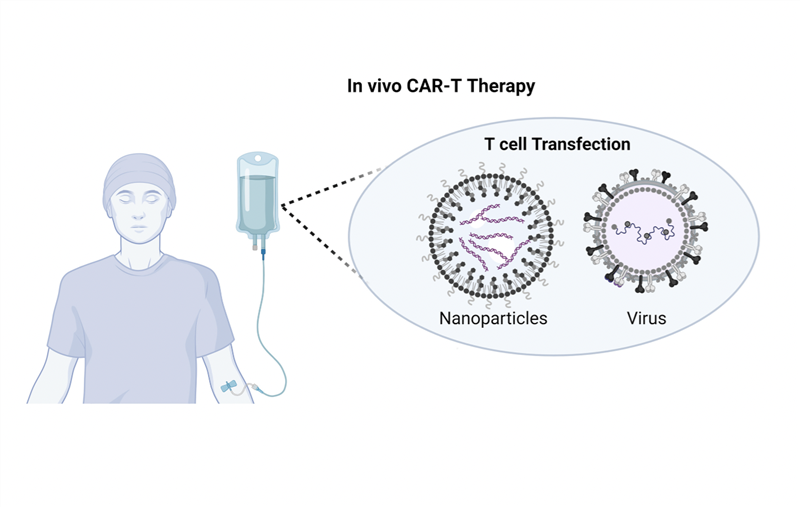
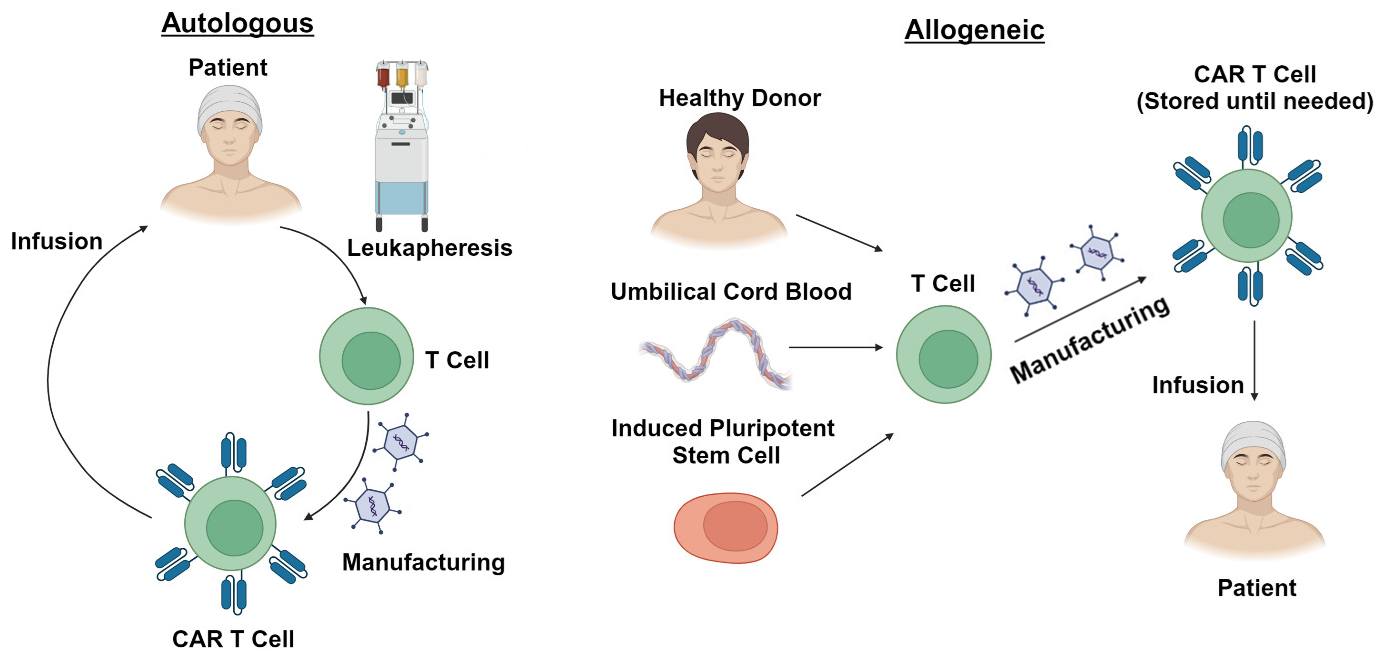
Liệu pháp tế bào T mang thụ thể kháng nguyên khảm (chimeric antigen receptor T-cell, CAR-T) đã khẳng định được hiệu quả trong điều trị các bệnh lý huyết học ác tính, với 7 sản phẩm CAR-T tự thân được cấp phép tại Hoa Kỳ và Châu Âu để điều trị y lympho, bệnh bạch cầu, đa u tủy xương. Quy trình liệu pháp CAR-T tự thân thường bao gồm các bước chính: thu thập tế bào T từ máu của chính bệnh nhân và chuyển gen để biểu hiện cấu trúc CAR trên tế bào T, nuôi cấy tăng sinh tế bào CAR-T thu được và truyền cho bệnh nhân. Ngoài ra, các nhà khoa học đã và đang thực hiện các chiến lược để sản xuất sản phẩm đồng loại (“off-the-shelf” allogeneic CAR-T), với nhiều lợi thế như sản xuất đồng loạt giúp giảm chi phí, chất lượng đồng nhất, không cần chờ đợi quá trình cải biến và nuôi cấy tăng sinh như phương pháp tự thân,... Không giống như phương pháp truyền thống, những tế bào T trong sản phẩm đồng loại được thu nhận từ người hiến khỏe mạnh, hoặc máu cuống rốn, hoặc biệt hóa từ tế bào gốc đa tiềm năng, sau đó cải biến để biểu hiện cấu trúc CAR trên bề mặt tế bào, nuôi cấy tăng sinh CAR-T và lưu trữ đông lạnh, sẵn sàng truyền cho bệnh nhân khi cần.
Ngày 03 tháng 11 năm 2025, Công ty Công nghệ sinh học Caribou Biosciences đã công bố những dữ liệu lâm sàng về hai sản phẩm CAR-T đồng loại đang được họ phát triển: Vispa-cel trong điều trị u lympho không Hodgkin tế bào B tái phát hoặc kháng trị (thử nghiệm lâm sàng ANTLER), và CB-011 trong điều trị đa u tủy xương (thử nghiệm lâm sàng CaMMouflage).
Vispacabtagene regedleucel (Vispa-cel, trước đây là CB-010), là sản phẩm CAR-T đồng loại kháng CD19, đồng thời chỉnh sửa PD-1 là một điểm kiểm soát miễn dịch nhằm hạn chế sự suy giảm sớm của những tế bào này tỏng cơ thể. Vispa-cel được sử dụng trong thử nghiệm lâm sàng giai đoạn 1 có tên ANTLER để điều trị u lympho không Hodgkin tế bào B tái phát hoặc kháng trị. Theo kết quả thử nghiệm, Vispa-cel có độ bền tương tự CAR-T tự thân, khả năng dung nạp tốt và chứng minh được hiệu quả đáng khích lệ: ở nhóm phù hợp HLA một phần (n = 22), tỷ lệ đáp ứng tổng thể (Overall response rate – ORR) đạt 82%, tỷ lệ đáp ứng hoàn toàn (Complete Response – CR) đạt 64%, tỷ lệ sống không bệnh tiến triển (Progression-free survival – PFS) sau 12 tháng đạt 51%; ở nhóm được tối ưu hóa (n = 35), các tỷ lệ này tương ứng là 86%, 63% và 53%. Tính an toàn của liệu pháp cũng được khẳng định, với các tác dụng phụ không nghiêm trọng, và không có trường hợp nào mắc bệnh ghép chống chủ (GvHD).
CB-011 là sản phẩm đồng loại kháng BCMA trong điều trị đa u tủy xương, được đánh giá an toàn và hiệu quả thông qua thử nghiệm lâm sàng giai đoạn 1 có tên CaMMouflage (NCT05722418). Trong thử nghiệm này, nhóm nghiên cứu đã quan sát được những phản ứng sâu sắc và lâu dài ở nhóm bệnh nhân được điều trị. Tỷ lệ đáp ứng tổng thể đạt 92%, với 75% đáp ứng hoàn toàn và 83% đáp ứng ít nhất một phần hoặc giảm ung thư. Hầu hết các bệnh nhân (91%) đều âm tính với bệnh tồn dư tối thiểu (số lượng rất nhỏ các tế bào ung thư còn lại trong cơ thể sau khi điều trị), ngoài ra ít gặp các tác dụng phụ khác.
Những kết quả này đánh dấu một bước tiến đáng khích lệ trong liệu pháp tế bào miễn dịch chống ung thư. Các đặc tính sinh học của Vispa-cell và CB-011 tương đương với CAR-T tự thân, đồng thời tính sẵn có và khả năng dung nạp tốt khiến nó phù hợp để sử dụng ngoại trú tại các trung tâm y tế lớn và các bệnh viện cộng đồng, mở rộng đáng kể khả năng tiếp cận với bệnh nhân. Những yếu tố chính liên quan đến kết quả thành công của bệnh nhân bao gồm tuổi của người hiến tặng (người hiến tặng trẻ có kết quả tốt hơn so với người lớn tuổi) và sự phù hợp HLA một phần (sự phù hợp của hai hay nhiều alen tương quan với kết quả tương đương đương với CAR-T tự thân). Công ty Caribou Biosciences tin rằng những sản phẩm này sẽ trở thành liệu pháp tế bào CAR-T đồng loại tiềm năng tốt nhất cho bệnh nhân, đồng thời sẽ tiến hành các thử nghiệm lâm sàng giai đoạn sau để đánh giá kỹ hơn về hiệu quả của chúng.
TÀI LIỆU THAM KHẢO
1. Thông cáo báo chí ngày 02 tháng 11 năm 2025 của Caribou Biosciences, Inc. https://www.globenewswire.com/news-release/2025/11/02/3178810/0/en/Caribou-Biosciences-to-Host-Webcast-to-Report-New-Data-Updates-from-Two-Allogeneic-CAR-T-Cell-Therapy-Programs-in-Lymphoma-and-Multiple-Myeloma.html
2. Thông tin dữ liệu nghiên cứu của thử nghiệm ANTLER trên Mạng lưới Tin tức Đầu tư https://investingnews.com/caribou-biosciences-announces-positive-data-from-antler-phase-1-trial-demonstrating-efficacy-and-durability-of-vispa-cel-an-allogeneic-car-t-cell-therapy-on-par-with-autologous-car-t-cell-therapies/
3. Thông tin về thử nghiệm lâm sàng NCT05722418 trên trang cơ sở dữ liệu các nghiên cứu lâm sàng của Thư Viện Y khoa Quốc gia Hoa Kỳ https://clinicaltrials.gov/study/NCT05722418
XEM THÊM
- Cải biến di truyền giúp tăng cường hiệu quả liệu pháp tế bào miễn dịch trong điều trị ung thư: TCR-T và CAR-T https://www.facebook.com/share/p/18mRyiUvJb/
- Liệu pháp CAR-T – bước đột phá của liệu pháp tế bào trong điều trị ung thư https://www.facebook.com/share/p/1ACHF2K2wY/
- CAR-E: Giải pháp tăng cường hiệu quả và tạo trí nhớ miễn dịch cho liệu pháp CAR-T, giúp ngăn ngừa khả năng tái phát ung thư sau điều trị bằng phương pháp này https://www.facebook.com/share/p/1BJvL3gP4L/
- CAR-T in vivo: chiến lược mới với tế bào CAR-T được sản xuất ngay trong cơ thể bệnh nhân https://www.facebook.com/share/p/19Yrq5KFJ2/