Cải biến di truyền giúp tăng cường hiệu quả liệu pháp tế bào miễn dịch trong điều trị ung thư: TCR-T và CAR-T
1. Liệu pháp miễn dịch tế bào T
Các liệu pháp miễn dịch tế bào T khác nhau tùy thuộc vào nguồn gốc tế bào, cách thức xử lý ngoài cơ thể và phương thức tế bào T nhận diện mục tiêu khi được truyền cho bệnh nhân. Các chiến lược khai thác liệu pháp miễn dịch tế bào T bao gồm:
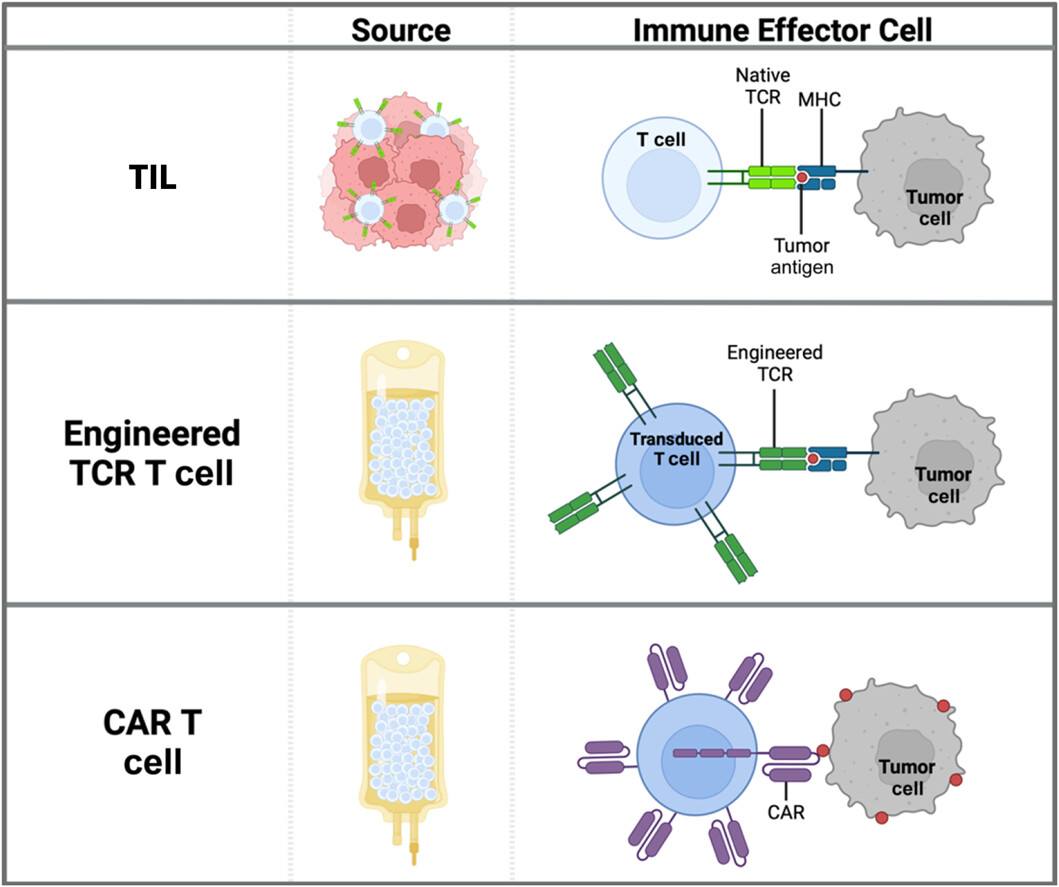
- Liệu pháp tế bào lympho thâm nhiễm khối u (Tumor-Infiltrating Lymphocyte, TIL): sử dụng các tế bào T trong khối u, với thụ thể tế bào T tự nhiên nhận diện các mục tiêu trên tế bào ung thư (xem bài viết về liệu pháp TIL tại https://ysinhtebao.com/lieu-phap-tb-mien-dich-khac/lieu-phap-til-trong-dieu-tri-u-dac-trien-vong-va-thach-thuc).
- Liệu pháp thụ thể tế bào T (T Cell Receptor-Engineered T Cell, TCR-T): Sử dụng các kỹ thuật di truyền để thiết kế các thụ thể tế bào T, bổ sung cho tế bào T giúp chúng nhận diện mục tiêu trên tế bào ung thư.
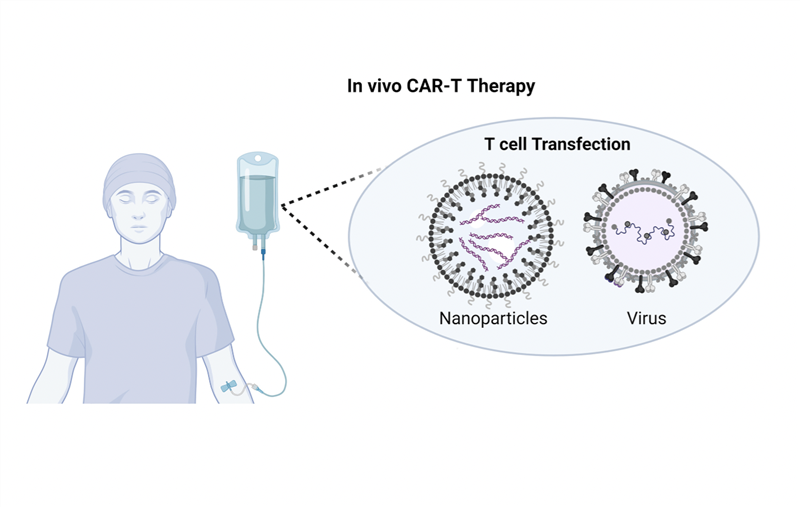
- Liệu pháp tế bào T với thụ thể kháng nguyên khảm (Chimeric Antigen Receptor T cell, CAR-T): sử dụng kỹ thuật di truyền để tạo ra các thụ thể nhân tạo, cung cấp cho tế bào T giúp chúng phát hiện các mục tiêu trên tế bào ung thư mà thụ thể tự nhiên không nhận diện được.
2. Liệu pháp TCR-T: biến đổi di truyền thụ thể tế bào T
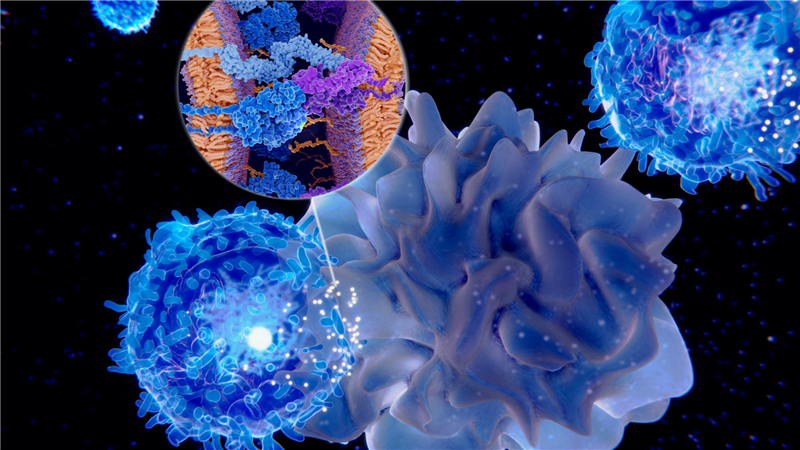
Nhờ thụ thể tế bào T (T Cell Receptor – TCR), tế bào T có khả năng nhận biết tự nhiên đối với các mục tiêu như vi khuẩn, virus, tế bào ung thư,... và tiêu diệt chúng. Đối với liệu pháp TCR-T, các nhà nghiên cứu ung thư đã xác định một dấu hiệu trên các tế bào ung thư, thiết kế một TCR nhận dạng được dấu hiệu đó, sau đó tách tế bào T từ bệnh nhân và thêm vào đó gen mã hóa TCR đã thiết kế để tạo nên TCR-T phát hiện tốt các tế bào ung thư.
Liệu pháp TCR-T đã được thử nghiệm lâm sàng để điều trị nhiều loại ung thư khác nhau, trong đó thu được những tín hiệu tích cực đối với u đặc. Tháng 08/2024, Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (US FDA) đã chấp thuận sản phẩm TECELRA (Afamitresgene autoleucel), là sản phẩm TCR-T tự thân hướng đến kháng nguyên A4 liên quan đến ung thư hắc tố (MAGE-A4) dùng trong điều trị sarcoma hoạt dịch. Các chiến lược hiện nay về TCR-T đang hướng đến khắc phục những nhược điểm khiến bệnh nhận hưởng những lợi ích hạn chế lâm sàng, bao gồm giảm độc tính trên bệnh nhân, tăng cường các dấu hiệu nhận diện khối u – đặc biệt là các tân kháng nguyên – để cải thiện hiệu quả và ngăn ngừa tổn thương cho các tế bào và mô khỏe mạnh.
3. Liệu pháp CAR-T: thụ thể nhân tạo nhận diện tế bào ung thư
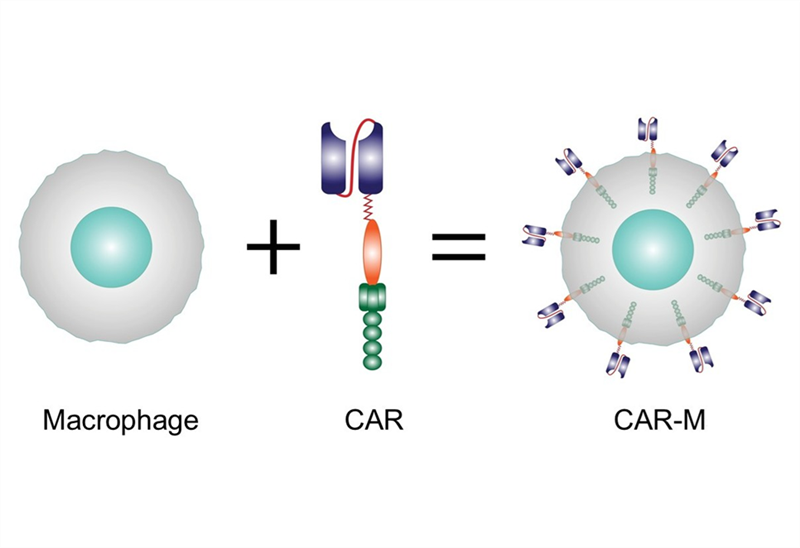
CAR-T là liệu pháp tế bào miễn dịch trong đó tế bào T được biến đối với một thụ thể nhân tạo, được gọi là thụ thể kháng nguyên khảm (Chimeric Antigen Receptor – CAR), để nhận diện tế bào ung thư. Tế bào T tự nhiên có TCR cho phép chúng phát hiện nhiều phân tử mà chúng xác định là tế bào ung thư, nhưng không phải tất cả các kháng nguyên, do đó các nhà nghiên cứu thiết kế nên CAR để phát hiện những thụ thể bề mặt mà TCR không nhận diện được.
Liệu pháp CAR-T đã chứng minh hiệu quả trong điều trị các bệnh lý ác tính huyết học. Hiện tại đã có 7 sản phẩm được US FDA cấp phép: 5 sản phẩm nhận diện CD19 trong điều trị u lympho và bệnh bạch cầu, gồm KYMRIAH (Tisagenlecleucel, được cấp phép tháng 08/2017), YESCARTA (Axicabtagene ciloleucel, 10/2017), TECARTUS (Brexucabtagene autoleucel, 07/2020), BREYANZI (Lisocabtagene maraleucel, 02/2021), AUCATZYL (Obecabtagene autoleucel, 11/2024); 2 sản phẩm nhận diện kháng nguyên trưởng thành tế bào B trong điều trị đa u tủy xương, gồm ABECMA (Idecabtagene vicleucel, được cấp phép tháng 03/2021), CARVYKTI (Ciltacabtagene autoleucel, 02/2022).
4. Những khác biệt giữa liệu pháp TCR-T và CAR-T
Cả hai liệu pháp này đều sử dụng các kỹ thuật di truyền để biến đổi tế bào T, khai thác sức mạnh của hệ thống miễn dịch nhằm điều trị ung thư, nhưng có một số khác biệt chính.
Về mặt cấu trúc: TCR là các thụ thể tự nhiên hoặc được biến đổi hạn chế để nhận diện các kháng nguyên khối u. CAR được thiết kế nhân tạo để nhận diện kháng nguyên cụ thể, đồng thời người ta có thể bổ sung trên cấu trúc CAR các vùng giúp tăng cường hoạt động cũng như duy trì sự hoạt hóa và sống còn của tế bào T.
Về khả năng nhận diện kháng nguyên: TCR nhận diện các kháng nguyên có trên bề mặt và bên trong tế bào, được trình diện trên bề mặt qua kháng nguyên bạch cầu người (HLA), cần có sự tương thích HLA giữa bệnh nhân và TCR. CAR nhận diện các kháng nguyên trên bề mặt tế bào và không phụ thuộc HLA. Vì thế, TCR có thể nhận diện kháng nguyên phổ rộng hơn CAR.
Về ứng dụng lâm sàng: TCR-T có nhiều hứa hẹn với các dạng ung thư u đặc như u hắc tố, ung thư phổi, ung thư cổ tử cung,… CAR-T chủ yếu điều trị các bệnh lý ác tính về máu như bệnh bạch cầu cấp/mạn dòng lympho (ALL/CLL), u lympho tế bào B lớn (LBCLu lympho tế bào B lớn (LBCL), u lympho dòng lympho nhỏ (SLL), u lympho nang (FL), u lympho tế bào màng ngoài (MCL), đa u tủy xương,… và khó hiệu quả với u đặc do hàng rào mô, môi trường vi mô ức chế.
TÀI LIỆU THAM KHẢO
1. Shafer P., et al. (2022). Cancer therapy with TCR-engineered T cells: current strategies, challenges, and prospects. Frontiers in immunology, 13, 835762. DOI: 10.3389/fimmu.2022.835762
2. Baulu E., et al. (2023). TCR-engineered T cell therapy in solid tumors: State of the art and perspectives. Science Advances, 9(7), eadf3700. DOI: 10.1126/sciadv.adf3700
3. Sterner R. C., et al. (2021). CAR-T cell therapy: current limitations and potential strategies. Blood cancer journal, 11(4), 69. DOI: 10.1038/s41408-021-00459-7
4. Chen Y. J., et al. (2023). CAR-T: what is next?. Cancers, 15(3), 663. DOI: 10.3390/cancers15030663
5. Haanen J., et al. (2024). Adoptive cell therapy for solid tumors: current status in melanoma and next-generation therapies. American Society of Clinical Oncology Educational Book, 44(3), e431608. DOI: 10.1200/EDBK_431608