Liệu pháp tế bào gốc trung mô CORDStrom với bệnh ly thượng bì bóng nước thể loạn dưỡng lặn (RDEB) và kế hoạch đăng ký cấp phép sản phẩm với FDA Hoa Kỳ
Ly thượng bì bóng nước hay bong biểu bì bullosa (Epidermolysis bullosa – EB) là một nhóm các rối loạn da di truyền đặc trưng bởi tình trạng da rất mỏng manh và phồng rộp. Trong các phân nhóm bệnh, thể loạn dưỡng lặn (Recessive Dystrophic EB – RDEB) và thể loạn dưỡng trội (Dominant Dystrophic EB – DDEB) đều do đột biến gen COL7A1 ảnh hưởng đến collagen loại VII, rất quan trọng đối với sự kết dính của da. RDEB là thể nghiêm trọng, gây phồng rộp lan rộng và vết thương mạn tính, dẫn đến các biến chứng đáng kể như giả dính ngón tay, sẹo nghiêm trọng, tăng nguy cơ ung thư biểu mô tế bào vảy. Tỷ lệ mắc RDEB khoảng 95 ca trên mỗi 1 triệu trẻ em sinh sống, trong đó 37% ở thể trung bình và nặng.
Theo thông cáo báo chí ngày 10/02/2015, Inmune Bio cho biết liệu pháp tế bào gốc CORDStrom của họ có khả năng giảm ngứa và đau, làm giảm hoạt động và cải thiện tình trạng tổn thương da ở những người tham gia nghiên cứu có độ tuổi từ 6 tháng đến 15 tuổi. CORDStrom là sản phẩm tế bào gốc trung mô dây rốn (hucMSC) đồng loài, được sản xuất theo tiêu chuẩn cGMP, được điều chỉnh tối ưu hóa các đặc tính chống viêm, điều hòa miễn dịch, chữa lành vết thương và các đặc tính khác. Trong nghiên cứu MissionEB, 30 trẻ em (dưới 16 tuổi) mắc RDEB ở mức độ trung bình và nặng được tuyển chọn vào nghiên cứu. Những người tham gia được chỉ định ngẫu nhiên sử dụng CORDStrom hoặc giả dược qua đường truyền tĩnh mạch 2 tuần/lần. Sau đó (3 hoặc 6 tháng kể từ lần truyền đầu tiên), họ được chuyển sang chế độ điều trị ngược lại, với hai lần truyền CORDStrom hoặc giả dược, như vậy toàn bộ bệnh nhân đều được đưa vào đánh giá hiệu quả của cả giả dược và MSC.
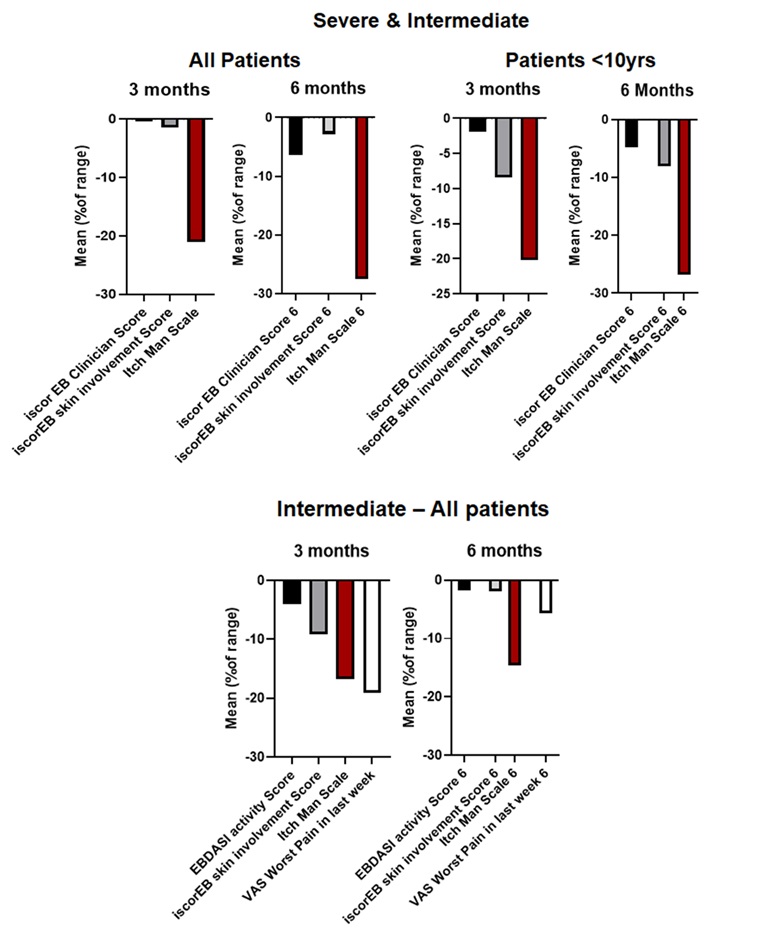
Kết quả thử nghiệm cho thấy CORDStrom được dung nạp tốt, không có biến cố bất lợi nghiêm trọng lên quan đến thuốc được báo cáo sau 3 tháng hoặc 6 tháng điều trị ở tất cả các phân nhóm. Ở trẻ em mắc bệnh nghiêm trọng, CORDStrom giúp giảm ngứa ở tháng thứ 3 và giảm liên tục hơn 27% ở tháng thứ 6, cho thấy mức độ ngứa giảm có ý nghĩa lâm sàng được duy trì theo thời gian. Đối với nhóm thể bệnh mức trung bình, CORDStrom mang lại nhiều cải thiện hơn, bao gồm giảm tổn thương da và giảm đau, cũng như giảm ngứa đáng kể. Ở nhóm mắc RDEB dưới 10 tuổi, CORDStrom cải thiện điểm số da, cho thấy tính toàn vẹn của da tốt hơn và giảm hoạt động của bệnh. Các cuộc phỏng vấn với đối tượng và người chăm sóc ủng hộ mạnh mẽ các lợi ích lâm sàng của CORDStrom; vì cả người chăm sóc và bệnh nhân đều có thể xác định chính xác khi nào dùng MSC, khi nào dùng giả dược – mặc dù là nghiên cứu mù đôi.
Những kết quả thử nghiệm đã giúp nhóm nghiên cứu quyết tâm đăng ký CORDStrom được chấp thuận trong điều trị RDEB nhi khoa, và có thể mở rộng chỉ định sản phẩm này như một nền tảng thuốc trong tương lai. FDA đã cấp cho CORDStrom chỉ định bệnh nhi hiếm gặp (rare pediatric disease designation – RPDD) để điều trị ly thượng bì bóng nước ngày 13/12/2024. Sản phẩm này cũng được cấp chứng nhận ODD (dành cho các thuốc được phát triển để điều trị các bệnh hiếm gặp và thường không mang lại lợi nhuận do sự thiếu phổ biến tình trạng bệnh) ngày 06/01/2025. Điều này mang lại những thuận lợi cho CORDStrom trong việc đăng ký cấp phép chính thức. Inmune Bio dự định đệ trình Đơn xin cấp phép sinh học (Biologics License Application – BLA) lên FDA Hoa Kỳ trong năm 2025, đồng thời chuẩn bị đệ trình Đơn xin cấp phép tiếp thị (Marketing Authorisation Application – MAA) lên Liên minh châu Âu và Vương quốc Anh vào năm 2026.
---------
TÀI LIỆU THAM KHẢO
https://www.biospace.com/press-releases/inmune-bio-announces-plan-to-submit-fda-biologics-license-application-bla-seeking-approval-of-cordstrom-for-treatment-of-recessive-dystrophic-epidermolysis-bullosa-rdeb (Thông cáo báo chí)









