Xét nghiệm vi sinh vật trong nuôi cấy tế bào động vật
1. Nhiễm vi sinh vật trong nuôi cấy tế bào
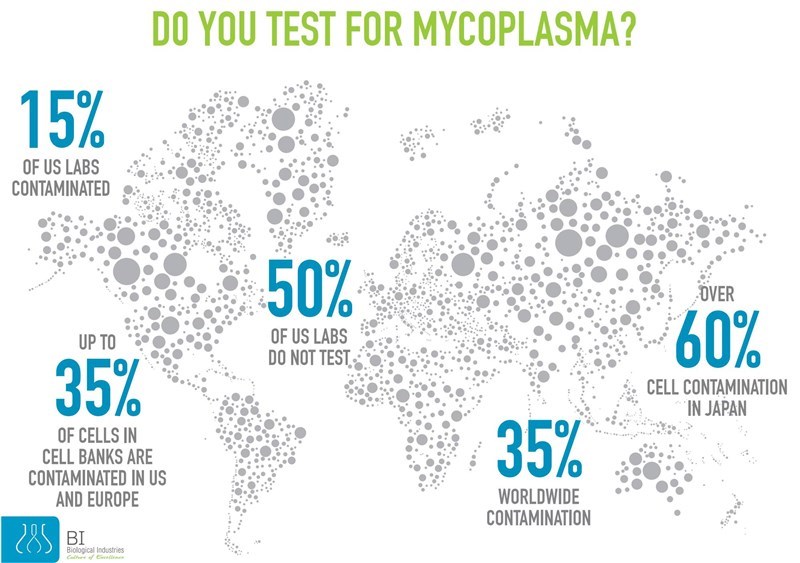
Các vi sinh vật nhiễm trong mẫu sẽ cạnh tranh nguồn dinh dưỡng với tế bào, làm tế bào chậm phát triển và sức sống kém; làm thay đổi quá trình trao đổi chất và biểu hiện gen của tế bào, làm tế bào bị biến đổi mạnh dẫn đến thay đổi các kết quả thử nghiệm; đe dọa tính an toàn của sản phẩm tế bào, gây bệnh cho bệnh nhân sử dụng tế bào (nếu ứng dụng trong lâm sàng hoặc thử nghiệm lâm sàng), một số vi sinh vật có nguy cơ gây bệnh cho kỹ thuật viên nuôi cấy tế bào thao tác với mẫu bị nhiễm.
Đa số các mẫu tế bào trong quá trình nuôi cấy bị nhiễm vi khuẩn, vi nấm đều có thể dễ dàng phát hiện với một số dấu hiệu như: môi trường đục, đổi màu do thay đổi pH, có mùi, quan sát thấy vi khuẩn hoặc vi nấm dưới kính hiển vi,… Mặc dù vậy, một số mẫu nuôi cấy bị nhiễm vi sinh vật không phát hiện được bằng trực quan, hoặc các sản phẩm tế bào bị nhiễm khuẩn trong quá trình chuẩn bị sản phẩm (không tiếp tục nuôi cấy), nên việc xét nghiệm vi sinh vật bằng phương pháp tin tưởng là điều cần thiết. Các tiêu chuẩn FDA Hoa Kỳ và AABB về sản phẩm liệu pháp tế bào đều quy định cần xét nghiệm vi khuẩn và vi nấm trong mẫu.

2. Nguyên nhân
- Từ kỹ thuật viên: không đảm bảo nguyên tắc vô trùng khi làm việc, trực tiếp làm mẫu bị nhiễm vi sinh vật từ cơ thể như tụ cầu da, vi khuẩn đường hô hấp - tiêu hoá
- Từ môi trường phòng thí nghiệm: không đảm bảo nguyên tắc vận hành phòng sạch vô khuẩn, hoặc sự cố cơ sở vật chất, dẫn đến vi vi sinh vật xâm nhập từ ngoài vào môi trường phòng thí nghiệm
- Từ vật tư, hóa chất: bị nhiễm vi sinh vật từ nguồn sản xuất, hoặc trong quá trình vận chuyển, bảo quản vật tư – hóa chất
- Từ mẫu tế bào khác: mẫu tế bào bị nhiễm vi sinh vật (chủ yếu từ nguồn phân lập không thể loại bỏ hoàn toàn vi sinh vật, ví dụ mẫu dây rốn mang theo nấm âm đạo, mẫu răng sữa có chứa vi khuẩn khoang miệng) làm nhiễm chéo sang các mẫu tế bào khác cùng nuôi cấy
3. Xét nghiệm vi sinh vật trong nuôi cấy tế bào
- FDA Hoa Kỳ quy định sản phẩm liệu pháp tế bào phải được xét nghiệm theo phương pháp mô tả trong Mục 21 CFR 610.12 (CFR: the Code of Federal Regulations – Bộ luật Liên bang) hoặc các phương pháp được chứng minh là tương đương. Phương pháp CFR sử dụng môi trường Thioglycollate lỏng và môi trường Casein đậu tương để phát hiện nhiều loại vi sinh vật dựa vào phân tích độ đục trong quá trình nuôi cấy ít nhất 14 ngày. Mặc dù được FDA coi là phương pháp tiêu chuẩn, nhưng phương pháp này tốn nhiều thời gian và công sức, cách thức nhận định chủ quan, và có ít dữ liệu được công bố về khả năng áp dụng đối với các sản phẩm liệu pháp tế bào.
- Các hệ thống nuôi cấy vi sinh vật tự động đang phát triển mạnh trên thị trường. Sự phát triển của vi sinh vật được xác định gián tiếp thông qua sự sản sinh CO2 trong quá trình sinh trưởng, nhờ cơ chất phát màu hoặc huỳnh quang được phát hiện qua các cảm biến nhạy hơn và nhanh hơn nhiều so với phương pháp so màu thủ công. Những hệ thống tự động hóa được sử dụng nhiều nhất là BacT/ALERT (bioMerieux) và Bactec (Becton Dickinson), chiếm trên 90% thị phần, và đã được chứng minh có thể sử dụng để kiểm tra vi sinh vật cho các sản phẩm liệu pháp tế bào. Việc lấy mẫu ngay tại phòng nuôi cấy vô trùng vào các chai cấy vi sinh, sau đó chuyển đến hệ thống tự động cũng tạo nên quy trình kín, tránh được vấn đề ngoại nhiễm gây dương tính giả cho xét nghiệm.
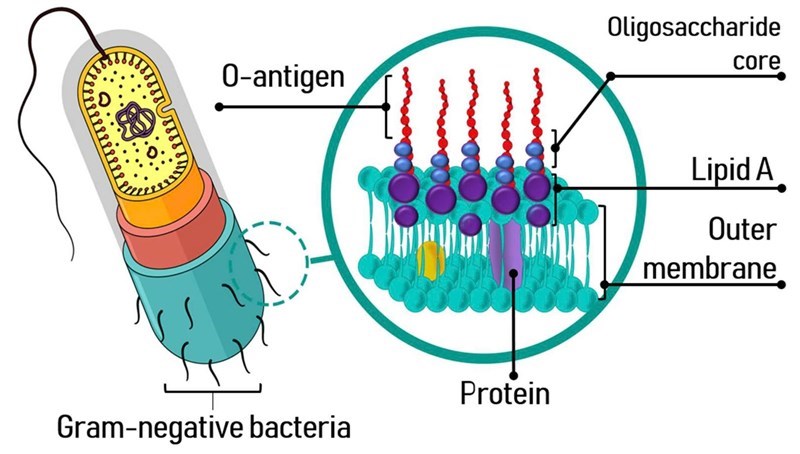
- Phương pháp nhuộm Gram có giới hạn phát hiện khá cao, ở mức 10^5 vi khuẩn/mL, cao hơn rất nhiều so với mẫu sản phẩm tế bào bị nhiễm trong quá trình chuẩn bị (thậm chí có thể cao hơn so với mẫu nhiễm trong quá trình nuôi cấy). Vì vậy, độ nhạy của phương pháp này không cho phép nó trở thành phương pháp phát hiện vi sinh vật trong mẫu tế bào, chỉ nên bổ sung cho các phương pháp nuôi cấy để hỗ trợ phân loại, định danh vi sinh vật.
TÀI LIỆU THAM KHẢO
1. Code of federal regulations (CFR). General biological products standards. Title 21, CFR Part 610 - general biological products standards. Washington, DC: US Government Printing Office, 2009 (revised annually).
2. United States Food and Drug Administration. (2008). Validation of Growth‐Based Rapid Microbiological Methods for Sterility Testing of Cellular and Gene Therapy Products.
3. AABB (2009). Cellular Therapy : Principles, Methods, and Regulations. 1st Edition, edition E.M. Areman and K. Loper.
4. Gebo J.E., & Lau A.F. (2020). Sterility testing for cellular therapies: what is the role of the clinical microbiology laboratory?. Journal of Clinical Microbiology, 58(7), 10-1128.
5. Khuu H.M., Patel N., Carter C.S., Murray P.R., & Read E.J. (2006). Sterility testing of cell therapy products: parallel comparison of automated methods with a CFR‐compliant method. Transfusion, 46(12), 2071-2082.