Liệu pháp CAR-T: bước đột phá của liệu pháp tế bào trong điều trị ung thư
1. Liệu pháp CAR-T là gì
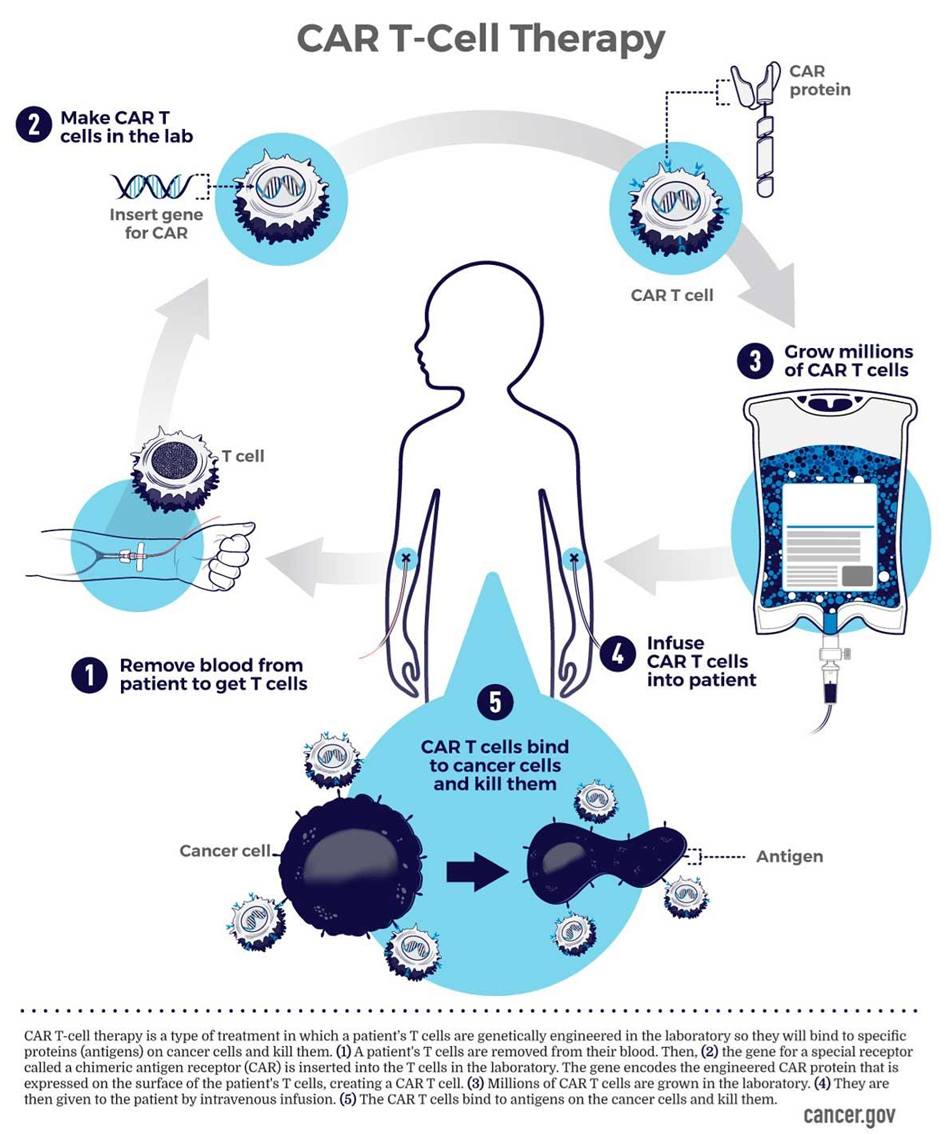
Thụ thể kháng nguyên khảm (Chimeric Antigen Receptor, CAR) là các protein thụ thể được thiết kế bao gồm cả chức năng liên kết với kháng nguyên đặc hiệu và chức năng kích hoạt tế bào miễn dịch. Các tế bào T mang cấu trúc CAR (CAR-T) có khả năng phát hiện đặc hiệu các tế bào ung thư, điều mà tế bào T bình thường không làm được hoặc nhận diện kém. Khi được truyền vào cơ thể bệnh nhân, tế bào CAR-T đi tìm và tiêu diệt tế bào ác tính, đồng thời có khả năng nhân lên để duy trì nguồn “thuốc sống” này trong cơ thế, ức chế ung thư.
2. Liệu pháp CAR-T trong các bệnh lý ác tính về máu
Liệu pháp CAR-T mang đến một phương pháp đầy hứa hẹn để điều trị một số bệnh ung thư máu, và các thử nghiệm lâm sàng hiện tại chủ yếu tập trung CAR-T đến các bệnh lý huyết học ác tính. Tính đến hết tháng 6 năm 2025, đã có 7 sản phẩm CAR-T được FDA Hoa Kỳ phê duyệt bao gồm:
- 5 sản phẩm được thiết kế với CAR nhận diện đặc hiệu CD19 trong điều trị u lympho và bệnh bạch cầu, bao gồm KYMRIAH (Tisagenlecleucel, được cấp phép tháng 08/2017), YESCARTA (Axicabtagene ciloleucel, 10/2017), TECARTUS (Brexucabtagene autoleucel, 07/2020), BREYANZI (Lisocabtagene maraleucel, 02/2021), AUCATZYL (Obecabtagene autoleucel, 11/2024);
- 2 sản phẩm được thiết kế với CAR nhận diện đặc hiệu kháng nguyên trưởng thành tế bào B (BCMA) trong điều trị đa u tủy xương, gồm ABECMA (Idecabtagene vicleucel, được cấp phép tháng 03/2021), CARVYKTI (Ciltacabtagene autoleucel, 02/2022).
Ngoài CD19 và BCMA là các đích phổ biến khi thiết kế CAR, các thử nghiệm lâm sàng hiện tại đang hướng tới những kháng nguyên tiềm năng khác trong các bệnh ung thư máu, như CD20 (u lympho không Hodgkin), CD30 (u lympho Hodgkin), CD33 (bệnh bạch cầu dòng tủy cấp tính– AML),… Một số nghiên cứu gần đây đang hướng tới CD45 là kháng nguyên phổ biến trên các tế bào máu, kết hợp các chiến lược giúp CAR-T phân biệt tế bào lành và ác tính, để mang đến giải pháp điều trị ung thư huyết học nói chung.
3. Liệu pháp CAR-T cho ung thư u đặc và bệnh lý khác
Ngược lại với những tiến bộ của CAR-T trong điều trị các bệnh lý huyết học ác tính, việc nghiên cứu và thử nghiệm liệu pháp này trên u đặc gặp rất nhiều hạn chế. Nguyên nhân có thể do tính không đồng nhất của kháng nguyên, vi môi trường khối u đặc ức chế miễn dịch nên ức chế hoặc bất hoạt CAR-T, rào cản vật lý và mô đệm ngăn cản tế bào CAR-T xâm nhập,… Tuy nhiên hiện nay, nhiều thử nghiệm đã có những chiến lược khắc phục hiện tượng trên, và cho thấy những tín hiệu tích cực về liệu pháp này trong điều trị u thần kinh đệm, sarcoma, ung thư biểu mô tế bào thận,… Tại hội nghị thường niên năm 2025 của Hiệp hội Ung thư lâm sàng Hoa Kỳ (ASCO 2025) cũng đã có những báo cáo về sử dụng CAR-T trong điều trị u não, ung thư dạ dày, ung thư đoạn nối dạ dày – thực quản,…
Ngoài ung thư, liệu pháp CAR-T cũng đang được thử nghiệm trong điều trị các bệnh tự miễn như lupus ban đỏ hệ thống, viêm cơ, xơ cứng hệ thống,… Cấu trúc CAR được thiết kế nhắm vào các tế bào miễn dịch cụ thể như tế bào B (có vai trò trong phản ứng tự miễn), hoặc CAR-T với tế bào T điều hòa có khả năng dung nạp kháng nguyên cụ thể giúp giảm đáp ứng miễn dịch.
4. Thụ thể CAR cho các loại tế bào khác
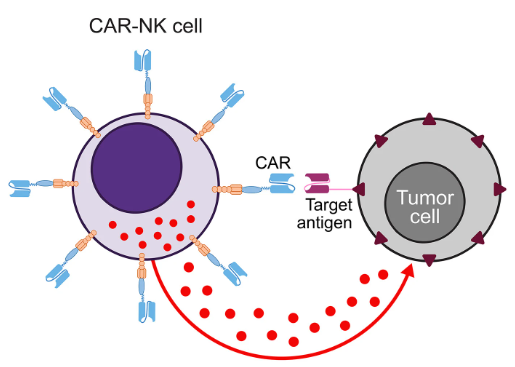
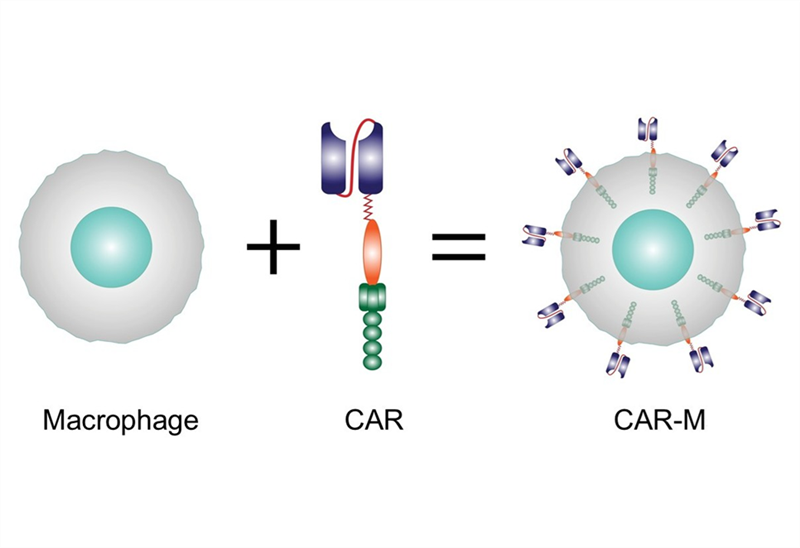
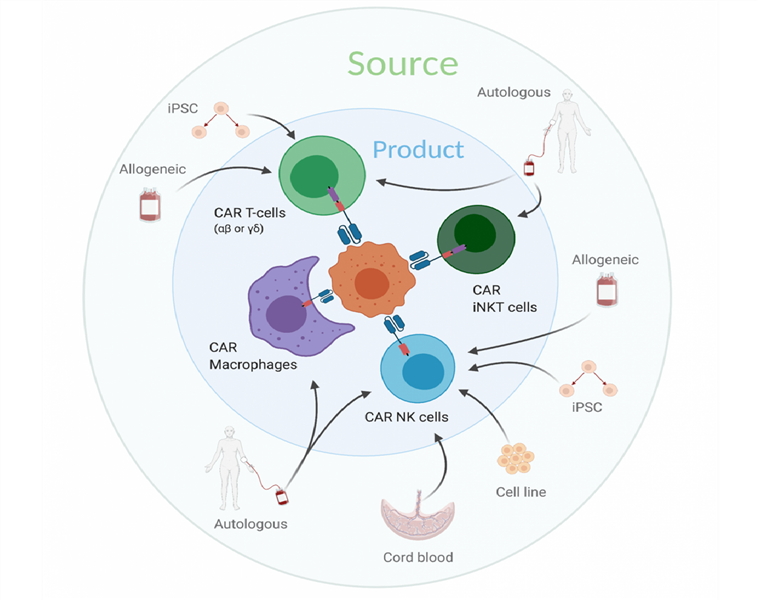
Ngoài CAR-T, cấu trúc CAR có thể được thiết kế cho nhiều loại tế bào miễn dịch khác như tế bào giết tự nhiên (CAR-NK, thử nghiệm điều trị đa u tủy xương, bệnh bạch cầu dòng tủy/dòng lympho cấp tính, ung thư buồng trứng,…), tế bào NKT (CAR-NKT, thử nghiệm điều trị u nguyên bào thần kinh, bệnh bạch cầu dòng lympho cấp/mạn tính, u lympho tế bào B,…), đại thực bào (CAR-M, thử nghiệm điều trị ung thư buồng trứng, vú, thực quản,…).
TÀI LIỆU THAM KHẢO
1. Wang C., et al. (2023). CAR-T cell therapy for hematological malignancies: History, status and promise. Heliyon, 9(11). DOI: 10.1016/j.heliyon.2023.e21776
2. Du B., et al. (2025). CAR-T therapy in solid tumors. Cancer Cell, 43(4), 665-679. DOI: 10.1016/j.ccell.2025.03.019
3. Vukovic J., et al. (2024). CAR-engineered T cell therapy as an emerging strategy for treating autoimmune diseases. Frontiers in Medicine, 11, 1447147. DOI: 10.3389/fmed.2024.1447147
4. Hadiloo K., et al. (2023). CAR-NKT cell therapy: a new promising paradigm of cancer immunotherapy. Cancer Cell International, 23(1), 86. DOI: 10.1186/s12935-023-02923-9
5. Hadiloo K., et al. (2023). The CAR macrophage cells, a novel generation of chimeric antigen-based approach against solid tumors. Biomarker research, 11(1), 103. DOI: 10.1186/s40364-023-00537-x
6. Wang W., et al. (2024). Breakthrough of solid tumor treatment: CAR-NK immunotherapy. Cell Death Discovery, 10(1), 40. DOI: 10.1038/s41420-024-01815-9.