LIỆU PHÁP TẾ BÀO GỐC
Liệu pháp tế bào gốc là hướng tiếp cận tiên tiến trong y học tái tạo, dựa trên khả năng tự làm mới và biệt hóa của tế bào gốc thành nhiều loại tế bào chuyên biệt trong cơ thể. Nhờ đặc tính này, tế bào gốc có tiềm năng hỗ trợ phục hồi mô và cơ quan bị tổn thương.
Tiềm năng phòng tránh và điều trị vật ghép chống chủ cấp tính sau ghép tế bào gốc tạo máu bằng cách tác động đến hệ vi khuẩn đường ruột
Ghép tế bào gốc tạo máu đồng loài (allogeneic hematopoietic stem cell transplantation – allo-HCT) được thực hiện bằng cách truyền tế bào gốc tạo máu của người hiến cho người nhận mắc các bệnh như ung thư máu, suy tủy xương, một số rối loạn máu di truyền,… Tác dụng phụ thường gặp nhất và cũng nguy hiểm nhất là bệnh mảnh ghép chống chủ cấp tính (Acute graft-versus-host disease – aGVHD), đó là tình trạng xảy ra khi các tế bào miễn dịch của người hiến tấn công các mô của người nhận (tình trạng cấp tính thường xảy ra trong vòng 3 tháng đầu sau ghép). Các nghiên cứu gần đây chứng minh vai trò quan trọng của hệ vi sinh vật trong aGVHD, trong đó chứng rối loạn vi khuẩn đường ruột góp phần vào quá trình bệnh sinh của nó. Tình trạng loạn khuẩn này có thể dẫn đến sự xuất hiện của các vi khuẩn cộng sinh gây bệnh, với nhiều loài thuộc chi cầu khuẩn Enterococcus, đặc biệt là E. faecalis và E. faecium, liên quan đến kháng nhiều loại thuốc ở bệnh nhân allo-HCT. Cấu trúc mô ruột ở chuột bình thường và chuột bị nhiễm E. faecalis được và không được điều trị với endolysin. Mới đây, một nhóm nghiên cứu tại Nhật Bản đã tiến hành phân tích chuyên sâu về hệ vi sinh đường ruột của bệnh nhân allo-HCT để từ đó xây dượng liệu pháp hiệu quả điều trị chứng loạn khuẩn đường ruột liên quan đến aGVHD (kết quả nghiên cứu mới được đăng gần đây trên tạp chí danh giá Nature ngày 10 tháng 7 năm 2024). Nhóm nghiên cứu đã kiểm tra hệ vi sinh đường ruột của bệnh nhân allo-HCT và phát hiện sự chiếm ưu thế của các loài Enterococcus, đặc biệt là E. faecalis. Điều này đặc biệt liên quan đến bệnh bạch cầu cấp tính, vì các chủng E. faecalis tuy rằng nhạy cảm với một số loại kháng sinh, nhưng lại sở hữu các gen liên quan đến cytolysin (một loại độc tố mạnh để tiêu hủy tế bào). Nghiên cứu sâu hơn, các nhà khoa học đã phát hiện một loại enzyme là endolysin, có tính kháng khuẩn mạnh mẽ đối với E. faecalis (enzyme này có nguồn gốc từ thực khuẩn thể (phage), là loại virus nhân lên và lây nhiễm trong các loài vi khuẩn và vi khuẩn cổ). Trong các thử nghiệm in vitro và in vivo, endolysin được chứng minh có hoạt tính phổ hẹp chống lại E. faecalis mà không ảnh hưởng đến các loài vi khuẩn đường ruột khác. Trên mô hình chuột, những con chuột bị aGVHD được điều trị bằng endolysin đã giảm đáng kể lượng vi khuẩn E. faecalis trong phân và ức chế sự phát triển của aGVHD. Đồng thời, trong một thử nghiệm khác, những con chuột có hệ vi khuẩn đường ruột giống với người được điều trị bằng endolysin đã giảm lượng vi khuẩn Enterococcus và cải thiện tỷ lệ sống sót. Phát hiện về enzyme endolysin hứa hẹn những ứng dụng trong tương lai trong việc ngăn ngừa hoặc điều trị aGVHD, mang lại hy vọng cho những can thiệp phù hợp trong ghép tế bào gốc tạo máu. TÀI LIỆU THAM KHẢO Fujimoto K., et al. An enterococcal phage-derived enzyme suppresses graft-versus-host disease. Nature, 2024; DOI: https://doi.org/10.1038/s41586-024-07667-8
24/01/2026

Thuốc điều trị ung thư cyclophosphamide giúp bệnh nhân ghép tế bào gốc tạo máu tránh được hiện tượng mảnh ghép chống vật chủ (GvHD)
Cấy ghép tế bào gốc tạo máu là phương pháp được áp dụng trong điều trị và hỗ trợ điều trị nhiều bệnh lý ung thư, nhằm khôi phục hệ thống tạo máu cho bệnh nhân. Độ tương thích của người hiến được xác định bằng tập hợp các dấu hiệu protein trên tế bào máu gọi là kháng nguyên bạch cầu người (Human Leukocyte Antigen – HLA), với 8 locus HLA–A, HLA–B, HLA–C, HLA–DR. Độ phù hợp hoàn toàn được xác định khi đạt điểm 8/8 (ngay cả trong những trường hợp anh chị em ruột, xác suất phù hợp hoàn toàn là 25%), còn độ phù hợp một phần được xác định khi đạt điểm 4/8 đến 7/8 (tỷ lệ gặp 50% ở anh chị em ruột). Khi ghép với độ phù hợp HLA thấp, các tế bào được ghép sẽ kích thích phản ứng miễn dịch trầm trọng ở bệnh nhân, gây nên tác dụng phụ nguy hiểm nhất (có thể gây chết người) của cấy ghép: mảnh ghép chống chủ (graft-versus-host disease – GvHD). Theo Viện Y tế Quốc gia Hoa Kỳ, GvHD thường xảy ra ở 60% đến 80% ca ghép mà người hiến tặng và người nhận không có quan hệ họ hàng. Theo một nghiên cứu được báo cáo tại Hội nghị 2024 của Hiệp hội Ung thư Lâm sàng Hoa Kỳ (ASCO), việc sử dụng một loại thuốc điều trị ung thư là cyclophosphamide vài ngày sau khi ghép tế bào gốc có thể giúp các trường hợp cấy ghép phù hợp một phần giảm thiểu hiện tượng GvHD. Khi theo dõi trên 70 bệnh nhân ung thư máu tiến triển được ghép phù hợp một phần có sử dụng cyclophosphamide, tỷ lệ bệnh nhân sống thêm toàn bộ (overall survival – OS) sau 1 năm là 79%, tương đương với những người được nhận sản phẩm cấy ghép từ người hiến phù hợp hoàn toàn. Sau một năm, 51% số bệnh nhân không còn phát hiện GvHD và không tái phát bệnh. Nhóm nghiên cứu mô tả dữ liệu này “rất ấn tượng”, đặc biệt là vì đã ghi nhận những bệnh nhân có nguy cơ cao và tuổi trung bình là 65. Những kết quả này đã mang lại cơ hội cho những bệnh nhân ung thư máu tìm được người hiến phù hợp hơn (đặc biệt là những người hiến trẻ, khỏe mạnh) và tỷ lệ ghép thành công cao hơn, khi mà sự phù hợp HLA không còn yêu cầu ở mức hoàn toàn. Ở mức độ phù hợp HLA ở mức 5/8 trở lên, trên 99% dân số sẽ tìm được người hiến tặng. Các nhà nghiên cứu cho biết cyclophosphamide ngày càng được sử dụng nhiều hơn trong thập kỷ qua để tăng cơ hội ghép tế bào gốc thành công từ người hiến tặng phù hợp HLA một phần. Hiện tại thử nghiệm lâm sàng giai đoạn II với hơn 300 bệnh nhân ở 30 cơ sở y tế tại Hoa Kỳ đang được thực hiện (mã số thử nghiệm NCT04904588, có thể tra cứu trên https://clinicaltrials.gov/). Những mục tiêu tiếp theo mà thử nghiệm hướng đến bao gồm tăng cường độ điều trị trước khi cấy ghép, áp dụng phác đồ cho các bệnh nhân nhi, tối ưu hóa việc sự dụng cyclophosphamide và kết hợp các phương pháp điều trị khác để giảm thiểu độc tính và nhiều vấn đề liên quan khác. TÀI LIỆU THAM KHẢO - Charlotte Schubert, “The Imperfect Match: Offering Transplants to More Blood Cancer Patients” (https://news.med.miami.edu/offering-transplants-to-more.../) - Al Malki M. M., et al. (2024). Post-transplant cyclophosphamide-based graft-versus-host disease prophylaxis following mismatched unrelated donor peripheral blood stem cell (PBSC) transplantation. Journal of Clinical Oncology 42 (16 suppl). Meeting Abstract: 2024 ASCO Annual Meeting I (https://ascopubs.org/doi/10.1200/JCO.2024.42.16_suppl.6503)
23/01/2026
Viagra giúp huy động tế bào gốc tạo máu nhanh chóng và hiệu quả
Cấy ghép tế bào gốc tạo máu là phương pháp được áp dụng trong điều trị và hỗ trợ điều trị nhiều bệnh lý ung thư, nhằm khôi phục hệ thống tạo máu cho bệnh nhân. Những tế bào gốc tạo máu thường chỉ cư trú trong tủy xương, trước đây thường được thu nhận bằng cách khoan vào thành trên xương chậu (mào chậu) để hút dịch tủy xương. Hiện nay, phương pháp chủ yếu là sử dụng các thuốc để huy động tế bào gốc tạo máu từ tủy xương đi vào hệ thống mạch máu, sau đó thu thập chúng từ máu ngoại vi. Phác đồ huy động tiêu chuẩn là tiêm yếu tố kích thích bạch cầu hạt (Granulocyte colony-stimulating factor, G-CSF) hằng ngày cho người hiến trong 4-6 ngày trước khi thu thập tế bào gốc. Mặc dù ít đau đớn hơn chọc hút tủy xương, tuy nhiên việc huy động tế bào gốc thường gây đau xương và một số tác dụng phụ khác, và không phải thành công trong mọi trường hợp. Theo một báo cáo mới công bố gần đây, nhóm nghiên cứu tại Viện Sinh học Tế bào gốc, Đại học Calofornia (Hoa Kỳ) đã chứng minh một chế độ thay thế giúp huy động tế bào gốc chỉ trong 2 giờ với hiệu suất cao. Chế độ này bao gồm một liều Viagra uống duy nhất và tiêm Plerixafor sau đó 2 giờ. Đây là 2 loại thuốc được Cục Quản lý Thực phẩm và Dược phẩm (FDA) phê duyệt, với chi phí thấp hơn nhiều G-CSF. Viagra, là một loại thuốc an toàn và được nghiên cứu kỹ lưỡng nhằm thúc đẩy việc giãn mạch, làm tăng lưu lượng máu đến các mô, được biết đến nhiều nhất như một loại thuốc điều trị rối loạn cương dương. Thuốc còn lại là Plerixafor, là chất ức chế Cxcr4 (một thụ thể trên bề mặt tế bào gốc tạo máu giúp chúng bám vào hốc trong tủy xương), được sử dụng để huy động tế bào gốc nhưng kém hiệu quả khi được sử dụng độc lập. Phương thức này huy động được tế bào gốc nhanh hơn rất nhiều và ít tốn kém hơn so với phác đồ chuẩn và đa số các phác đồ đang được nghiên cứu. Nó càng có ý nghĩa với những người cần được huy động nhưng không thể sử dụng G-CSF, ví dụ bệnh nhân mắc bệnh hồng cầu hình liềm sẽ bị loại thuốc này làm trầm trọng thêm các triệu chứng bệnh, nhưng nếu dùng chế độ huy động mới có thể thu được các tế bào gốc tạo máu, chỉnh sửa di truyền và truyền trở lại cho bệnh nhân. Nhóm nghiên cứu cho biết: khi mạch máu được giãn bằng Viagra, các tế bào được Plerixafor huy động sẽ có khả năng đi vào dòng máu tốt hơn. Đây là những loại thuốc sẵn có và đã được FDA phê duyệt nên có khả năng nhanh chóng trở thành phác đồ được sử dụng hơn so với việc nghiên cứu các loại thuốc mới để huy động tế bào gốc. Nghiên cứu này được tài trợ bởi Hiệp hội Ung thư Hoa Kỳ (American Association for Cancer Research, AACR), đã được thử nghiệm thành công trên chuột và sẽ sớm được đánh giá tính an toàn và hiệu quả trên người. TÀI LIỆU THAM KHẢO Smith-Berdan S., Bercasio A., Rajendiran S., and Forsberg E. C. (2019). Viagra enables efficient, single-day hematopoietic stem cell mobilization. Stem Cell Reports, 13(5), 787-792. DOI: https://doi.org/10.1016/j.stemcr.2019.09.004
23/01/2026
Tình trạng kinh tế xã hội của người hiến tế bào ảnh hưởng đến kết quả cấy ghép tế bào gốc tạo máu (HSC) trong điều trị ung thư.
Theo một nghiên cứu mới công bố trên PNAS (Proceedings of the National Academy of Sciences) ngày 15/07/2024, tình trạng kinh tế xã hội của người hiến tế bào ảnh hưởng đến kết quả sức khỏe của bệnh nhân ung thư máu được ghép tế bào gốc tạo máu, bất kể tình trạng kinh tế xã hội của bệnh nhân ung thư. Nghiên cứu hồi cứu được thực hiện trên 2.005 bệnh nhân ung thư máu được điều trị bằng ghép tế bào gốc tạo máu ở 125 bệnh viện tại Hoa Kỳ, thời gian theo dõi là 120 tháng. Với việc phân tầng tương đối đồng đều các đối tượng nghiên cứu thành 4 nhóm, nghiên cứu đã chỉ ra những bệnh nhân được nhận tế bào từ người hiến có kinh tế xã hội ở nhóm khó khăn nhất đã giảm 9,7% tỷ lệ sống toàn trạng và tăng 6,6% tỷ lệ tử vong liên quan đến cấy ghép trong ba năm so với nhóm nhận tế bào từ người hiến có kinh tế xã hội ở nhóm tốt nhất. Kết quả này phù hợp với những nghiên cứu trước đây liên quan đến sự bất lợi về kinh tế xã hội với chức năng tế bào miễn dịch và quá trình tạo máu bị thay đổi, chúng thực sự tồn tại dai dẳng ngay cả khi tế bào được chuyển vào môi trường vật chủ mới (người được hiến tặng). Sự khác biệt về tỷ lệ sống sót toàn trạng (A), tỷ lệ tử vong liên quan đến điều trị (B), tỷ lệ sống thêm không bệnh (C) và tỷ lệ tái phát (D) được phân tầng theo tình trạng kinh tế xã hội của người hiến tặng (tình trạng kinh tế xã hội giảm dần từ Nhóm 1 đến Nhóm 4). Nhóm nghiên cứu mong muốn tiến hành những nghiên cứu sâu hơn để điều chỉnh các yếu tố sinh lý nhằm đưa ra những biện pháp giảm thiểu các kết quả bất lợi cho sức khỏe do tình trạng kinh tế xã hội gây ra. Đồng thời, phát hiện này cho thấy một trong những ảnh hưởng sâu sắc đến sức khỏe của sự bất bình đẳng xã hội và nêu bật nhu cầu cấp thiết về chăm sóc sức khỏe cộng đồng. TÀI LIỆU THAM KHẢO Turcotte L. M., et al. (2024). The health risk of social disadvantage is transplantable into a new host. Proceedings of the National Academy of Sciences, 121(30), e2404108121. DOI: https://doi.org/10.1073/pnas.240410812
23/01/2026

Mô hình “phổi trên vi mạch” (lung-on-a-chip) đầu tiên của người được xây dựng từ tế bào gốc của một người hiến duy nhất và mô hình nghiên cứu bệnh lao
1. Mô hình organ-on-a-chip Một organ-on-a-chip (OoC), có thể hiểu là “cơ quan trên vi mạch”, là một con chip trên đó chứa các tế bào được nuôi cấy 3D kết hợp cùng các kênh dẫn truyền để mô phỏng các hoạt động và phản ứng sinh lý của một cơ quan hoặc một hệ thống cơ quan. Trên các kênh này, chất lỏng có thể được bơm linh hoạt như cung cấp máu, hoặc không khí được dẫn truyền giống như hoạt động hô hấp ở phổi. Bằng cách hoạt động mô phỏng giống hệt các mô phức tạp trong cơ thể, hệ thống này mang lại những lợi thế lớn hơn nhiều so với nuôi cấy tế bào tiêu chuẩn hay động vật trong nghiên cứu mô hình bệnh lý, phát triển thuốc, thử nghiệm độc tố,… Mô hình lung-on-a-chip (LoC) – “phổi trên vi mạch” là hệ thống mô phỏng hoạt động của phổi con người, tương tự như nhiều cơ quan khác. Ở phổi, các túi khí gọi là phế nang diễn ra quá trình trao đổi khí thiết yếu, đồng thời cũng là rào chắn quan trọng chống lại virus và vi khuẩn đi qua đường hô hấp. Các nhà nghiên cứu đã mô phỏng cấu trúc phế nang trên con chip nhỏ để hiểu cách chúng hoạt động và phản ứng với sự nhiễm trùng. Từ trước tới nay, các thiết bị LoC được tạo ra từ hỗn hợp các tế bào của bệnh nhân và các tế bào thương mại trên thị trường, nghĩa là chưa mô phỏng hoàn toàn chức năng phổi hoặc quá tình tiến triển bệnh phối của một cá nhân cụ thể. 2. Mô hình lung-on-a-chip phát triển từ tế bào gốc của một người hiến duy nhất và mô hình nghiên cứu bệnh lao Các nhà nghiên cứu tại Viện Francis Crick (Anh) kết hợp cùng các chuyên gia của AlveoliX (Bỉ) đã tạo ra mô hình lung-on-a-chip đầu tiên chỉ sử dụng tế bào gốc lấy từ một người duy nhất. Những con chip này mô phỏng chức năng và bệnh lý ở phổi của từng cá nhân, hứa hẹn sẽ thử nghiệm các phương pháp điều trị bệnh lao và nhiều bệnh hô hấp khác. Nhóm nghiên cứu đã tạo ra các tế bào biểu mô phế nang và nội mô mạch máu từ tế bào gốc đa tiềm năng cảm ứng (induced pluripotent stem cell – iPSC) ở người, đây là loại tế bào có khả năng biệt hóa thành hầu hết các loại tế bào có trong cơ thể. Hai loại tế bào này được nuôi cấy riêng biệt ở mặt trên và mặt dưới của một màng mỏng con chip để tái tạo hàng rào túi khí. Ngoài ra, AlveoliX đã thiết kế hệ thống chuyên dụng để tạo ra lực kéo giãn ba chiều theo nhịp điệu tác động lên túi khí được tạo ra, mô phỏng lại chuyển động của hô hấp. Điều này kích thích hình thành các vi nhung mao, một đặc điểm quan trọng của tế bào biểu mô phế nang để tăng diện tích bề mặt cho các chức năng của phổi. Sau đó, các nhà khoa học đã thêm các đại thực bào (cũng được tạo ra từ iPSC của người đó) và vi khuẩn lao Mycobacterium tuberculosis vào chip để mô phỏng giai đoạn đầu của quá trình nhiễm bệnh. Trên cấu trúc này đã hình thành các cụm đại thực bào chứa lõi hoạt tử - gồm các tế bào chết hoại tử ở trung tâm, được bao ngoài bởi các đại thực bào sống. Sau 5 ngày nhiễm trùng, hàng tào tế bào nội mô và biểu mô bị sụp đổ, mô phỏng việc phế nang bị phá vỡ. Hiện nay, nhiễm trùng đường hô hấp và các biến chứng của nó tạo nên mối quan ngại lớn về sức khỏe cộng động. Việc tạo ra các mô hình lung-on-a-chip giúp hiểu rõ cấu trúc phổi để nghiên cứu bệnh học và phương pháp điều trị bệnh. Đặc biệt, các chip được tạo ra từ các tế bào của một người duy nhất sẽ cho phép chúng ta mô phỏng tình trạng phổi và khả năng đáp ứng thuốc của từng cá nhân, từ đó đưa ra phương pháp điều trị phù hợp cho từng người (y học cá thể hóa). TÀI LIỆU THAM KHẢO Luk C. H., et al. (2026). Autologous human iPSC–derived alveolus-on-chip reveals early pathological events of Mycobacterium tuberculosis infection. Science Advances, 12(1), eaea9874. DOI: https://doi.org/10.1126/sciadv.aea9874
23/01/2026
Sự hình thành những quần thể tế bào không đồng nhất trong quá trình biệt hóa của tế bào gốc đa tiềm năng
Tế bào gốc đa tiềm năng ở người (human Pluripotent Stem Cell – hPSC) là những tế bào có khả năng biệt hóa thành tất cả các loại tế bào có trong cơ thể, nhưng không biệt hóa được thành các tế bào thuộc phần phụ ngoài phôi (nhau thai, cuống rốn) nên không phát triển được thành cơ thể hoàn chỉnh. Những loại tế bào gốc đa tiềm năng được quan tâm nhiều nhất bao gồm tế bào gốc phôi (Embryonic Stem Cell – ESC) và tế bào gốc đa tiềm năng cảm ứng (induced Pluripotent Stem Cell – iPSC). Quá trình biệt hóa của hPSC hiếm khi diễn ra hoàn toàn đồng nhất, thường chứa hỗn hợp các tế bào ở các giai đoạn khác nhau. Sự thiếu đồng nhất này là kết quả của việc các tế bào phản ứng khác nhau với tín hiệu biệt hóa, tạo ra những tế bào khác nhau ngay cả trong điều kiện được kiểm soát. Sự không đồng nhất giữa các dòng và trong cùng một dòng: Sự khác biệt giữa các dòng tế bào gốc và sự khác biệt trong cùng một dòng đều góp phần tạo nên sự thiếu đồng nhất. Đặc điểm di truyền, trạng thái ngoại gen (epigenetic) và những điều kiện nuôi cấy có thể ảnh hưởng đến hiệu quả của việc từng tế bào duy trì tính đa tiềm năng, hoặc chuyển sang các dòng tế bào chuyên hóa. Khi tế bào trải qua quá trình biệt hóa, chúng có thể diễn ra với tốc độ khác nhau. Một số tế bào chuyển đổi nhanh chóng, trong khi những tế bào khác chậm hơn, hoặc chúng đi theo các con đường khác nhau. Sự biệt hóa không đồng bộ này làm tăng khả năng tạo ra các trạng thái tế bào lệch khỏi con đường biệt hóa dự tính. Hình thành các loại tế bào không mong muốn: Khi các phân nhóm tế bào không biệt hóa hoàn toàn được thành tế bào đích, chúng có thể trở thành các dạng trung gian chưa trưởng thành hoặc hình thành các loại tế bào không thường có trong cơ thể sống. Những trạng thái này làm tăng độ phức tạp dẫn đến khó khăn trong ứng dụng tiếp theo, đồng thời làm giảm khả năng thực hiện chức năng mong muốn của sản phẩm cuối. Ngay cả khi quá trình biệt hóa tạo ra loại tế bào mong muốn, các tế bào tạo ra thường thiếu sự đa dạng, thiếu độ trưởng thành về chức năng và thiếu độ phức tạp về cấu trúc khi so sánh với các mô tự nhiên. Hạn chế này vẫn là một thách thức lớn trong việc tạo mô hình phát triển, nghiên cứu bệnh tật và tạo ra sản phẩm cho mục đích điều trị. TÀI LIỆU THAM KHẢO Atkeson T., et al. (2025). A novel paradigm for single-cell annotation in stem cell research. Stem Cell Reports. DOI: https://doi.org/10.1016/j.stemcr.2025.102707
23/01/2026
Tính an toàn và khả năng điều trị bệnh tim quá tải áp lực tâm thất trên mô hình khỉ của tế bào gốc người
Quá tải áp lực tâm thất là một dạng bệnh lý tim mạch nguy hiểm, xảy ra khi sức căng thành tâm thất trong quá trình tâm thu quá mức do áp lực trong tâm thất tăng cao. Các nguyên nhân chính trực tiếp gây nên hiện tượng này là tắc nghẽn dòng chảy ra (hẹp động mạch phổi, động mạch chủ), hoặc sức cản cao đối với dòng máu chảy qua mạch máu ngoại vi mà tâm thất được nối vào (tăng huyết áp phổi, tăng huyết áp toàn thân). Bệnh nhân thường bị khó chịu ở nhiều cấp độ, khó thở, hồi hộp, hầu hết đều dẫn đến suy tim, thậm chí tử vong. Ở thời điểm hiện tại, việc điều trị cục bộ là giải pháp tạm thời, bệnh nhân cần được ghép tim – tuy nhiên việc ghép tim gặp nhiều khó khăn, phức tạp nên số lượng thực hiện được chưa cao. Trong hoàn cảnh đó, cấy ghép tế bào gốc để tái tạo mô, hỗ trợ chức năng tim trở thành một hướng đi đầy hi vọng. Một nghiên cứu được thực hiện bởi các nhà khoa học Hoa Kỳ, mới đăng tải trên tạp chí Cell Transplantation đầu tháng 11/2024 cho thấy những tế bào cơ tim được tạo nên từ tế bào gốc đa tiềm năng cảm ứng ở người có thể tích hợp vào tim đang trong tình trạng quá tải áp lực tâm thất ở khỉ. Trong nghiên cứu này, liệu pháp tế bào được sử dụng như một phương pháp điều trị bổ sung cho những phương pháp chữa bệnh hiện có. Các nhà khoa học đã thu thập nguyên bào sợi từ da của người hiến, sau đó tái lập trình để tạo ra tế bào gốc đa tiềm năng cảm ứng (induced Pluripotent Stem Cells – iPSCs) rồi điều hướng để chúng biệt hóa thành các loại tế bào tương thích với cơ tim. Những tế bào này được tiêm vào tim của khỉ mang bệnh lý quá tải áp lực tâm thất. Các tế bào đã tích hợp thành công vào lớp cơ tim. Tình trạng tim và sức khỏe tổng thể được theo dõi chặt chẽ trong suốt quá trình nghiên cứu. Các cơn nhịp nhanh thất xảy ra ở 5 trong tổng số 16 động vật thí nghiệm, trong đó 2 cá thể có tốc độ nhanh liên tục, tuy nhiên hiện tượng này biến mất trong vòng 19 ngày sau khi ghép tế bào. Kết quả của nghiên cứu đã chứng minh tính an toàn và khả năng ứng dụng của liệu pháp tế bào gốc đối với bệnh quả tải áp lực tâm thất. Đây là một bước tiến đầy hứa hẹn để ứng dụng tế bào gốc trong điều trị các bệnh tim mạch trên người sau này. --------- TÀI LIỆU THAM KHẢO Scholz J., et al. (2024). Human Stem Cell–Derived Cardiomyocytes Integrate Into the Heart of Monkeys With Right Ventricular Pressure Overload. Cell Transplantation, 33, 09636897241290367.
23/01/2026

Cấy ghép các tấm organoid võng mạc từ tế bào gốc phôi người để đóng lỗ hoàng điểm trên mô hình khỉ
Hoàng điểm (điểm vàng) là một bộ phận nằm ở trung tâm của võng mạc, hình bầu dục rộng khoảng 3 mm, bao gồm tế bào gậy và tế bào nón, nơi đây là vị trí cho thị lực cao nhất giúp chúng ta có thể đọc sách, lái xe, nhìn các chi tiết nhỏ. Lỗ hoàng điểm xảy ra khi xuất hiện một vết rách nhỏ bên trong hoàng điểm, không tự liền lại và gây ảnh hưởng đến thị lực. Bệnh nhân lỗ hoàng điểm có cảm giác nhìn mờ, khi nhìn thẳng vật thể bị bẻ cong hoặc méo mó. Trong những năm qua qua, những tiến bộ trong kỹ thuật phẫu thuật đã đạt tỷ lệ đóng kín trên 90%, nhưng các trường hợp kháng trị vẫn thường xuyên được ghi nhận. Việc xử lý các lỗ hoàng điểm tái phát sau phẫu thuật là một thách thức lớn. Bên cạnh đó, ghép võng mạc đã cho thấy thành công về mặt giải phẫu, nhưng khả năng cải thiện thị lực vẫn còn hạn chế và không tránh khỏi hiện tượng khiếm khuyết trường thị giác ngoại vi. Các nhà khoa học Nhật Bản đã thử nghiệm sửa chữa thành công các lỗ hoàng điểm trên mô hình khỉ bằng cách cấy ghép các tấm organoid võng mạc có nguồn gốc từ tế bào gốc phôi người. Sau khi cấy ghép, các lỗ hoàng điểm đã đóng lại bằng cách liên tục lấp đầu không gian bằng mô võng mạc. Việc cấy ghép này đạt những kết quả tích cực khi mô ghép có thể sống sót và trưởng thành, các tế bào thụ cảm ánh sáng (tế bào gậy và tế bào nón) cũng phát triển tốt. Những thí nghiệm bổ sung cho thấy sự cải thiện về khả năng tập trung của mắt và phản ứng với ánh sáng. Tuy nhiên, các nhà khoa học cũng chỉ ra một số cảnh báo, bao gồm tình trạng thải ghép nhé, có thể hạn chế khả năng tích hợp chức năng của mô được cấy ghép. Trong nghiên cứu này, họ đã kiểm soát tình trạng thải ghép bằng cách tiêm steroid. Ngoài ra, đây chỉ là kết quả đơn lẻ và mô hình không mô phỏng chính xác bệnh lý của lỗ hoàng điểm kháng trị ở người. Các tác giả cũng cho biết cần có thêm nhiều nghiên cứu khác để kiểm tra lợi thế của võng mạc có nguồn gốc từ tế bào gốc, bao gồm cả tác dụng bảo vệ đối với tế bào võng mạc của vật chủ, và cách thức tế bào trong mảnh ghép ảnh hưởng đến chức năng thị giác. Nhóm nghiên cứu cũng có kế hoạch thử nghiệm thiết lập một số hình thức giao tiếp synap giữa vật chủ và mảnh ghép trong thời gian quan sát dài hơn hay không. Mặc dù vậy, nghiên cứu này cho thấy tiềm năng cho lớn về việc cấy ghép tế bào gốc có thể trở thành một lựa chọn điều trị thực tế, an toàn và hiệu quả với rủi ro xâm lấn tối thiểu, đặc biệt là với các trường hợp lỗ hoàng điểm khó. Kết quả nghiên cứu được đăng trên tạp chí Stem Cell Reports đầu tháng 10 năm 2024. TÀI LIỆU THAM KHẢO Iwama Y., et al. (2024). Transplantation of human pluripotent stem cell-derived retinal sheet in a primate model of macular hole. Stem Cell Reports. DOI: https://doi.org/10.1016/j.stemcr.2024.09.002
23/01/2026
Liệu pháp tế bào gốc trung mô (MSC) từ dây rốn có thể cải thiện chức năng gan ở trẻ sơ sinh bị teo đường mật
Trong cơ thể, mật là dịch tiêu hóa giúp cơ thể phân hủy và hấp thụ chất béo cùng các vitamin tan trong chất béo. Mật được sản xuất bởi gan và được vận chuyển đến ruột thông qua ống mật. Teo đường mật là tình trạng viêm và xơ hóa ở đường mật, ngăn cản dịch mật chảy từ gan xuống ruột non, khiến mật bị ứ đọng gây tổn thương gan, dẫn đến suy gan và tử vong nếu không phẫu thuật chữa khỏi. Đây là một trong những nguyên nhân phổ biến nhất gây bệnh gan mạn tính ở trẻ sơ sinh và là lý do chính khiến trẻ em phải ghép gan. Phẫu thuật Kasai là phương pháp điều trị chính cho trẻ sơ sinh bị teo đường mật bẩm sinh, được thực hiện bằng cách cắt bỏ các ống mật bị tắc và sử dụng một phần ruột non để nối trực tiếp từ gan xuống ruột, khôi phục dòng chảy của ruột. Tuy nhiên, khả năng sống sót lâu dài của gan vẫn còn hạn chế: chỉ khoảng 40% sau 10 năm, và 20-30% sau 20 năm. Nhiều nghiên cứu trước đây đã mở ra hy vọng về tiềm năng lâm sàng của liệu pháp tế bào gốc trong việc làm chậm tiến triển bệnh, cải thiện tình trạng rối loạn chức năng gan. Trong một nghiên cứu mới công bố trên Journal of Pediatric Surgery, GS. Nguyễn Thanh Liêm và cộng sự đã chứng minh tế bào gốc trung mô từ dây rốn (umbilical cord-derived mesenchymal stem cell, UC-MSC) có thể cải thiện kết quả điều trị ở trẻ sơ sinh bị teo đường mật đã trải qua phẫu thuật Kasai tiêu chuẩn. Nhóm nghiên cứu đã điều trị cho 32 trẻ sơ sinh bằng phẫu thuật Kasai (thực hiện khi 52-112 ngày tuổi), sau đó 16 trẻ được chăm sóc tiêu chuẩn, 16 trẻ được truyền UC-MSC qua động mạch gan với liều lượng 1 triệu tế bào/kg cơ thể ở giai đoạn 6,1-13 tháng tuổi. Kết quả cho thấy, sau khoảng 12 tháng kể từ khi điều trị bằng tế bào gốc, nồng độ các dấu hiệu tổn thương gan trong máu (như bilirubin huyết thanh, các men gan, albumin,…) được cải thiện đáng kể so với trẻ chỉ được chăm sóc tiêu chuẩn. Nhóm truyền UC-MSC cũng có sự giảm điểm số PELD (The Pediatric End-Stage Liver Disease), một thước đo tiêu chuẩn để theo dõi mức độ nghiêm trọng của tổn thương gan ở bệnh nhân nhi. Tỷ lệ sống sót cũng cao hơn ở nhóm được điều trị tế bào gốc sau khoảng 3 năm (tỷ lệ sống sót 100%, trong khi nhóm chăm sóc tiêu chuẩn có 2/16 trẻ tử vong do suy gan giai đoạn cuối). Liệu pháp UC-MSC cũng được chứng minh là an toàn, khi không có biến cố bất lợi nào liên quan đến truyền dịch được ghi nhận trong quá trình truyền tế bào, và các biến cố bất lợi ghi nhận được trong quá trình theo dõi ở nhóm truyền tế bào gốc cũng ít hơn đang kể so với nhóm chỉ được chăm sóc tiêu chuẩn. Những kết quả trên đã cho thấy UC-MSC có thể là một liệu pháp bổ sung tiềm năng cho phẫu thuật Kasai ở trẻ sơ sinh bị teo đường mật, với động mạch gan là con đường đưa tế bào gốc nhanh chóng, an toàn và hiệu quả vào gan. Tuy vậy, nhóm nghiên cứu nhấn mạnh cần có những nghiên cứu lớn hơn để xác nhận lợi ích của liệu pháp với nhóm bệnh nhân này, do bước đầu mới chỉ nghiên cứu trên số lượng bệnh nhân nhỏ và thiếu sự phân nhóm ngẫu nhiên. TÀI LIỆU THAM KHẢO Nguyen Thanh Liem, et al. (2025). Outcomes of allogeneic umbilical cord mesenchymal stem cell infusion for liver cirrhosis due to biliary atresia after Kasai operation. Journal of Pediatric Surgery 60(11): 162624. https://doi.org/10.1016/j.jpedsurg.2025.162624
23/01/2026

Đề xuất gỡ bỏ bài báo mới công bố về “tế bào gốc giúp làm giảm nguy cơ suy tim sau cơn đau tim” do những vấn đề nghiêm trọng liên quan đến dữ liệu
Ngày 29 tháng 10 năm 2025, tạp chí khoa học The BMJ công bố kết quả một nghiên cứu cho thấy truyền tế bào gốc trung mô tách từ lớp thạch Wharton trong dây rốn (Wharton’s jelly derived mesenchymal stem cell, WJ-MSC) vào động mạch vành trong 3-7 ngày sau cơn đau tim giúp giảm tỷ lệ suy tim và các vấn đề liên quan, cũng như cải thiện chức năng tim so với việc chỉ được điều trị tiêu chuẩn. Báo cáo này đã gợi ý về việc truyền WJ-MSC có thể là một thủ thuật bổ sung có giá trị cho những bệnh nhân trải qua cơn đau tim để ngăn ngừa suy tim, giảm nguy cơ xảy ra các biến cố tim mạch bất lợi trong tương lai. Kết quả này gây tiếng vang lớn trên các phương tiện truyền thông, trong đó tờ New Scientist gọi nghiên cứu này là “bằng chứng mạnh mẽ nhất cho thấy tế bào gốc có thể giúp tim tự phục hồi”. Bạn đọc có thể tham khảo toàn văn bài báo tại https://doi.org/10.1136/bmj-2024-083382 hoặc tóm tắt tại https://ysinhtebao.com/tbg-trung-mo/lieu-phap-msc-giup-giam-nguy-co-suy-tim-sau-nhoi-mau-co-tim. Khoảng một tuần sau khi The BMJ đăng bài, website Retraction Watch đã tổng hợp những phát hiện về sự không nhất quán trong dữ liệu, có thể ảnh hưởng nghiêm trọng đến kết quả của nghiên cứu này. Nổi bật là những bình luận của Dorothy Bishop (một nhà nghiên cứu tại Đại học Oxford, Vương quốc Anh, https://www.psy.ox.ac.uk/people/dorothy-bishop) và Nick Brown (Nghiên cứu sinh tại Đại học Groningen, Hà Lan) trên PubPeer, một trang web phi lợi nhuận cho phép người dùng bình duyệt các báo cáo khoa học sau khi xuất bản. Họ đều yêu cầu cần gỡ bỏ bài báo ngay lập tức, do những vấn đề về số liệu “không thể xảy ra ngẫu nhiên”, bao gồm một số điểm đáng chú ý như sau: - Nghiên cứu chỉ tuyển dụng bệnh nhân dưới 65 tuổi, tuy nhiên trong dữ liệu đi kèm có 127 bệnh nhân trên 65 tuổi. - Xuất hiện một “mô hình lặp lại kỳ lạ”, trong đó cứ 101 bản ghi dữ liệu thì hầu như tất cả các giá trị đều giống hệt nhau. Cân nặng của 288 trong 334 trường hợp được báo cáo đều là số nguyên và bội số của 5 (tính theo đơn vị kilogam), cũng là một dấu hiệu đáng chú ý. - Một số vấn đề về dữ liệu có thể đã được phát hiện trong quá trình bình duyệt ngang hàng (peer review), tuy nhiên dường như các tác giả đã không chia sẻ dữ liệu cho đến sau khi bình duyệt (tuy nhiên có những thông tin cho rằng dữ liệu đã được tải lên và chỉ chia sẻ với người bình duyệt, sau khi kết thúc quá trình bình duyệt thì dữ liệu mới được công khai). - Có sự xung đột lợi ích tiềm ẩn đối với tác giả Anthony Mathur, một cổ đông và là người được ủy thác của Heart Cells Foundation, tổ chức từ thiện tài trợ cho một đơn vị thực hiện liệu pháp tế bào gốc cho bệnh nhân mắc bệnh tim. - Một số vấn đề khác, bao gồm "sự khác biệt" giữa số lượng đối tượng được đăng ký (420) và số lượng bản ghi dữ liệu (360). Phản hồi những ý kiến này, tác giả liên hệ của bài báo, Armin Attar tuyên bố: nhóm tác giả đã nhận thấy một số điểm không nhất quán của dữ liệu trong quá trình kiểm tra nội bộ, và đang tiến hành đánh giá với một quá trình mất khoảng 2-3 tuần. Trong khi đó, Emma Dickinson, giám đốc quan hệ truyền thông của tạp chí The BMJ (nơi xuất bản bài báo), phát biểu: “Chúng tôi đã ghi nhận những lo ngại. BMJ rất coi trọng những cáo buộc về sự khác biệt trong dữ liệu.” Nhóm tác giả gồm 10 thành viên, trong đó 7 người đến từ Đại học Shiraz (Iran), 1 người làm việc tại Đại học Sharjah (UAE) và 2 người công tác tại Đại học Queen Mary London (Vương quốc Anh). Attar (tác giả đầu) có 5 bài báo khác bị đánh dấu, trong khi Azarpira (tác giả cuối) có tới 36 bài báo bị đánh dấu trên PubPeer vì những lo ngại về hình ảnh (trùng lặp hình ảnh trong các bài báo) và những vấn đề dữ liệu. Những ứng dụng về tế bào gốc trong điều trị các bệnh lý về tim đã từng gây nên những tranh cãi trong quá khứ. Năm 2018, Đại học Harvard và Bệnh viện Brigham and Woman's (Hoa Kỳ) đã đề nghị gỡ bỏ hơn 30 bài báo từ phòng thí nghiệm của Piero Anversa (một chuyên gia tim mạch tại trường Y Harvard), sau đó hàng chục bài trong số này đã bị tuyên bố gỡ bỏ. Cập nhật: Ngày 31/03/2026, Tạp chí BMJ chính thức rút bài báo, với lý do vẫn còn những lo ngại về độ tin cậy của thử nghiệm và tính toàn vẹn của dữ liệu, trong khi tác giả chính và cơ quan quản lý chưa thể giải quyết thỏa đáng những lo ngại đó. TÀI LIỆU THAM KHẢO https://retractionwatch.com/2025/11/06/sleuths-flag-complete-mismatch-in-data-of-bmj-stem-cell-study/ BÀI VIẾT LIÊN QUAN: - Liệu pháp tế bào gốc trung mô (MSC) giúp giảm nguy cơ suy tim sau nhồi máu cơ tim https://ysinhtebao.com/tbg-trung-mo/lieu-phap-msc-giup-giam-nguy-co-suy-tim-sau-nhoi-mau-co-tim - Chính thức: Tạp chí BMJ rút lại bài báo khoa học về nghiên cứu “tế bào gốc giúp làm giảm nguy cơ suy tim sau cơn đau tim” thực hiện tại Iran https://ysinhtebao.com/tin-tuc/bmj-rut-lai-bai-bao-ve-tbg-giup-lam-giam-nguy-co-suy-tim-sau-con-dau-tim
23/01/2026

Liệu pháp tế bào gốc trung mô (MSC) giúp giảm nguy cơ suy tim sau nhồi máu cơ tim
Thử nghiệm lâm sàng PREVENT-TAHA8 cho thấy những kết quả đáng ngạc nhiên về tiềm năng giảm nguy cơ suy tim sau nhồi máu cơ tim của MSC
23/01/2026
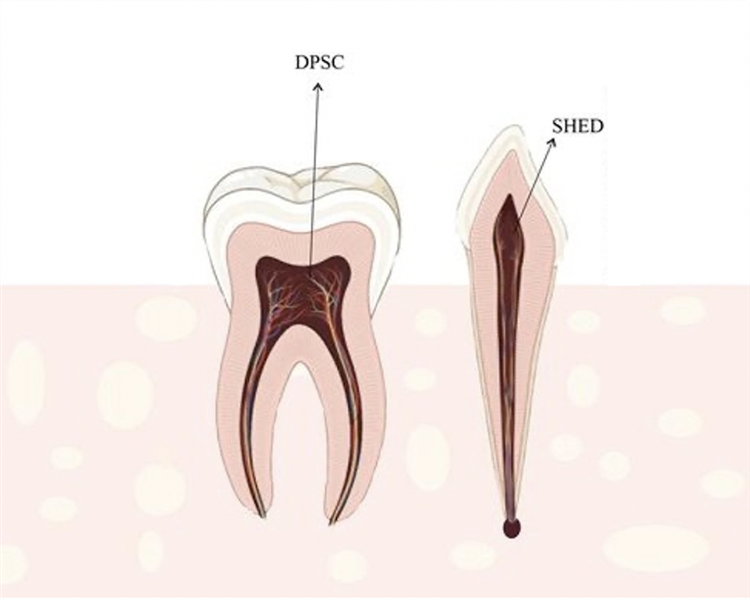
Tính đa tiềm năng và điều hòa miễn dịch của tế bào gốc tủy răng sữa
1. Tế bào gốc tủy răng sữa Tế bào gốc từ tủy răng sữa (Stem cells from human exfoliated deciduous teeth – SHED) được coi là quần thể tế bào đầy hứa hẹn cho liệu pháp tế bào và kỹ thuật mô. Đây là những tế bào gốc còn non, có khả năng tăng sinh và hình thành các loại tế bào chuyên hóa tốt hơn so với tế bào gốc từ người trưởng thành. SHED nhận được sự quan tâm lớn của các nhà nghiên cứu, nhờ quá trình thu thập mẫu răng không xâm lấn mà chỉ tận dụng rác thải sinh học của quá trình thay răng tự nhiên, đồng thời tăng sinh mạnh, biệt hóa thành nhiều loại tế bào khác nhau và có khả năng điều hòa miễn dịch. 2. Tính đa tiềm năng của tế bào gốc tủy răng sữa SHED mang các đặc điểm của tế bào gốc trung mô (Mesenchymal stem cell – MSC), nên có khả năng biệt hóa thành các loại tế bào của mô liên kết như xương, sụn, mỡ, cơ,… SHED đã được chứng minh là có khả năng biệt hóa xương cao hơn so với MSC từ các nguồn khác như mô mỡ, dây rốn, tủy xương,... Nhờ đặc tính này, SHED đã và đang được thử nghiệm nhiều trong các nghiên cứu về tái tạo xương và răng. Ví dụ, nhóm nhà khoa học Lee và cộng sự (Hàn Quốc) đã sản xuất các tấm tế bào từ SHED để ghép vào bên trong các trường hợp khe hở vòm miệng giúp tái tạo xương. Prahasanti và cộng sự cũng đã sử dụng vật liệu carbonate apatit để kết hợp với SHED thúc đẩy quá trình tái tạo xương. SHED và các tế bào gốc nha khoa khác có nguồn gốc từ tế bào mào thần kinh (Neural crest cells), nên có khả năng biệt hóa thần kinh cao hơn so với MSC từ các nguồn khác, tạo nên nguồn nguyên liệu đầy hứa hẹn cho các rối loạn thần kinh như chấn thương tủy sống, Parkinson, Alzheimer,… SHED có thể hình thành các quả cầu giống thần kinh, khi cấy vào thể vân của chuột mắc bệnh Parkinson đã cải thiện các rối loạn hành vi, bảo vệ các tế bào sản xuất dopamine và một số loại tế bào thần kinh khác trong cơ thể chuột. Bằng cách cảm ứng với nhiều chất khác nhau, các nhà khoa học đã biệt hóa in vitro được SHED thành tế bào giống thần kinh hoạch xoắn ốc, tế bào thần kinh ngoại biên, tế bào thần kinh đệm hình sao (astrocyte),… SHED cũng được sử dụng trong tái tạo nhiều loại mô khác. Yếu tố tăng trưởng nội mô mạch máu (Vascular endothelial growth factor) có thể kích thích SHED biệt hóa nội mô – sinh mạch, thúc đẩy quá trình tái tạo mạch máu. SHED cũng có thể biệt hóa thành tế bào gan, tế bào ống đường mật, tế bào beta tiết insulin, tế bào thụ cảm ánh sáng võng mạc. 3. Khả năng điều hòa miễn dịch SHED và các tế bào gốc nha khoa khác có thể tương tác với vi môi trường viêm để điều hòa miễn dịch tại chỗ. Nhiều nghiên cứu cho thấy môi trường điều kiện hóa không huyết thanh của SHED (serum-free conditioned media of SHED, SHED-CM) hoặc các thể tiết ngoại bào (extracellular vesicle, EV) có chức năng điều hòa các tế bào hoặc mô khác, cho thấy liệu pháp không sử dụng trực tiếp tế bào là một chiến lược hiệu quả trong y học tái tạo. Nhiều nghiên cứu đã sử dụng SHED-CM để điều trị thoái hóa khớp, viêm võng mạc sắc tố, Parkinson, tái tạo xương, … SHED-EV được thử nghiệm trong điều trị viêm nha chu, lupus ban đỏ hệ thống, chống viêm sụn khớp thái dương hàm,… Với tác dụng điều biến các tế bào miễn dịch, SHED, SHED-CM và SHED-EV đã có tác dụng tích cực với nhiều bệnh toàn thân như Alzheimer, suy gan cấp, xơ gan, tổn thương thận cấp, trẻ hóa da,… Như vậy, nhờ việc được thu từ nguồn mô không xâm lấn và khả năng tinh mạnh mẽ, SHED đang trở thành một nguồn nguyên liệu đầy hứa hẹn cho liệu pháp tế bào. Đặc tính đa tiềm năng và khả năng điều hòa miễn dịch đã thúc đẩy chúng tham gia nhiều hơn trong các thử nghiệm điều trị bệnh. Liệu pháp tế bào dựa trên SHED có thể sử dụng trực tiếp tế bào, hay sử dụng môi trường cảm ứng (SHED-CM) và thể tiết ngoại bào (SHED-EV), đều mang lại những tín hiệu đầy hứa hẹn. Tuy nhiên, các cơ chế hoạt động của quá trình biệt hóa cần được nghiên cứu sâu hơn để có thể đưa liệu pháp dựa trên SHED trở thành hiện thực lâm sàng. TÀI LIỆU THAM KHẢO 1. Rosa V., et al. (2016). Pluripotency of stem cells from human exfoliated deciduous teeth for tissue engineering. Stem Cells International, 2016(1), 5957806. https://doi.org/10.1155/2016/5957806 2. Guo R., and Yu J. (2022). Multipotency and immunomodulatory benefits of stem cells from human exfoliated deciduous teeth. Frontiers in Dental Medicine, 3, 805875. https://doi.org/10.3389/fdmed.2022.805875
23/01/2026







