TẾ BÀO GỐC TẠO MÁU

“Bệnh nhân Oslo” – trường hợp tiếp theo được chữa khỏi HIV nhờ ghép tế bào gốc
Người đàn ông Na Uy là trường hợp tiếp theo trong số ít những người được xác định chữa khỏi HIV nhờ ghép tế bào gốc, và là trường hợp đầu tiên trong số này được ghép tủy xương từ người thân trong gia đình.
17/04/2026

Chỉnh sửa vùng khởi động của gen HBG1 và HBG2 trên tế bào gốc tạo máu để điều trị bệnh thiếu máu hồng cầu hình liềm
Thử nghiệm lâm sàng RUBY (https://clinicaltrials.gov/study/NCT04853576) cho thấy phương pháp điều trị đầy hứa hẹn bằng cách chỉnh sửa gen trên tế bào gốc tạo máu đối với bệnh hồng cầu hình liềm, một rối loạn di truyền có rất ít lựa chọn chữa khỏi.
06/04/2026

Marne-Cel - liệu pháp tế bào gốc chỉnh sửa gen được FDA phê duyệt nhanh để điều trị hội chứng thiếu hụt sự bám dính bạch cầu loại I (LAD-I)
Ngày 26/03/2026, FDA đã phê duyệt marnetegragene autotemcel (marne-cel, tên thương mại: Kresladi, sản phẩm của hãng Rocket Pharmaceuticals) để điều trị hội chứng thiếu hụt sự bám dính bạch cầu loại I nghiêm trọng ở bệnh nhân nhi không thể ghép tế bào gốc tạo máu đồng loại.
30/03/2026
FDA phê duyệt liệu pháp tế bào gốc tạo máu chỉnh sửa gen đầu tiên cho hội chứng Wiskott-Aldrich.
Trong thông cáo báo chí ngày 09 tháng 12 năm 2025 của Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (The U.S. Food and Drug Administration, US FDA), đơn vị này đã công bố phê duyệt Waskyra (etuvetidigene autotemcel), liệu pháp gen dựa trên tế bào đầu tiên để điều trị hội chứng Wiskott-Aldrich. Waskyra được chỉ định cho bệnh nhi từ 6 tháng tuổi trở lên và người lớn mắc hội chứng Wiskott-Aldrich có đột biến gen WAS, những người có thể ghép tế bào gốc tạo máu (hematopoietic stem cell – HSC) nhưng không có người hiến phù hợp về kháng nguyên bạch cầu người (human leukocyte antigen – HLA). Hội chứng Wiskott-Aldrich (Wiskott-Aldrich syndrome, WAS) là một rối loạn di truyền hiếm gặp của hệ thống tạo máu do đột biến gen WAS trên nhiễm sắc thể giới tính X gây ra, hầu như chỉ xảy ra ở nam giới với tỷ lệ mắc khoảng 1/250.000 nam giới. Bệnh thường biểu hiện ở trẻ em với các triệu chứng nhiễm trùng tái phát, chảy máu, chàm và tăng nguy cơ mắc bệnh tự miễn và u lympho. Việc điều trị bệnh chủ yếu là kiểm soát triệu chứng và ngăn ngừa biến chứng, phương pháp duy nhất có thể chữa khỏi là ghép tế bào gốc tạo máu đồng loại, nhưng tiềm ần nhiều rủi ro và cần người hiến tặng phù hợp. Waskyra bao gồm các tế bào gốc tạo máu của chính bệnh nhân, đã được cải biến di truyền để mang các bản sao chức năng của gen WAS, sau đó được truyền tĩnh mạch để phục hồi quá trình sản xuất tế bào máu, nhờ đó giải quyết nguyên nhân gốc rễ của bệnh. Tính an toàn và hiệu quả của Waskyra được đánh giá dựa trên một nghiên cứu lâm sàng đa quốc gia, nhãn mở, đơn nhóm với 10 bệnh nhân WAS 1-9 tuổi, và một chương trình tiếp cận mở rộng với 17 bệnh nhân WAS 1-35 tuổi. Kết quả cho thấy lợi ích lâm sàng đáng kể và bền vững cho bệnh nhân, bao gồm sự giảm đáng kể các biểu hiện bệnh chính gây ra bệnh tật và tử vong. Tỷ lệ nhiễm trùng nặng giảm 93% trong giai đoạn từ 6 đến 18 tháng sau điều trị so với tỷ lệ 12 tháng trước điều trị. Các biến cố chảy máu từ trung bình đến nặng giảm 60% trong 12 tháng đầu sau điều trị so với 12 tháng trước điều trị. Hầu hết bệnh nhân không ghi nhận hiện tượng chảy máu từ trung bình đến nặng sau 4 năm điều trị. Các tác dụng phụ thường gặp nhất liên quan đến Waskyra bao gồm phát ban, nhiễm trùng đường hô hấp, giảm bạch cầu hạt kèm sốt, nhiễm trùng liên quan đến ống thông, nôn mửa, tiêu chảy, tổn thương gan và xuất huyết dưới da. Sự chấp thuận của FDA dành cho liệu pháp này là một cột mốc mang tính đột phá, đáp ứng nhu cầu cấp thiết cho những bệnh nhân WAS, những người đã cho rằng họ có “một cuộc sống đầy lo lắng và sợ hãi kinh hoàng” mà không có bất kỳ liệu pháp điều trị nào được phê duyệt. Trong quá trình xem xét cấp phép cho Waskyra, FDA đã thể hiện sự linh hoạt về quy định phù hợp trên 4 lĩnh vực quan trọng: các vấn đề liên quan đến bệnh hiếm gặp (WAS chỉ gặp ở khoảng 1/250.000 nam giới), thiết kế thử nghiệm (không yêu cầu nhóm chứng do số lượng bệnh nhân rất ít), cơ chế tác dụng rõ ràng, quy tình sản xuất và kiểm soát. Điều này cho phép phê duyệt kịp thời các sản phẩm cho các bệnh hiếm gặp, nghiêm trọng, đe dọa tính mạng, đồng thời cân bằng cẩn thận các yêu cầu dữ liệu trước phê duyệt với các cam kết sau khi đưa sản phẩm ra thị trường. Đây là sản phẩm liệu pháp tế bào và gen đầu tiên được FDA phê duyệt từ một tổ chức phi lợi nhuận, với nhà phát triển là Fondazione Telethon ETS có trụ sở tại Italy. Sản phẩm Waskyra cũng được Cơ quan Dược phẩm Châu Âu (European Medicines Agency, EMA) khuyến nghị cấp phép lưu hành tại Liên minh Châu Âu (the European Union, EU). TÀI LIỆU THAM KHẢO 1. Thông cáo báo chí ngày 09 tháng 12 năm 2025 của Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ về việc phê duyệt phương pháp điều trị gen đầu tiên cho hội chứng Wiskott-Aldrich https://www.fda.gov/news-events/press-announcements/fda-approves-first-gene-therapy-treatment-wiskott-aldrich-syndrome 2. Bản tin ngày 14 tháng 11 năm 2025 của Cơ quan Dược phẩm Châu Âu về liệu pháp gen đầu tiên điều trị hội chứng hiếm gặp Wiskott-Aldrich https://www.ema.europa.eu/en/news/first-gene-therapy-treat-rare-disease-wiskott-aldrich-syndrome
24/01/2026

FDA phê duyệt liệu pháp tế bào đầu tiên điều trị bệnh thiếu máu bất sản nặng.
Thiếu máu bất sản (aplastic anemia) là một hội chứng suy tủy xương đặc trưng bởi giảm toàn bộ các tế bào máu ngoại vi và giảm sản tủy xương, dẫn đến cơ thể mệt mỏi, suy giảm miễn dịch nên dễ nhiễm trùng, chảy máu không kiểm soát. Bệnh thiếu máu bất sản nặng hoặc rất nặng là một trường hợp cấp cứu huyết học và cần được điều trị kịp thời. Các dạng thiếu máu bất sản được biết đến nhiều như hội chứng thiếu máu Fanconi, loạn sản sừng bẩm sinh, thiếu máu bất sản gia đình, hội chứng giảm tiểu cầu kèm mất xương quay,… Đầu tháng 12 năm 2025, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (The U. S. Food and Drug Administration – US FDA) đã phê duyệt omidubicel-onlv (tên thương mại: Omisirge, nhà sản xuất: Gamida Cell Ltd.) là liệu pháp cấy ghép tế bào gốc tạo máu đầu tiên dành cho bệnh nhân mắc bệnh thiếu máu bất sản nặng (severe aplastic anemia - SAA). Omidubicel-onlv là liệu pháp tế bào gốc tạo máu đồng loại có nguồn gốc từ máu dây rốn, năm 2023 đã được phê duyệt điều trị cho người lớn và trẻ em từ 12 tuổi trở lên mắc bệnh ác tính về huyết học, dự kiến được ghép tế bào gốc máu dây rốn nhằm giảm nguy cơ nhiễm trùng cũng như rút ngắn thời gian phục hồi bạch cầu trung tính sau khi điều trị bằng phương pháp hủy tủy. Gần đây, FDA chấp thuận chỉ định thêm cho người lớn và trẻ em từ 6 tuổi trở lên mắc bệnh thiếu máu bất sản nặng sau khi điều trị bằng phương pháp giảm cường độ mà không tìm được người hiến tế bào gốc tương thích. Sự phê duyệt này được cấp sau quá trình xem xét ưu tiên, dựa trên kết quả thử nghiệm lâm sàng giai đoạn I/II nhãn mở, đơn trung tâm đang diễn ra trên bệnh nhân thiếu máu bất sản nặng (mã số NCT03173937), trong đó Omidubicel đã giúp phục hồi bạch cầu trung tính sớm và bền vững ở 12/14 bệnh nhân nghiên cứu, với thời gian phục hồi trung bình là 11 ngày. Mới đây nhất, các kết quả cập nhật được trình bày tại cuộc họp thường niên của Hiệp hội Huyết học Hoa Kỳ ngày 08/12/2025 thấy 18/19 bệnh nhân có tuổi trung bình 20 tuổi đã phục hồi bạch cầu trung tính trong vòng trung bình 8 ngày, tỷ lệ sống sót không bệnh và tỷ lệ sống sót tổng thể đều đạt 94%, chỉ có 16% mắc bệnh ghép chống chủ (Graft versus Host Disease – GvHD) cấp tính độ II, không có trường hợp nào mắc GvHD cấp tính nghiêm trọng hoặc mạn tính. Sự phê duyệt này cho thấy bước tiến đáng kể trong việc lựa chọn điều trị cho những bệnh nhân huyết học. Cấy ghép tế bào gốc mang lại tiềm năng chữa khỏi bệnh thiếu máu bất sản, nhưng nhiều bệnh nhân không tìm được người hiến phù hợp. Sản phẩm Omidubicel có thể cung cấp phương pháp điều trị thay thế cho những bệnh nhân này, với độ an toàn và hiệu quả cao. Các tác dụng phụ thường gặp nhất liên quan đến Omidubicel bao gồm giảm bạch cầu hạt kèm sốt, nhiễm trùng do virus và vi khuẩn, tăng đường huyết, giảm tiểu cầu miễn dịch, viêm phổi, và tình trạng giảm tế bào máu tự miễn đã xảy ra ở khoảng 25% bệnh nhân. NGUỒN https://www.medscape.com/viewarticle/fda-oks-first-cell-therapy-severe-aplastic-anemia-2025a1000yfl TÀI LIỆU THAM KHẢO 1. Danh mục sản phẩm Liệu pháp tế bào và gen được FDA cấp phép https://www.fda.gov/vaccines-blood-biologics/cellular-gene-therapy-products/approved-cellular-and-gene-therapy-products 2. Thông tin thử nghiệm lâm sàng NCT03173937 https://clinicaltrials.gov/study/NCT03173937 3. Thông cáo báo chí ngày 08/12/2025 cập nhật kết quả thử nghiệm NCT03173937 https://www.gamida-cell.com/press_release/additional-positive-results-for-omidubicel-in-treating-severe-aplastic-anemia-presented-at-ash/
24/01/2026
Ghép tế bào gốc tạo máu đồng loại: người hiến trẻ tuổi mặc dù không cùng huyết thống nên được ưu tiên hơn người hiến cùng huyết thống nhưng lớn tuổi
Các nhà nghiên cứu đã chứng minh rằng tuổi người hiến đóng vai trò quan trọng trong sự thành công của ghép tế bào gốc tạo máu đồng loại.
24/01/2026
Liệu pháp tế bào gốc chỉnh sửa gen cho bệnh lý huyết sắc tố
Chỉnh sửa tế bào gốc tạo máu sau đó ghép cho bệnh nhân được xác nhận là phương pháp điều trị hiệu quả cho bệnh lý huyết sắc tố.
24/01/2026
Kết quả cấy ghép tế bào gốc tạo máu ở 813 bệnh nhi thiếu máu Fanconi
Thiếu máu Fanconi là một bệnh di truyền hiếm gặp, không đồng nhất về mặt di truyền và lâm sàng, đặc trưng bởi các bất thường bẩm sinh và mắc phải, suy tủy xương và tăng nguy cơ mắc các bệnh ác tính. Thiếu máu Fanconi được công nhận là nguyên nhân phổ biến nhất gây ra suy tủy xương (bone marrow failure – BMF) di truyền hoặc thiếu máu bất sản (aplastic anemia – AA), có liên quan chặt chẽ với sự xuất hiện các bất thường tiền ác tính và có thể chuyển thành hội chứng loạn sản tủy (myelodysplastic syndrome – MDS) và bệnh bạch cầu dòng tủy cấp tính (acute myeloid leukemia – AML). Ghép tế bào gốc tạo máu (hematopoietic stem cell transplantation – HSCT) đồng loại được xác định là lựa chọn điều trị duy nhất cho bệnh nhân thiếu máu Fanconi liên quan đến BMF/AA và AML/MDS. Trong một báo cáo đăng trên tạp chí Blood (tạp chí thuộc Hiệp hội Huyết học Hoa Kỳ – American Society of Hematology – ASH), một nhóm nghiên cứu đã tiến hành phân tích hồi cứu đa trung tâm, trên 813 trẻ em mắc thiếu máu Fanconi ở 137 trung tâm, được ghép tế bào gốc tạo máu lần đầu trong giai đoạn năm 2010 – 2018, với 778 chỉ định suy tủy xương/thiếu máu bất sản (BMF/AA) và 35 chỉ định bệnh bạch cầu dòng tủy cấp tính/hội chứng loạn sản tủy (AML/MDS). Một số kết quả chính: - Thời gian mọc mảnh ghép (engraftment) trung bình với bạch cầu trung tính là 15 ngày, tỷ lệ tích lũy phục hồi bạch cầu trung tính ngày thứ 100 là 95%; thời gian mọc mảnh ghép trung bình với tiểu cầu là 20 ngày, tỷ lệ tích lũy phục hồi tiểu cầu ngày thứ 100 là 88%. - Tỷ lệ ghép thất bại (graft failure) nguyên phát là 2% (n = 17), thứ phát là 3% (n = 21). - Tỷ lệ sống tổng thể (overall survival – OS) sau 1 năm là 87%, sau 5 năm là 83%. OS thấp hơn đáng kể ở nhóm bệnh nhân ≥10 tuổi và nhóm ghép do AML/MDS so với các nhóm đối lập. OS tương đương giữa nhóm có người hiến phù hợp cùng hoặc không cùng huyết thống, đồng thời cao hơn nhóm có người hiến không phù hợp cùng hoặc không cùng huyết thống. - Tỷ lệ sống không biến cố (Event-free survival – EFS) sau 1 năm là 82%, sau 5 năm là 78%, cũng bị ảnh hưởng bởi các yếu tố tương tự như OS. - Tỷ lệ sống không GvHD và không tái phát (GVHD-free, relapse-free survival – GRFS) sau 1 năm là 73%, sau 5 năm là 70%, cũng bị ảnh hưởng bởi các yếu tố tương tự như OS và EFS. - Tổng cộng 123 ca tử vong trong quá trình theo dõi, với 93 trường hợp (76%) tử vong liên quan đến ghép: bệnh mảnh ghép chống chủ (Graft-versus-host disease – GvHD) n = 40 (33%), nhiễm trùng n = 34 (28%), suy cơ quan n = 7 (6%), tái phát n = 14 (11%),… - Bệnh mảnh ghép chống chủ (GvHD): tỷ lệ tích lũy GvHD cấp tính vào ngày thứ 100 sau ghép ở độ 2 – 4 là 23%, độ 3 – 4 là 12%, tỷ lệ tích lũy GvHD mạn tính sau 1 năm là 8%, sau 5 năm là 12%. - 16 bệnh nhân (2%) phát triển bệnh ác tính thứ phát (bệnh bạch cầu, hội chứng loạn sản tủy, bệnh u lympho,…) là điểm thường thấy ở bệnh nhân thiếu máu Fanconi. - Ảnh hưởng của liệu pháp huyết thanh: trong 441 bệnh nhân có người hiến phù hợp cùng huyết thống, các bệnh nhân sử dụng alemtuzumab có OS, EFS, GRFS cao hơn và tỷ lệ mắc GvHD thấp hơn, các bệnh nhân không sử dụng liệu pháp huyết thanh có OS, EFS, GRFS kém hơn và tỷ lệ mắc GvHD cao hơn (nhóm còn lại sử dụng Antithymocyte Globulin – ATG). Những dữ liệu này củng cổ thêm vai trò của ghép tế bào gốc tạo máu trong điều trị thiếu máu Fanconi, điển hình là các bệnh nhân suy tủy xương/thiếu máu bất sản (BMF/AA) và bệnh bạch cầu dòng tủy cấp tính/hội chứng loạn sản tủy (AML/MDS). Bệnh nhân nên được ghép sớm (<10 tuổi) nếu tìm được người hiến phù hợp, với người hiến phù hợp có hoặc không có quan hệ huyết thống, sử dụng alemtuzumab,… là một số yếu tố giúp tăng tỷ lệ thành công, giảm nguy cơ GvHD của ca ghép. Bệnh nhân thiếu máu Fanconi dường như có nguy cơ ung thư không thay đổi sau ghép tế bào gốc, dữ liệu này cần theo dõi lâu hơn để có đánh giá đầy đủ. TÀI LIỆU THAM KHẢO Lum S. H., et al. (2024). Outcomes of hematopoietic stem cell transplantation in 813 pediatric patients with Fanconi anemia. Blood, 144(12), 1329-1342. DOI: https://doi.org/10.1182/blood.2023022751
24/01/2026
Thảo luận về Orca-T, một liệu pháp tế bào mới có thể thay ghế ghép tế bào gốc tạo máu đồng loại (alloHSCT)
Ghép tế bào gốc tạo máu (Hematopoietic Stem Cell Transplantation – HSCT) là quá trình đưa các tế bào gốc tạo máu (HSC) (thường lấy từ tủy xương, máu ngoại vi hoặc máu cuống rốn) để nhân lên trong cơ thể bệnh nhân và sản xuất các tế bào máu bình thường. HSCT thường được thực hiện cho những bệnh nhân mắc một số bệnh về máu hoặc tủy xương, như đa u tủy xương, bệnh bạch cầu dòng tủy/dòng lympho cấp tính/mạn tính, một số loại u lympho,… HSCT có thể là tự thân (autologous HSCT – autoHSCT) trong đó sử dụng tế bào gốc của chính bệnh nhân, hoặc đồng loại (allogeneic HSCT – alloHSCT) với việc sử dụng tế bào gốc của người hiến, đôi khi một số tài liệu còn chia thêm nhóm “đồng gen” (syngeneic HSCT) là trường hợp sử dụng tế bào gốc của anh chị em song sinh cùng trứng. Trong thực hành alloHSCT, biến chứng nghiêm trọng được quan tâm nhất là bệnh mảnh ghép chống chủ (graft versus host disease – GvHD), xảy ra khi các tế bào lympho T có khả năng miễn dịch từ mô ghép của người hiến nhận diện các mô của người nhận là tác nhân lạ, và bắt đầu phản ứng miễn dịch chống lại chúng, dẫn đến tổn thương mô ở nhiều cơ quan khác nhau. GvHD có thể chia thành nhiều loại với những đặc điểm và chiến lược theo dõi, điều trị khác nhau: GvHD cấp tính cổ điển (xuất hiện trong vòng 100 ngày sau khi ghép với các triệu chứng lâm sàng điển hình của bệnh GVHD cấp tính); GVHD cấp tính dai dẳng, tái phát hoặc khởi phát muộn (biểu hiện các triệu chứng lâm sàng của GVHD cấp tính cổ điển nhưng sau 100 ngày kể từ ngày ghép); GvHD mạn tính cổ điển (xuất hiện sau 100 ngày ghép với các đặc điểm lâm sàng cổ điển của bệnh GVHD mạn tính), hội chứng chồng chéo (có thể xảy ra bất cứ lúc nào sau khi ghép với các đặc điểm của cả GVHD cấp tính và mạn tính). Trong nỗ lực hạn chế GvHD khi ghép đồng loại, Orca Bio đã phát triển liệu pháp Orca-T, được tạo ra từ các tế bào T điều hòa, tế bào gốc CD34+ và tế bào T thông thường thu nhận từ máu ngoại vi của người hiến phù hợp. Liệu pháp này đang được đánh giá trong thử nghiệm lâm sàng giai đoạn 3 Precision-T (NCT05316701) để đánh giá tính an toàn, hiệu quả và khả năng dung nạp so với alloHSCT thông thường ở những bệnh nhân mắc bệnh bạch cầu tủy cấp tính (AML), bệnh bạch cầu lympho cấp tính (ALL), hội chứng loạn sản tủy nguy cơ cao (MDS) và bệnh bạch cầu cấp tính kiểu hình hỗn hợp (MPAL). Trong một cuộc thảo luận trên OncLive, các khách mời là những nhà khoa học uy tín đã đưa ra những quan điểm về liệu pháp Orca-T, với những tính năng chính như: sự suy giảm tế bào T của người hiến giúp giảm thiểu nguy cơ mắc GVHD trong khi vẫn duy trì hiệu quả điều trị, phương pháp tiếp cận được cải biến để tăng cường khả năng mọc mảnh ghép và giảm các biến chứng do miễn dịch. Sử dụng Orca-T, bệnh nhân chỉ cần dùng một loại thuốc ức chế miễn dịch duy nhất là Tacrolimus thay vì dùng hỗn hợp nhiều thuốc như alloHSCT, giúp giảm độc tính liên quan đến các phác đồ ức chế miễn dịch rộng, đồng thời kiểm soát các phản ứng miễn dịch tốt hơn. Xem chi tiết bài thảo luận tại https://www.onclive.com/view/orca-t-a-new-allogeneic-cell-therapy---defining-orca-t-and-potential-advantages-compared-with-conventional-allohsct
24/01/2026
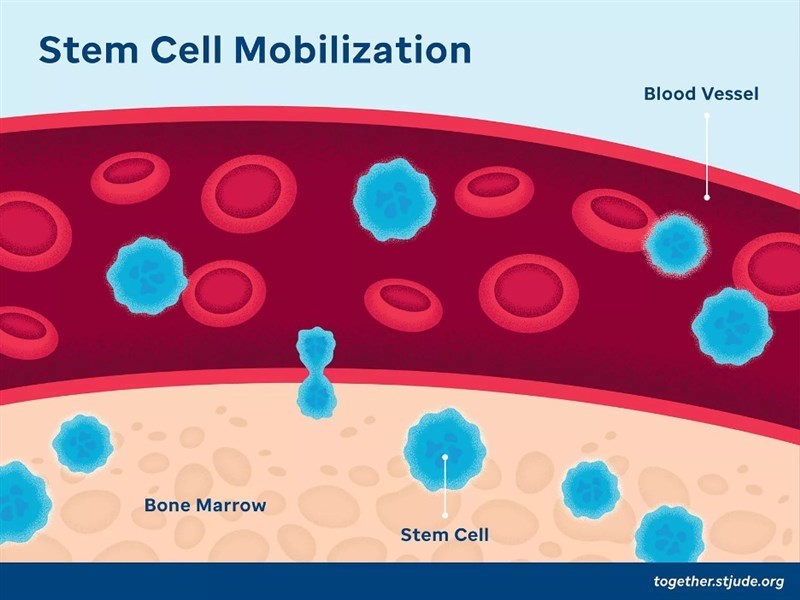
Cách thức mới để hoạt hóa tế bào gốc tạo máu tủy xương – cơ hội huy động tế bào gốc một cách hiệu quả và an toàn phục vụ cho cấy ghép
Tế bào gốc tạo máu (Hematopoietic stem cell – HSC) là những tế bào chưa trưởng thành, có vai trò tái tạo các tế bào máu trong cơ thể. Chúng thường tồn tại ở trạng thái nghỉ, phân chia chậm, nhưng khi có tín hiệu kích hoạt sẽ chuyển sang trạng thái hoạt động, nhân lên nhanh chóng và biệt hóa thành các tế bào chức năng. Ghép HSC giúp bổ sung tế bào máu và tế bào miễn dịch cho người bệnh, là yếu tố quan trọng trong điều trị nhiều bệnh lý huyết học như bệnh bạch cầu dòng tủy/dòng lympho cấp tính/mạn tính, u lympho Hodgkin/không Hodgkin, đa u tủy xương, tan máu bẩm sinh, thiếu máu hồng cầu hình liềm,… Trong một nghiên cứu mới công bố cuối tháng 02/2025 trên tạp chí Nature Immunology trên mô hình chuột, các nhà khoa học đã phát hiện ra một loại protein điều hòa phiên mã DNA có tên là FLI-1 có vai trò quan trọng trong quá trình tái tạo HSC ở tủy xương và huy động để di chuyển vào máu. Khi vắng mặt yếu tố này, HSC ở trạng thái tĩnh và ít tương tác với các tế bào tủy xung quanh, đặc biệt là các tế bào nội mô tạo nên mạch máu. Ngược lại, hoạt động của FLI-1 khôi phục sự tương tác và tăng khả năng thích ứng của HSC với hốc tế bào nội mô, thúc đẩy chúng vào trạng thái hoạt hóa, cải thiện đáng kể khả năng tăng sinh và phục hồi nguồn HSC ở vật chủ mới (là người nhận đối với trường hợp ghép HSC). Thậm chí, các đột biến gây ra hoạt động quá mức của FLI-1 là tác nhân gây ra một số bệnh bạch cầu. Việc sản xuất tạm thời FLI-1 trong các tế bào gốc tủy xương đang ở trạng thái nghỉ sẽ kích hoạt những tế bào này nhanh chóng tăng số lượng, giúp tăng cơ hội cấy ghép thành công. Các nhà nghiên cứu đã phát triển phương pháp sử dụng mRNA (tương tự như vaccine RNA) để kích thích HSC bằng FLI-1 chỉ trong vài ngày, nên không xảy ra tình trạng tăng sinh mất kiểm soát, không gây ung thư. Họ cũng chứng minh được rằng HSC từ máu cuống rốn có tiềm năng tái tạo lớn hơn HSC từ máu ngoại vi có liên quan đến mức độ hoạt động của FLI-1. Đồng thời, mối quan hệ giữa HSC và môi trường xung quanh trong tủy xương (đặc biệt là hốc mạch máu) cũng được làm rõ: hoạt động của tế bào gốc không do chúng tự quyết định, cũng không được xác định hoàn toàn bởi các tín hiệu hốc mạch của tế bào nội mô, mà phụ thuộc vào tín hiệu và khả năng thích ứng giữa hai yếu tố này. Nhóm nghiên cứu có kế hoạch tiếp tục phát triển những thử nghiệm tiền lâm sàng trong đó sử dụng mRNA đã được chỉnh sửa để đưa FLI-1 tạm thời vào HSC, với mục tiêu cuối cùng là thử nghiệm lâm sàng trên bệnh nhân. Phương pháp tiếp cận này có thể mở đường cho việc điều trị nhiều bệnh lý huyết học cần ghép HSC với hiệu quả ổn định, lâu dài và an toàn. TÀI LIỆU THAM KHẢO Itkin T., et al. (2025). Transcriptional activation of regenerative hematopoiesis via microenvironmental sensing. Nature Immunology, 1-13. DOI: https://doi.org/10.1038/s41590-025-02087-w
24/01/2026
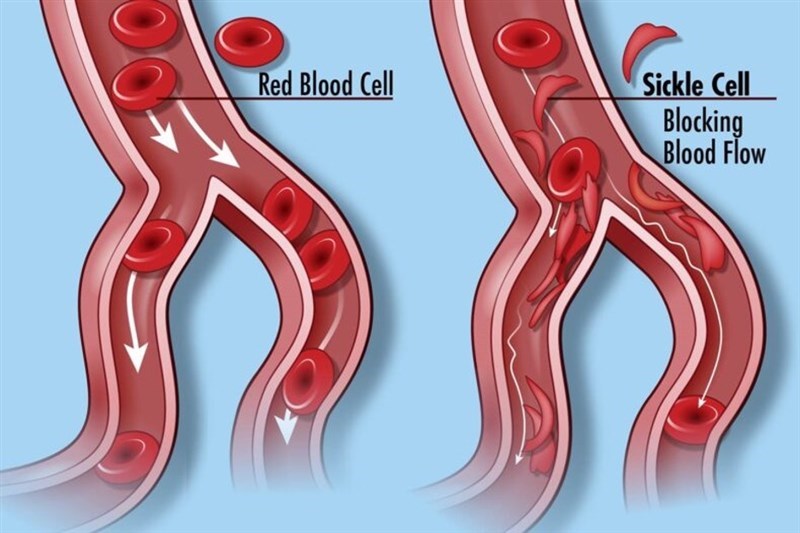
Hiệu quả điều trị bệnh hồng cầu hình liềm bằng phương pháp ghép tủy xương từ người hiến “phù hợp một nửa” (haploidentical)
Bệnh hồng cầu hình liềm (hay thiếu máu hồng cầu hình liềm – Sickle cell anemia) là một dạng thiếu máu di truyền do đột biến gen sản xuất hemoglobin – hợp chất không thể thiếu trong cấu trúc hồng cầu, dẫn đến không có đủ các tế bào hồng cầu khỏe mạnh để vận chuyển oxy trong cơ thể. Khác với người bình thường có các tế bào hồng cầu hình đĩa và linh hoạt, trong cơ thể người bệnh hồng cầu hình liềm, các tế bào hồng cầu trở nên cứng, dính và có hình dạng giống như lưỡi liềm hoặc mặt trăng khuyết, chúng không vận chuyển được oxy, đồng thời dễ bị mắc kẹt trong mạch máu làm chậm hoặc ngăn chặn các hồng cầu khác mang oxy đến các bộ phận của cơ thể. Liệu pháp tế bào và chỉnh sửa gen được kỳ vọng có thể điều trị bệnh một cách hiệu quả, trong đó một số sản phẩm đã được cấp phép chính thức, ví dụ Lyfgenia (lovotibeglogene autotemcel) và Casgevy (exagamglogene autotemcel) được FDA Hoa Kỳ phê duyệt cuối năm 2023. Theo một thử nghiệm được hoàn thành tại Anh mới đây, một quy trình cấy ghép tủy xương đã được chứng minh là an toàn và có thể chữa khỏi bệnh cho bệnh nhân mắc hồng cầu hình liềm, với chi phí thấp hơn so với các sản phẩm liệu pháp chỉnh sửa gen. Kết quả thử nghiệm mới được đăng tải trên tạp chí NEJM Evidence cuối tháng 02/2025. Đây là một thử nghiệm lâm sàng đa trung tâm giai đoạn II (mã số NCT03263559), nhãn mở, thử nghiệm phương pháp ghép tủy xương đơn bội cường độ giảm. Ghép tủy xương cung cấp cho bệnh nhân các tế bào gốc tạo máu được lấy từ người hiến khỏe mạnh, những tế bào này sẽ tạo ra những tế bào máu bình thường không mang đột biến gây ra hồng cầu hình liềm. Tủy xương được lấy từ người hiến tặng "phù hợp một nửa” (haploidentical) về các dấu hiệu miễn dịch với bệnh nhân để hạn chế sự đào thải miễn dịch, ví dụ như cha mẹ, con cái, anh chị em ruột, cháu trai/cháu gái, chú dì hoặc anh chị em họ của bệnh nhân. Điều này có nghĩa là các yếu tố miễn dịch có mặt và hoạt động trên các tế bào tủy của người hiến phải phù hợp với ít nhất một nửa các yếu tố đó trên các tế bào của người nhận. Trong số 54 người tham gia nghiên cứu (độ tuổi từ 15,5 đến 43,2), có 42 người được ghép tủy xương, trước khi ghép được hóa trị liều thấp và xạ trị toàn thân, sau ghép được dùng cyclophosphamide và một số loại thuốc khác (mycophenolate mofetil, sirolimus, fludarabine,…) để tránh mảnh ghép chống chủ (GvHD). Kết quả cho thấy sau 2 năm điều trị, 95% bệnh nhân vẫn còn sống sót, với 88% bệnh nhân sống sót không có biến cố bất lợi (chỉ có 2 người bị suy ghép nguyên phát, 1 người bị suy ghép thứ phát). Tỷ lệ mắc GvHD cấp tính độ 3-4 vào ngày 100 chỉ là 4,8%, trong khi tỷ lệ GvHD mạn tính sau 2 năm là 22,4%. Có 2 trong số 4 trường hợp tử vong được xác định do biến chứng nhiễm trùng sớm. Những kết quả trên chứng minh phương pháp này có tỷ lệ thành công rất cao, tương đương hoặc tốt hơn những sản phẩm liệu pháp gen đã được phê duyệt. Các nhà nghiên cứu cũng thực hiện so sánh phương pháp này và liệu pháp gen. Phương pháp ghép tủy xương có thể áp dụng với hầu hết các bệnh nhân hồng cầu hình liềm, trong khi liệu pháp gen đòi hỏi bệnh nhân cần trải qua hóa trị liều cao, có nguy cơ tổn thương một số cơ quan đích hoặc nguy cơ mắc bệnh bạch cầu, nên nhiều người không đủ điều kiện thực hiện. Một ca ghép tủy chỉ yêu cầu bệnh nhân nằm viện khoảng 8 ngày, còn đối với liệu pháp gen là 6-8. Số lần truyền máu trung bình sau khi ghép tủy xương là 6, thấp hơn nhiều con số 50 lần khi điều trị bằng liệu pháp gen. Tổng chi phí cho một ca ghép tủy xương thấp hơn 4-6 lần so với một ca điều trị bằng liệu pháp gen. Đây là một tín hiệu rất tích cực trong điều trị bệnh hồng cầu hình liềm, với tỷ lệ thành công cao, an toàn, chi phí thấp. Đồng thời, bệnh nhân được tăng cơ hội điều trị do không cần tìm người hiến hoàn toàn phù hợp miễn dịch mà chỉ cần cấy ghép phù hợp một nửa. TÀI LIỆU THAM KHẢO Kassim A. A., et al. (2025). Haploidentical bone marrow transplantation for sickle cell disease. NEJM evidence, 4(3). DOI: https://doi.org/10.1056/EVIDoa2400192.
24/01/2026
Giải mã hoạt động của tế bào gốc tạo máu sau khi cấy ghép đồng loài
Ghép tế bào gốc tạo máu (hematopoietic stem cell transplantation – HSCT) đồng loài được thực hiện bằng cách truyền tế bào gốc tạo máu của người hiến cho người nhận mắc các bệnh như ung thư máu, suy tủy xương, một số rối loạn máu di truyền,… Quy trình này thay thế các tế bào máu bị tổn thương của bệnh nhân bằng các tế bào gốc khỏe mạnh từ người hiến tặng, nhờ đó tái tạo toàn bộ hệ thống máu và miễn dịch của bệnh nhân. Mặc dù đã được thực hiện trong hơn 50 năm qua, nhưng vẫn còn nhiều câu hỏi về cách thức hoạt động của tế bào gốc sau cấy ghép vẫn chưa có lời giải đáp. Lần đầu tiên, các nhà khoa học đã theo dõi những gì xảy ra với tế bào gốc sau khi cấy ghép trong nhiều năm. Điều này có thể mở đường cho các chiến lược mới trong lựa chọn người hiến, tăng tỷ lệ thành công cũng như độ an toàn. Nghiên cứu được công bố trên tạp chí uy tín Nature ngày 30 tháng 10 năm 2024. Trong nghiên cứu này, 10 cặp anh chị em là người hiến – người nhận ghép tế bào gốc tạo máu (thời gian ghép từ 9 đến 31 năm trước) được lấy máu để giải trình tự toàn hệ gen, nhằm phân tích các biến thể xảy ra trong suốt cuộc đời ở tế bào gốc của người hiến và người nhận, từ đó theo dõi xem có bao nhiêu tế bào gốc sống sót và phân chia tái tạo các tế bào mới trong cơ thể bệnh nhân. Đây là điều từ trước tới nay chưa thực hiện được. Nhóm nghiên cứu phát hiện ra rằng những ca ghép với người hiến trẻ tuổi hơn (18 – 47 tuổi) có khoảng 5.000 – 30.000 tế bào gốc sống sót lâu dài, cao hơn khoảng 10 lần so với những ca ghép có người hiến ở độ tuổi cao (50 – 66 tuổi). Bệnh nhân nhận tế bào từ những người trẻ tuổi hơn thường có kết quả tốt hơn, với khả năng miễn dịch được cải thiện và giảm nguy cơ tái phát. Quá trình cấy ghép cũng làm hệ thống tạo máu của người nhận già đi khoảng 10 – 15 năm (được đánh giá qua sự đa dạng tế bào gốc thấp hơn), nguyên nhân do sự phân chia khoảng 25 lần từ những tế bào gốc sống sót để tái tạo được toàn bộ hệ thống tạo máu. Điều đáng ngạc nhiên là tế bào gốc trải qua quá trình phân chia đó một cách nhanh chóng, nhưng chúng có ít đột biến gen mới phát sinh so với ban đầu. Một số yếu tố di truyền cũng được xác định là giúp tế bào gốc phát triển tốt hơn những tế bào khác, về mặt lý thuyết thì những gen này có thể được nghiên cứu sử dụng để cải thiện khả năng thành công của quy trình cấy ghép. Kết quả của nghiên cứu này mang lại những hi vọng về việc xây dựng các chiến lược ghép tế bào gốc tạo máu đồng loài an toàn và hiệu quả hơn. TÀI LIỆU THAM KHẢO Spencer Chapman M., et al. (2024). Clonal dynamics after allogeneic haematopoietic cell transplantation. Nature, 1-9. DOI: https://doi.org/10.1038/s41586-024-08128-y
24/01/2026




