FDA phê duyệt liệu pháp tế bào gốc tạo máu chỉnh sửa gen đầu tiên cho hội chứng Wiskott-Aldrich.
Trong thông cáo báo chí ngày 09 tháng 12 năm 2025 của Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (The U.S. Food and Drug Administration, US FDA), đơn vị này đã công bố phê duyệt Waskyra (etuvetidigene autotemcel), liệu pháp gen dựa trên tế bào đầu tiên để điều trị hội chứng Wiskott-Aldrich. Waskyra được chỉ định cho bệnh nhi từ 6 tháng tuổi trở lên và người lớn mắc hội chứng Wiskott-Aldrich có đột biến gen WAS, những người có thể ghép tế bào gốc tạo máu (hematopoietic stem cell – HSC) nhưng không có người hiến phù hợp về kháng nguyên bạch cầu người (human leukocyte antigen – HLA).
Hội chứng Wiskott-Aldrich (Wiskott-Aldrich syndrome, WAS) là một rối loạn di truyền hiếm gặp của hệ thống tạo máu do đột biến gen WAS trên nhiễm sắc thể giới tính X gây ra, hầu như chỉ xảy ra ở nam giới với tỷ lệ mắc khoảng 1/250.000 nam giới. Bệnh thường biểu hiện ở trẻ em với các triệu chứng nhiễm trùng tái phát, chảy máu, chàm và tăng nguy cơ mắc bệnh tự miễn và u lympho. Việc điều trị bệnh chủ yếu là kiểm soát triệu chứng và ngăn ngừa biến chứng, phương pháp duy nhất có thể chữa khỏi là ghép tế bào gốc tạo máu đồng loại, nhưng tiềm ần nhiều rủi ro và cần người hiến tặng phù hợp.
Waskyra bao gồm các tế bào gốc tạo máu của chính bệnh nhân, đã được cải biến di truyền để mang các bản sao chức năng của gen WAS, sau đó được truyền tĩnh mạch để phục hồi quá trình sản xuất tế bào máu, nhờ đó giải quyết nguyên nhân gốc rễ của bệnh. Tính an toàn và hiệu quả của Waskyra được đánh giá dựa trên một nghiên cứu lâm sàng đa quốc gia, nhãn mở, đơn nhóm với 10 bệnh nhân WAS 1-9 tuổi, và một chương trình tiếp cận mở rộng với 17 bệnh nhân WAS 1-35 tuổi. Kết quả cho thấy lợi ích lâm sàng đáng kể và bền vững cho bệnh nhân, bao gồm sự giảm đáng kể các biểu hiện bệnh chính gây ra bệnh tật và tử vong. Tỷ lệ nhiễm trùng nặng giảm 93% trong giai đoạn từ 6 đến 18 tháng sau điều trị so với tỷ lệ 12 tháng trước điều trị. Các biến cố chảy máu từ trung bình đến nặng giảm 60% trong 12 tháng đầu sau điều trị so với 12 tháng trước điều trị. Hầu hết bệnh nhân không ghi nhận hiện tượng chảy máu từ trung bình đến nặng sau 4 năm điều trị. Các tác dụng phụ thường gặp nhất liên quan đến Waskyra bao gồm phát ban, nhiễm trùng đường hô hấp, giảm bạch cầu hạt kèm sốt, nhiễm trùng liên quan đến ống thông, nôn mửa, tiêu chảy, tổn thương gan và xuất huyết dưới da.
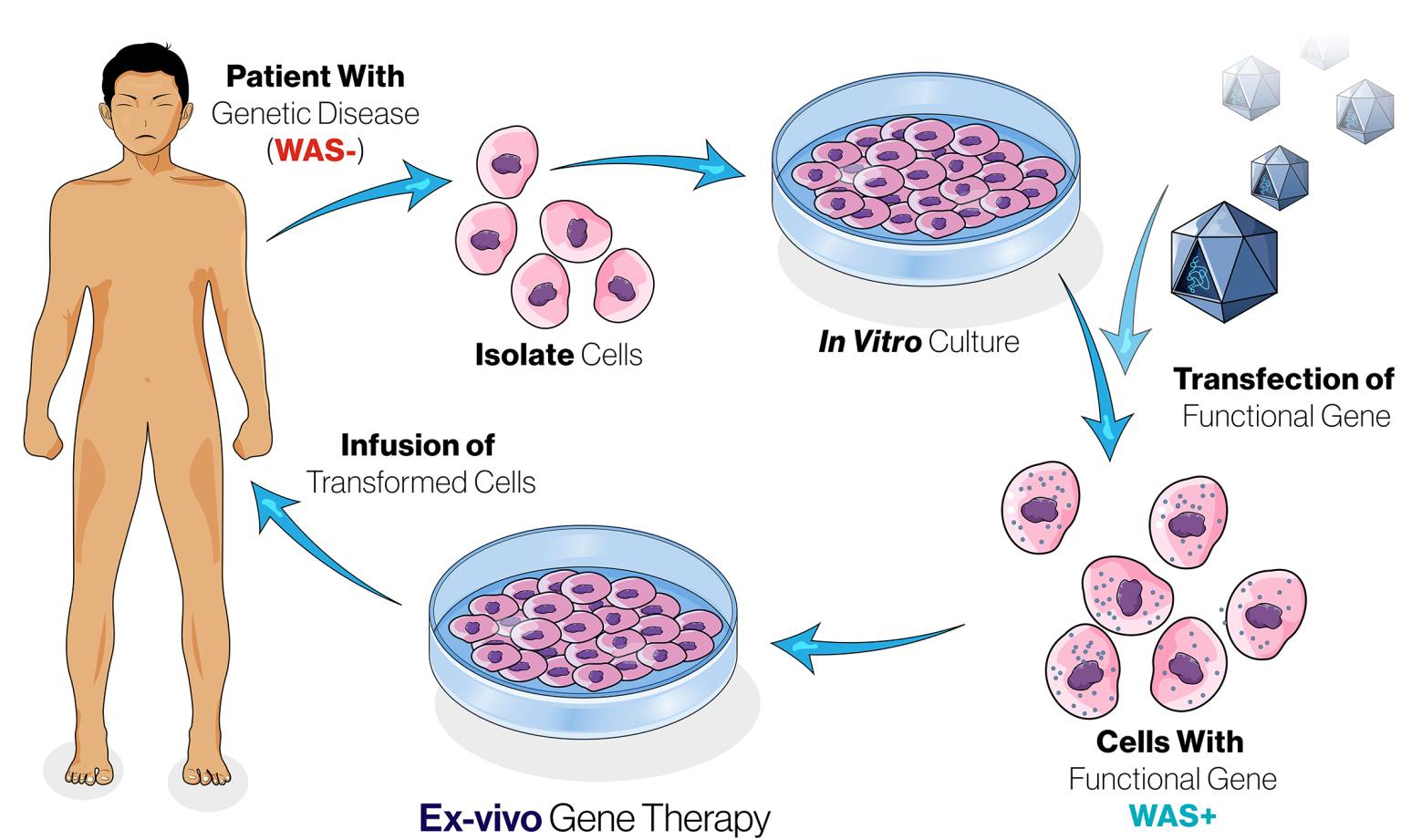
Sự chấp thuận của FDA dành cho liệu pháp này là một cột mốc mang tính đột phá, đáp ứng nhu cầu cấp thiết cho những bệnh nhân WAS, những người đã cho rằng họ có “một cuộc sống đầy lo lắng và sợ hãi kinh hoàng” mà không có bất kỳ liệu pháp điều trị nào được phê duyệt. Trong quá trình xem xét cấp phép cho Waskyra, FDA đã thể hiện sự linh hoạt về quy định phù hợp trên 4 lĩnh vực quan trọng: các vấn đề liên quan đến bệnh hiếm gặp (WAS chỉ gặp ở khoảng 1/250.000 nam giới), thiết kế thử nghiệm (không yêu cầu nhóm chứng do số lượng bệnh nhân rất ít), cơ chế tác dụng rõ ràng, quy tình sản xuất và kiểm soát. Điều này cho phép phê duyệt kịp thời các sản phẩm cho các bệnh hiếm gặp, nghiêm trọng, đe dọa tính mạng, đồng thời cân bằng cẩn thận các yêu cầu dữ liệu trước phê duyệt với các cam kết sau khi đưa sản phẩm ra thị trường.
Đây là sản phẩm liệu pháp tế bào và gen đầu tiên được FDA phê duyệt từ một tổ chức phi lợi nhuận, với nhà phát triển là Fondazione Telethon ETS có trụ sở tại Italy. Sản phẩm Waskyra cũng được Cơ quan Dược phẩm Châu Âu (European Medicines Agency, EMA) khuyến nghị cấp phép lưu hành tại Liên minh Châu Âu (the European Union, EU).
TÀI LIỆU THAM KHẢO
1. Thông cáo báo chí ngày 09 tháng 12 năm 2025 của Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ về việc phê duyệt phương pháp điều trị gen đầu tiên cho hội chứng Wiskott-Aldrich https://www.fda.gov/news-events/press-announcements/fda-approves-first-gene-therapy-treatment-wiskott-aldrich-syndrome
2. Bản tin ngày 14 tháng 11 năm 2025 của Cơ quan Dược phẩm Châu Âu về liệu pháp gen đầu tiên điều trị hội chứng hiếm gặp Wiskott-Aldrich https://www.ema.europa.eu/en/news/first-gene-therapy-treat-rare-disease-wiskott-aldrich-syndrome