ỨNG DỤNG THEO BỆNH LÝ

“Bệnh nhân Oslo” – trường hợp tiếp theo được chữa khỏi HIV nhờ ghép tế bào gốc
Người đàn ông Na Uy là trường hợp tiếp theo trong số ít những người được xác định chữa khỏi HIV nhờ ghép tế bào gốc, và là trường hợp đầu tiên trong số này được ghép tủy xương từ người thân trong gia đình.
17/04/2026

Liệu pháp CAR-T điều trị thành công đồng thời ba bệnh tự miễn trên cùng một bệnh nhân
Sau một năm sử dụng liệu pháp CAR-T, một người phụ nữ Đức mắc đồng thời 3 bệnh tự miễn nghiêm trọng đã không cần điều trị gì thêm, thay vì phải sống chung với 9 liệu pháp khác nhau như hàng chục năm trước.
10/04/2026
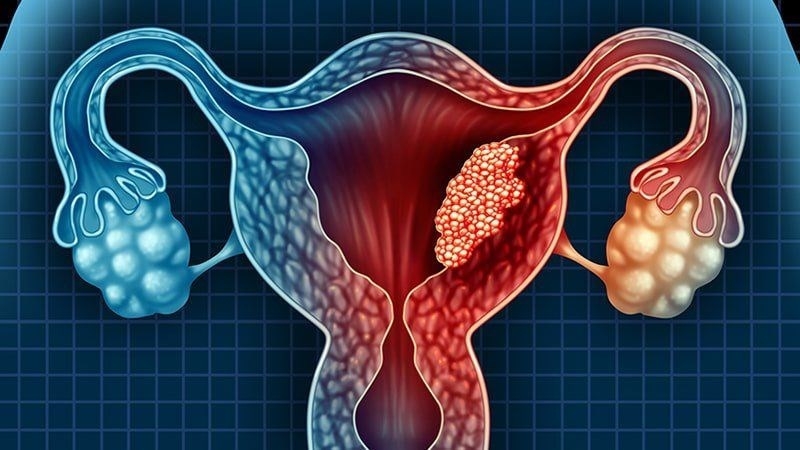
Liệu pháp CAR-NKT mang lại hiệu quả vượt trội khi điều trị ung thư nội mạc tử cung trong nghiên cứu tiền lâm sàng
Trong một nghiên cứu mới công bố, các nhà khoa học cho thấy liệu pháp tế bào CAR-NKT hiệu quả hơn các liệu pháp miễn dịch hiện tại như CAR-T, CAR-NK trong điều trị ung thư nội mạc tử cung.
26/03/2026
Tế bào gốc từ răng sữa cho thấy tiềm năng trong điều trị bại não
Trên mô hình động vật, liệu pháp tế bào gốc cho thấy hiệu quả trong điều trị bại não, ngay cả việc bắt đầu thực hiện sau khi các tổn thương vận động đã xuất hiện.
12/03/2026
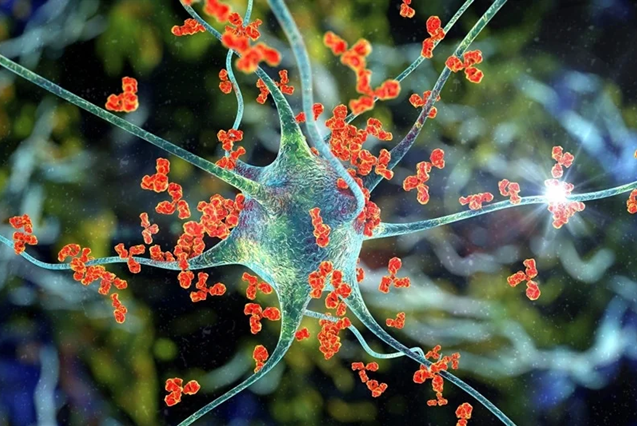
Bệnh tự miễn: khi hệ miễn dịch bảo vệ cơ thể quay lại tấn công tế bào khỏe mạnh
Bệnh tự miễn đề cập đến phản ứng miễn dịch của cơ thể chống lại các tế bào hoặc mô khỏe mạnh, có thể gây nên những tổn thương không thể phục hồi.
05/02/2026
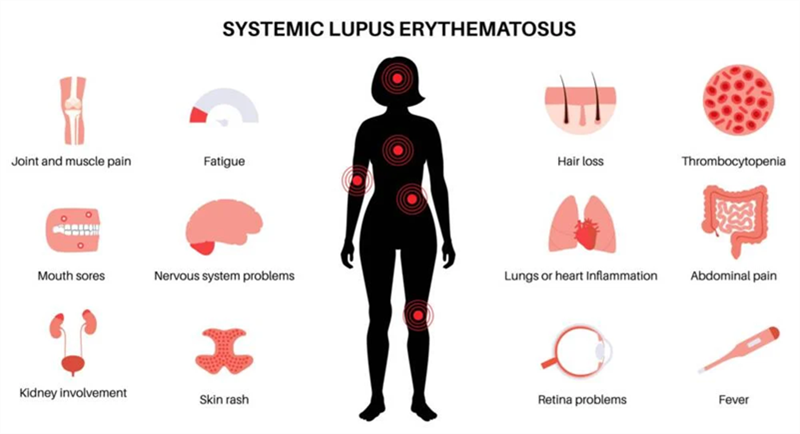
Triển vọng điều trị bệnh lupus ban đỏ hệ thống (SLE) bằng liệu pháp CAR-T đồng loại
Liệu pháp CAR-T đã chứng minh hiệu quả lâm sàng trong điều trị ung thư huyết học, và đang có những tín hiệu lạc quan đối với ung thư u rắn. Những kết quả gần đây cho thấy liệu pháp này có triển vọng trong điều trị các bệnh tự miễn như lupus ban đỏ hệ thống.
29/01/2026
Liệu pháp tế bào gốc phục hồi chức năng não sau đột quỵ/tai biến mạch máu não
Đột quỵ, còn gọi là tai biến mạch máu não, là tình trạng các tế bào não bị tổn thương nghiêm trọng do dòng máu cung cấp cho não bị gián đoạn hoặc giảm đáng kể, khiến các tế bào này chết đi do thiếu oxy và dinh dưỡng. Bệnh có thể do hai nguyên nhân chính là nhồi máu não (do cục máu đông hoặc mảng xơ vữa làm tắc nghẽn mạch máu) chiếm khoảng 85% trường hợp, hoặc xuất huyết não (do mạch máu bị vỡ gây chảy máu vào não). Thống kê cho thấy khoảng 1/4 số người trưởng thành bị đột quỵ ít nhất một lần trong đời, và 1/2 trong số họ chịu những di chứng nặng như liệt, suy giảm khả năng nói, hiện tại chưa có liệu pháp nào có thể phục hồi hoàn toàn những tổn thương này. Các nhà khoa học tại Đại học Zurich (Thụy Sỹ) đã công bố kết quả nghiên cứu cho thấy cấy tế bào gốc có thể khắc phục những tổn thương do đột quỵ, đánh dấu một cột mốc quan trọng trong điều trị các rối loạn não. Họ đã sử dụng tế bào gốc thần kinh (neural stem/progenitor cells – NSC/NPC) ở người, là loại tế bào có thể hình thành các loại tế bào khác nhau của hệ thần kinh. Những tế bào này được thu nhận từ quá trình biệt hóa của tế bào gốc đa tiềm năng cảm ứng (induced pluripotent stem cell – iPSC), được tạo ra từ quá trình tái lập trình từ tế bào đã biệt hóa. Nhóm nghiên cứu đã gây đột quỵ tổn thương vĩnh viễn ở chuột, với các đặc điểm rất giống với triệu chứng của đột quỵ ở người. Sau 7 ngày kể từ khi gây đột quỵ, họ đã cấy ghép tế bào gốc thần kinh vào vùng não bị tổn thương và theo dõi diễn biến bằng nhiều phương pháp khác nhau, bao gồm chẩn đoán hình ảnh và xét nghiệm sinh hóa. Các nhà khoa học đã phát hiện ra rằng các tế bào gốc đã tồn tại trong suốt thời gian theo dõi, hầu hết chúng đã biệt hóa thành các tế bào thần kinh và có thể giao tiếp với các tế bào não chuột. Không chỉ tái tạo tế bào thần kinh, những tế bào gốc được cấy ghép đã thúc đẩy những quá trình tái tạo khác: hình thành mạch máu mới, suy giảm các quá trình của phản ứng viêm, cải thiện tính toàn vẹn của hàng rào máu não. Chức năng vận động của chuột đột quỵ sau khi được sử dụng liệu pháp cũng đã được phục hồi, với những bằng chứng về phân tích dáng đi được hỗ trợ bởi AI. A) Biệt hóa tế bào gốc đa tiềm năng cảm ứng (iPSC) thành tế bào gốc thần kinh (NPC) sử dụng cho liệu pháp. B) Các tế bào gốc thần kinh (NPC) biệt hóa thành tế bào thần kinh sau khi được cấy ghép vào não chuột. C) Thiết kế nghiên cứu. Những kết quả này đã mang lại hy vọng về khả năng ứng dụng trên người. Các tế bào gốc được nuôi cấy mà không sử dụng hóa chất có nguồn gốc động vật (xeno-free), một yêu cầu bắt buộc để có thể ứng dụng vào điều trị cho bệnh nhân. Nhóm nghiên cứu cũng có phát hiện mới về thời điểm sử dụng liệu pháp tế bào gốc, việc cấy ghép có lẽ hiệu quả hơn khi được thực hiện sau khoảng một tuần kể từ khi xảy ra cơn đột quỵ, thay vì thực hiện ngay sau đó như đa phần những thử nghiệm trước đây. Trong điều kiện lâm sàng, khoảng thời gian đó có thể tạo điều kiện thuận lợi đáng kể cho việc chuẩn bị sản phẩm và bệnh nhân để triển khai liệu pháp. Các nhà khoa học đang tiếp tục thực hiện những nghiên cứu tiếp theo, bao gồm kiểm soát sự phát triển của tế bào gốc trong não, đưa tế bào gốc vào cơ thể bằng cách truyền nội mạch thay vì tiêm vào não, từ đó có thể cải thiện hiệu quả và tính an toàn trước khi thử nghiệm lâm sàng trên người. --------- Tài liệu tham khảo: 1. Weber R. Z., et al. (2025). Neural xenografts contribute to long-term recovery in stroke via molecular graft-host crosstalk. Nature Communications, 16(1), 8224. DOI: https://doi.org/10.1038/s41467-025-63725-3 2. Weber R. Z., et al. (2025). Delayed Transplantation of Neural Stem Cells Improves Initial Graft Survival after Stroke. Advanced Science, e04154. DOI: https://doi.org/10.1002/advs.202504154 --------- Xem thêm: - Đại cương về tế bào gốc: Tế bào gốc đa tiềm năng cảm ứng (iPSC) – tái lập trình tế bào soma https://www.facebook.com/share/p/1EfjgptWa7/ - Đại cương về tế bào gốc: Tế bào gốc đa tiềm năng cảm ứng (iPSC): đặc điểm sinh học và ứng dụng https://www.facebook.com/share/p/1Jx2H7LuN8/ - Phát hiện tế bào gốc thần kinh bên ngoài não và tủy sống: khám phá mở ra con đường mới cho y học tái tạo https://www.facebook.com/share/p/1JabuH8cQ4/ - Liệu pháp tế bào gốc trung mô (MSC) giúp phục hồi não sau đột quỵ thiếu máu não cục bộ https://www.facebook.com/share/p/1BKaees6wU/ - Triển vọng của liệu pháp tế bào gốc trung mô (MSC) trong điều trị đột quỵ thiếu máu cục bộ gây tổn thương não ở trẻ sơ sinh https://www.facebook.com/share/p/1GBAzK8wct/
23/01/2026
Phương pháp đột phá kết hợp công nghệ tế bào gốc và in 3D để tái tạo sợi thần kinh, phục hồi chấn thương tủy sống
Tủy sống có chức năng dẫn truyền tín hiệu giữa não và phần còn lại của cơ thể. Chấn thương tủy sống bao gồm tổn thương bất kỳ phần nào của tủy sống, hoặc tổn thương các dây thần kinh ở cuối tủy sống (được gọi là đuôi ngựa), gây ra những thay đổi vĩnh viễn về chức năng của cơ thể ở dưới vị trí chấn thương (bị liệt). Hiện tại, các phương pháp điều trị vẫn chưa có cách phục hồi hoàn toàn tổn thương và tình trạng liệt, do các tế bào thần kinh bị chết, các sợi thần kinh không thể tái tạo tại vị trí chấn thương. Gần đây, các nhà khoa học đã đưa ra một quy trình đột phá kết hợp giữa công nghệ tế bào gốc, nuôi cấy mô và in 3D sinh học để phục hồi tình trạng đó. Phương pháp này bao gồm việc tạo ra một khung in 3D (được gọi là khung organoid) với các kênh vi mô, các kênh này sau đó được nuôi cấy với các tế bào tiền thân thần kinh tủy sống (spinal neural progenitor cell – sNPC) đặc hiệu theo từng khu vực, có nguồn gốc từ tế bào gốc đa tiềm năng cảm ứng (induced pluripotent stem cell – iPSC). Các kênh vi mô của khung 3D có vai trò định hướng sự phát triển của tế bào gốc, đảm bảo các sợi thần kinh mới phát triển theo đúng hướng mong muốn, nhờ đó có thể tạo nên kênh dẫn truyền khi được đặt vào tủy sống, thay thế vùng bị tổn thương. Sau đó, nhóm nghiên cứu đã cấy ghép sản phẩm này vào những con chuột bị đứt tủy sống hoàn toàn. Sau 12 tuần cấy ghép, phần lớn các tế bào đã biệt hóa thành tế bào thần kinh, tích hợp vào mô tủy sống của vật chủ, giúp phục hồi chức năng đáng kể ở chuột chấn thương. Sơ đồ thí nghiệm. A) Quy trình in các khung đỡ organoid tủy sống. Khung 3D gồm một đế thủy tinh và khung đỡ silicon với ba kênh vi mô theo từng lớp. Mực in 3D chứa tế bào tiền thân thần kinh tủy sống (sNPC), Matrigel và môi trường thần kinh có yếu tố tăng trưởng, được định vị bên trong các kênh vi mô. Toàn bộ khung này được nuôi cấy để biệt hóa in vitro cho đến khi hình thành organoid. B) Cấy ghép các khung organoid vào chuột chấn thương tủy sống. Các khung organoid được tách ra khỏi đế thủy tinh, lắp ráp vào khoảng trống ở tủy sống của chuột mô hình (bị tạo chấn thương bằng cắt ngang tủy sống) để thúc đẩy phục hồi chức năng. Mặc dù nghiên cứu đang ở giai đoạn đầu trên động vật mô hình, nhưng nó đã mở ra hướng đi mới đầy hy vọng trong điều trị chấn thương tủy sống. Nhóm nghiên cứu đang có những biện pháp cải tiến hơn để cải thiện chất lượng và khả năng ứng dụng của sản phẩm 3D này, đồng thời hy vọng có thể áp dụng công nghệ đó cho các thử nghiệm lâm sàng trong tương lai. --------- TÀI LIỆU THAM KHẢO Han G., et al. (2025). 3D‐Printed Scaffolds Promote Enhanced Spinal Organoid Formation for Use in Spinal Cord Injury. Advanced Healthcare Materials. doi.org/10.1002/adhm.202404817
23/01/2026
Liệu pháp tế bào gốc có thể là phương pháp điều trị an toàn và hiệu quả với bệnh Parkinson
Bệnh Parkinson là một bệnh thoái hóa thần kinh đặc trưng bởi sự mất dần các tế bào sản xuất dopamine (một chất dẫn truyền thần kinh), làm mất kiểm soát vận động cơ bắp, khiến cho bệnh nhân bị cứng cơ, chuyển động chậm, run rẩy và rối loạn dáng đi. Các phương pháp điều trị hiện tại có thể giúp giảm những triệu chứng ở giai đoạn đầu, nhưng hiệu quả giảm dần kèm theo sự gia tăng các tác dụng phụ như loạn động. Liệu pháp tế bào với việc bổ sung các tế bào thần kinh sản xuất dopamine trong não có thể là một phương pháp hiệu quả hơn. Mới đây, hai thử nghiệm lâm sàng cùng được công bố trên tạp chí uy tín Nature đều sử dụng các tế bào gốc để điều trị bệnh Parkinson, kết quả đã cho thấy tính an toàn của liệu pháp, đồng thời thu được những đánh giá hiệu quả ban đầu khả quan, mặc dù vẫn cần nghiên cứu thêm để đánh giá chi tiết hơn về lợi ích lâm sàng mà bệnh nhân có thể nhận được. Trong một thử nghiệm lâm sàng giai đoạn I/II tại Nhật Bản, 7 bệnh nhân đã được cấy ghép các tế bào tiền thân của tế bào thần kinh sản xuất dopamine (có nguồn gốc từ tế bào gốc đa tiềm năng cảm ứng của người – iPSC) vào cả hai bên bán cầu não. Sau 24 tháng theo dõi, nhóm nghiên cứu không ghi nhận biến cố bất lợi nghiêm trọng nào, không phát hiện tế bào phát triển quá mức hay tạo u (là rủi ro thường được quan tâm khi ghép tế bào gốc đa tiềm năng). Trọng tâm chính của thử nghiệm là kiểm tra tính an toàn và tìm kiếm các tác dụng phụ, nhưng các tác giả cũng theo dõi những thay đổi trong các triệu chứng vận động và sản xuất dopamine, trong đó các tế bào được cấy ghép đã sản xuất dopamine và các triệu chứng vận động giảm: 5 trong số 6 người dùng thuốc điều trị tiêu chuẩn có sự cải thiện về chức năng vận động, đồng thời sau khi ngừng thuốc thì 4 người vẫn duy trì sự cải thiện đó. Liệu pháp tế bào gốc đa tiềm năng trong điều trị bệnh Parkinson. Các tế bào gốc đa tiềm năng như tế bào gốc đa tiềm năng cảm ứng (Induced pluripotent stem cell) và tế bào gốc phôi (embryonic stem cell) có khả năng phân chia vô hạn và biệt hóa thành bất kỳ loại tế bào nào trong cơ thể. Chúng được biệt hóa thành tế bào tiền thân của tế bào thần kinh sản xuất dopamine ở cấp độ sử dụng trong lâm sàng, sau đó được cấy ghép vào não ở vị trí nhân bèo hay bèo sẫm (putamen), là vùng kết hợp với nhân đuôi (caudate nucleus) để tạo nên vân não (striatum). Vân não kết nối với vùng đen (substantia nigra), là nơi mất tế bào thần kinh sản xuất dopamine nghiêm trọng nhất. Trong một thử nghiệm lâm sàng khác ở giai đoạn I, nhóm nghiên cứu Mỹ và Canada đã đánh giá tính an toàn của bemdaneprocel – một sản phẩm tế bào tiền thân của tế bào thần kinh sản xuất dopamine, có nguồn gốc từ tế bào gốc phôi người (hESC). Theo đó, 12 bệnh nhân được phẫu thuật ghép bemdaneprocel vào nhân bèo cả hai bên não, với 5 người dùng liều thấp (0,9 triệu tế bào trên mỗi nhân bèo) và 7 người dùng liều cao (2,7 triệu tế bào mỗi nhân bèo). Sản phẩm nói chung được dung nạp tốt và không có tác dụng phụ nghiêm trọng nào được báo cáo trong suốt 18 tháng theo dõi, không ghi nhận trường hợp loạn động nào – trước đây thường liên quan đến cấy ghéo mô thai nhi trong điều trị Parkinson. Một số cải thiện về chức năng vận động đã được quan sát thấy trên những bệnh nhân ở cả hai nhóm, kết quả chụp PET (chụp cắt lớp phóng xạ positon) đã xác nhận các tế bào được cấy ghép đã sống sót và sản xuất dopamine. Cả hai thử nghiệm lâm sàng này đều đánh giá tính an toàn của sản phẩm tế bào tiền thân thân của tế bào thần kinh sản xuất dopamine, có nguồn gốc từ tế bào gốc đa tiềm năng của người, được ghép đồng loài để điều trị bệnh Parkinson. Hiệu quả điều trị chỉ được ghi nhận như một dạng kết quả mở rộng của nghiên cứu và cần thêm các nghiên cứu khác để đánh giá sâu hơn. Cả hai đều có một số hạn chế như cỡ mẫu nhỏ, nghiên cứu nhãn mở (các nhà nghiên cứu và bệnh nhân đều biết ai đang được điều trị như thế nào, có thể dẫn đến những đánh giá cảm tính khi ghi nhận kết quả). Mặc dù vậy, những kết quả này cho thấy tính an toàn và những tín hiệu lạc quan về hiệu quả trong việc sử dụng liệu pháp tế bào gốc trong điều trị bệnh Parkinson, từ đó gợi mở những thử nghiệm lâm sàng giai đoạn tiếp theo. --------- TÀI LIỆU THAM KHẢO 1. Okano H. (2025). Clinical trials test the safety of stem-cell therapy for Parkinson's disease, Nature. DOI: 10.1038/d41586-025-00688-x (News & views). 2. Sawamoto N., et al. (2025). Phase I/II trial of iPS-cell-derived dopaminergic cells for Parkinson's disease. Nature. DOI: 10.1038/s41586-025-08700-0. 3. Tabar V., et al. (2025). Phase I trial of hES cell-derived dopaminergic neurons for Parkinson's disease. Nature. DOI: 10.1038/s41586-025-08845-y.
23/01/2026
Phương pháp điều trị bằng tế bào gốc giúp cải thiện tình trạng chấn thương tủy sống
Theo thông tin từ Thời báo Nhật Bản (The Japan Times) ngày 22/03/2025, các nhà khoa học đến từ Đại học Keio ở Tokyo đã cải thiện được chức năng vận động của 2 trong số 4 bệnh nhân chấn thương tủy sống bằng phương pháp điều trị tế bào gốc.
23/01/2026
Tiềm năng điều trị chấn thương tủy sống bằng tế bào gốc thần kinh biến đổi gen
Các tế bào thần kinh tủy sống có sợi trục dài đóng vai trò truyền tín hiệu từ não đến các bộ phận khác của cơ thể, kiểm soát hoạt động và cảm giác của các cơ quan. Chấn thương tủy sống gây ra tổn thương không thể hồi phục cho các tế bào thần kinh và sợi trục, làm gián đoạn quá trình truyền tín hiệu, thường gây liệt ở dưới vùng tổn thương. Chấn thương tủy sống thường xảy ra do ngã, tai nạn giao thông, tai nạn thể thao,… làm nạn nhân thường bị tàn tật suốt đời. Hiện tại chưa có phác đồ điều trị hoặc quản lý lâm sàng hiệu quả dành cho bệnh nhân chấn thương tủy sống.
23/01/2026
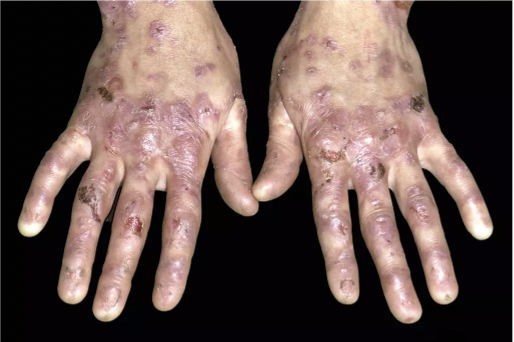
Liệu pháp tế bào gốc trung mô CORDStrom với bệnh ly thượng bì bóng nước thể loạn dưỡng lặn (RDEB) và kế hoạch đăng ký cấp phép sản phẩm với FDA Hoa Kỳ
Kết quả thử nghiệm lâm sàng MissionEB (ISRCTN14409785) cho thấy liệu pháp tế bào gốc CORDStrom (được phát triển bởi công ty Inmune Bio) có khả năng cải thiện tình trạng bệnh ở trẻ em mắc bệnh ly thượng bì bóng nước thể loạn dưỡng lặn trung bình và nặng. Những dữ liệu này thúc đẩy Inmune Bio nộp đơn lên Cục Quản lý Thực phẩm và Dược phẩm (FDA) Hoa Kỳ để xin phê duyệt liệu pháp này ngay trong năm nay, sau đó dự kiến sẽ đăng ký tại Vương quốc Anh và Liên minh Châu Âu.
23/01/2026





