ỨNG DỤNG THEO BỆNH LÝ

Điều trị viêm da dị ứng bằng tế bào gốc trung mô (MSC)
Viêm da dị ứng là một rối loạn viêm mạn tính ở da điển hình, đặc trưng bởi các tổn thương da dạng chàm (eczema) và ngứa dữ dội, ảnh hưởng lớn đến chất lượng cuộc sống. Có nhiều cơ chế bệnh sinh khác nhau gây nên viêm da dị ứng, như yếu tố di truyền, khiếm khuyết hàng rào biểu bì và các yếu tố miễn dịch gây bệnh. Việc điều trị viêm da dị ứng thường là điều trị tại chỗ sử dụng corticosteroid, chất ức chế calcineurin, chất đối kháng thụ thể leukotriene và thuốc kháng histamine, các thuốc này làm giảm tạm thời các triệu chứng nhưng đồng thời gây những tác dụng phụ và kháng thuốc trong điều trị lâu dài. Các phương pháp điều trị mới (kháng thể đơn dòng, dùng tế bào gốc) đang được thử nghiệm và hi vọng được áp dụng trong trong tương lai gần. Tế bào gốc/tế bào đệm trung mô (Mesenchymal stem/stromal cell – MSC) là loại tế bào đa tiềm năng giới hạn, có khả năng tự đổi mới và biệt hóa được thành nhiều loại tế bào khác nhau trong cơ thể, hiện được nghiên cứu ứng dụng nhiều nhất trong liệu pháp tế bào. MSC có thể được thu nhận từ nhiều nguồn khác nhau trong cơ thể, như dây rốn, tủy răng sữa, tủy xương, mô mỡ,… Ngoài những thử nghiệm trong tái tạo mô, MSC đã được nghiên cứu điều trị nhiều loại bệnh liên quan đến miễn dịch và bệnh tự miễn, như hen suyễn, lupus ban đỏ hệ thống, viêm khớp dạng thấp, đa xơ cứng, viêm da dị ứng. Việc ứng dụng MSC trong điều trị những bệnh này dựa trên khả năng điều hòa miễn dịch của chúng, như ức chế hoạt động của tế bào T và B, giải phóng các cytokine chống viêm (IL-10 và TGF-β), giảm sự phát triển của IL-4 và IFNγ, giảm sản xuất lgE,… Khoảng 10 năm gần đây, nhiều nghiên cứu đã hướng đến điều trị viêm da dị ứng bằng MSC. Các nhiên cứu tiền lâm sàng cho thấy sự tiến triển bệnh có thể bị ức chế bởi MSC có nguồn gốc từ máu dây rốn (UCB-MSC), tủy xương (BM-MSC) hoặc mô mỡ (AD-MSC), trong đó loại tế bào gốc, quá trình chuẩn bị tế bào, số lượng tế bào được cấy ghép, tần suất sử dụng, các mục tiêu theo dõi đánh giá tiến triển bệnh,… khiến các nghiên cứu chưa có sự thống nhất về hiệu quả điều trị. Cơ chế MSC làm giảm phản ứng dị ứng vẫn chưa rõ ràng, vì hầu hết các nghiên cứu không tập trung vào điều trị tại chỗ mà điều hòa phản ứng viêm toàn thân (trong đó một thử nghiệm đã cho thấy tác dụng bảo vệ được quan sát rõ ràng hơn khi tiêm MSC dưới da). MSC cũng không tự động ức chế miễn dịch mà được kích thích để có các đặc tính điều hòa miễn dịch, ví dụ sử dụng các yếu tố mồi như IFN-γ, TNF-α và IL-1β. Mặc dù các nghiên cứu tiền lâm sàng cho những kết quả khả quan, tuy nhiên hiện mới chỉ có một thử nghiệm lâm sàng giai đoạn I/IIa được công bố trong sử dụng MSC để điều trị viêm da dị ứng. MSC từ máu cuống rốn (UCB-MSC) được tiêm dưới da ở 34 người trưởng thành bị viêm da dị ứng mức độ trung bình đến nặng, sau đó đánh giá bằng điểm chỉ số diện tích và mức độ nghiêm trọng của bệnh chàm - eczema (EASI). Kết quả là sự cải thiện triệu chứng được quan sát ở các bệnh nhân thử nghiệm, đặc biệt là nhóm điều trị với liều MSC cao hơn (5 x 10^7 tế bào) có điểm EASI giảm 50% ở hơn một nửa số bệnh nhân (6/11) mà không có tác dụng phụ. Hiện tại, một số thử nghiệm lâm sàng với số lượng bệnh nhân lớn hơn và thiết kế nghiên cứu chặt chẽ hơn đang được thực hiện, như các thử nghiệm NCT02888704, NCT04137562, NCT04179760 (Thư viện Y khoa Quốc gia Hoa Kỳ, https://clinicaltrials.gov/ct2/home). --------- TÀI LIỆU THAM KHẢO Daltro S.R.T., et al. (2020). Mesenchymal stem cells and atopic dermatitis: a review. Frontiers in cell and developmental biology, 8, 326. DOI: 10.3389/fcell.2020.00326
23/01/2026
Thử nghiệm lâm sàng giai đoạn I/II chứng minh tiêm lặp lại tế bào gốc trung mô (MSC) đã cải thiện tình trạng thoái hóa khớp gối
Viêm xương khớp (Osteoarthritis), trong đó có thoái hóa khớp gối, là bệnh khớp phổ biến nhất, dẫn đến đau mạn tính, chất lượng cuộc sống kém và tăng tỷ lệ tỷ vong, gây nên gánh nặng xã hội lớn do chi phí chăm sóc sức khỏe tăng cao và giảm tuổi lao động. Hiện tại chưa có loại thuốc điều trị nào thực sự có thể điều trị bệnh hiệu quả, các mục tiêu hiện tại hướng đến việc phát triển các liệu pháp tế bào để cải thiện tình trạng bệnh. Những nghiên cứu về việc sử dụng tế bào gốc trung mô (MSC) có nguồn gốc từ tủy xương hoặc mô mỡ tự thân, hay MSC từ dây rốn (UC-MSC) đồng loài đã cho thấy những bằng chứng ban đầu về hiệu quả lâm sàng sau thời gian theo dõi. Trong một nghiên cứu được công bố năm 2019, các nhà khoa học đã thực hiện thử nghiệm lâm sàng ngẫu nhiên, mù ba, có đối chứng giai đoạn I/II (mã số NCT02580695) để đánh giá tính an toàn và hiệu quả điều trị của MSC dây rốn đồng loài (nguồn MSC dễ tiếp cận hơn và có một số đặc tính sinh học cao hơn MSC mô mỡ hay tủy xương) trong điều trị thoái hóa khớp gối. Tổng số 26 bệnh nhân tham gia nghiên cứu được chia thành 3 nhóm ngẫu nhiên: tiêm khớp liều đơn duy nhất UC-MSC (nhóm MSC-1, n = 9), hoặc liều UC-MSC lặp lại sau 6 tháng kể từ lần tiêm đầu tiên (nhóm MSC-2, n = 9), với đối chứng là nhóm dùng axit hyarulonic lặp lại sau 6 tháng (nhóm đối chứng HA, n = 8, đây là phương pháp điều trị bổ sung độ nhớt đã được chấp thuận cho bệnh nhân thoái hóa khớp gối). Sau quá trình theo dõi kéo dài 12 tháng, không có tác dụng phụ nghiêm trọng nào được báo cáo. Chỉ những bệnh nhân được điều trị bằng MSC mới có cải thiện đáng kể về chỉ số đau và chức năng so với ban đầu. Những bệnh nhân được tiêm MSC 2 lần đã giảm 86% cơn đau và 89% khả năng vận động sau 12 tháng so với nhóm đối chứng tiêm HA có chỉ số lần lượt là 38% và 50%. Nhóm tiêm MSC 1 lần duy nhất có sự cải thiện liên tục, và đạt được mức độ triệu chứng tương tự nhóm đối chứng ở tháng thứ 12 (sau lần tiêm HA thứ hai). Đáng chú ý là những bệnh nhân tiêm HA chỉ sau 6 tháng đã mất tác dụng đối với chỉ số đau và chức năng vận động, cần tiêm lại liều thứ hai để tiếp tục phục hồi. Những kết quả này được thể hiện rõ trên thang đánh giá điểm đau WOMAC và thang đánh giá trực quan về đau VAS. Dựa trên kết quả chụp cộng hưởng từ (MRI) sau 6 và 12 tháng kể từ khi bắt đầu điều trị, không có bằng chứng nào về tổn thương sụn hoặc vôi hóa khớp được phát hiện, không có sự thay đổi nào so với hình ảnh ban đầu hoặc giữa các nhóm được tìm thấy ở bất kỳ mục nào trong 14 mục của thang điểm WORMS. Những kết quả trên cho thấy UC-MSC là phương pháp điều trị an toàn cho thoái hóa khớp gối, và sự cải thiện tình trạng thoái hóa khớp gối cao hơn rõ rệt so với phương pháp tiêm dịch khớp truyền thống. Trong đó, tiêm MSC lặp lại sau 6 tháng có hiệu quả tốt hơn tiêm MSC một lần duy nhất. Sẽ cần những nghiên cứu với cỡ mẫu lớn hơn, thời gian đánh giá lâu hơn và chỉ tiêu đánh giá rộng hơn đề xác định hiệu quả của phương pháp ghép tế bào gốc trong điều trị bệnh này. Tuy nhiên, những kết quả trên, kết hợp với một số công bố khác gần đây, đã cho thấy MSC là một công cụ đáng chú ý, mang lại những hy vọng lớn về cải thiện tình trạng bệnh và chất lượng cuộc sống cho bệnh nhân thoái hóa khớp gối. --------- TÀI LIỆU THAM KHẢO Matas J., et al. (2019). Umbilical cord-derived mesenchymal stromal cells (MSCs) for knee osteoarthritis: repeated MSC dosing is superior to a single MSC dose and to hyaluronic acid in a controlled randomized phase I/II trial. Stem cells translational medicine, 8(3), 215-224.
23/01/2026

Liệu pháp tế bào đảo tụy có nguồn gốc từ tế bào gốc đồng loại chứng minh hiệu quả trong điều trị tiểu đường tuýp 1
Tiểu đường là bệnh rối loạn chuyển hóa, cơ thể không dung nạp được glucose dẫn đến lượng đường trong máu cao hơn bình thường, từ đó gây nên những biến chứng nguy hiểm như bệnh tim mạch, tổn thương thận, thần kinh, tăng nguy cơ nhiễm trùng,… Ước tính trên thế giới năm 2021 có khoảng hơn 500 triệu người được xác định mắc tiểu đường, ngoài ra có hơn 200 triệu người mắc bệnh chưa được chẩn đoán. Tiểu đường gồm 2 loại chính: tiểu đường tuýp 1 (cơ thể không thể sản xuất insulin do tế bào beta tuyến tụy chịu trách nhiệm sản xuất chúng bị phá hủy) và tiểu đường tuýp 2 (cơ thể đề kháng với insulin), khiến insulin không có hoặc không thể vận chuyển glucose từ máu vào các tế bào. Trong một nghiên cứu mới trình bày ngày 20/06/2025 tại hội nghị thường niên của Hiệp hội Bệnh tiểu đường Hoa Kỳ, các nhà khoa học đã công bố kết quả một thử nghiệm lâm sàng giai đoạn I/II (mã số FORWARD-101, NCT04786262) trong đó chứng minh hiệu quả điều trị tiểu đường tuýp 1 của sản phẩm zimislecel. Zimislecel (VX-880) là một liệu pháp tế bào đảo tụy sản xuất insulin, được biệt hóa hoàn toàn từ tế bào gốc đồng loại, được truyền vào tĩnh mạch cửa gan kết hợp các chiến lược ức chế miễn dịch để phục hồi khả năng sản xuất insulin cho bệnh nhân tiểu đường type 1. Trong nghiên cứu này, một nhóm bệnh nhân (nhóm A) được truyền nửa liều zimislecel (0,4 tỷ tế bào) với tùy chọn truyền nửa liều thứ hai trong vòng 2 năm để đánh giá tính an toàn của liệu pháp, nhóm bệnh nhân khác được truyền liều zimislecel đầy đủ duy nhất một lần để đánh giá tính an toàn và hiệu quả. Kết quả có 14 người tham gia nghiên cứu đã hoàn thành ít nhất 12 tháng theo dõi và đưa vào phân tích, đều có sự dung nạp tế bào và phục hồi chức năng sản xuất insulin. Cả 12 trường hợp thuộc nhóm dùng liều truyền đầy đủ đều không bị hạ đường huyết nghiêm trọng, trong đó 10/12 người sau 1 năm đã không cần tiêm thuốc insulin, 2 bệnh nhân còn lại chỉ cần tiêm với liều thấp hơn thông thường. Các biến chứng thường ở mức trung bình và nhẹ, bao gồm tăng men gan, giảm bạch cầu, giảm chức năng thận ở mức kiểm soát, có 2 trường hợp tử vong nhưng dường như không liên quan đến liệu pháp (1 trường hợp do viêm màng não bởi nhiễm nấm cryptococcus, 1 trường hợp do chứng mất trí nhớ nghiêm trọng kèm theo kích động do tình trạng suy giảm nhận thức thần kinh có từ trước tiến triển). Những kết quả trên cho thấy hiệu quả đáng kinh ngạc của liệu pháp tế bào đảo tụy zimislecel, với một liều truyền duy nhất đã có thể phục hồi chức năng sản xuất insulin của cơ thể. Kết quả này mang đến những hy vọng rất lớn cho các bệnh nhân tiểu đường tuýp 1 trong việc giảm hoặc tránh sự phụ thuộc vào tiêm insulin để kiểm soát đường huyết. Liệu pháp cũng đã chứng minh sự an toàn, không có các biến cố nghiêm trọng, tuy nhiên bệnh nhân phải sử dụng thuốc ức chế miễn dịch chống thải ghép, có thể làm tăng nguy cơ nhiễm trùng và lâu dài làm tăng nguy cơ ung thư. Nhìn chung, đây là bằng chứng cho thấy các đảo tụy có thể được sản xuất từ tế bào gốc đa năng tiềm năng và có thể sử dụng để điều trị hiệu quả bệnh tiểu đường loại 1. --------- TÀI LIỆU THAM KHẢO 1. Reichman T. W., et al. (2025). Stem Cell–Derived, Fully Differentiated Islets for Type 1 Diabetes. New England Journal of Medicine. DOI: 10.1056/NEJMoa2506549 2. Hồ sơ sản phẩm Zimislecel https://adisinsight.springer.com/drugs/800042297
23/01/2026
Tế bào gốc trung mô (MSC) trong điều trị Lupus ban đỏ hệ thống: nghiên cứu mới xác định dấu ấn sinh học tiềm năng để dự báo hiệu quả điều trị
Lupus ban đỏ hệ thống (Systemic Lupus Erythematosus – SLE) là một bệnh lý viêm tự miễn mạn tính có biểu hiện bệnh ở nhiều hệ cơ quan, xảy ra chủ yếu ở phụ nữ trẻ tuổi. Thông thường, hệ thống miễn dịch có vai trò bảo vệ cơ thể khỏi bị nhiễm trùng, tuy nhiên đôi khi chúng quay lại tấn công các mô ở các bộ phận khác nhau của cơ thể, dẫn đến những tổn thương ở đó, tạo nên bệnh. SLE gặp đa phần ở phụ nữ (90% các trường hợp chẩn đoán mắc bệnh), trong đó phụ nữ trong độ tuổi sinh nở (14–45 tuổi) dễ bị ảnh hưởng nhất. Các thuốc hiện tại như glucocorticoid hay thuốc ức chế miễn dịch chưa thể chữa khỏi bệnh, người ta đang hướng đến những phương pháp khác như liệu pháp tế bào gốc. Tế bào gốc trung mô (Mesenchymal stem cell – MSC) với đặc tính ức chế miễn dịch có thể đóng vai trò quan trọng trong việc ngăn ngừa các bệnh tự miễn. Trong các nghiên cứu tiền lâm sàng và thử nghiệm lâm sàng, cấy ghép MSC đã cho thấy kết quả khả quan trong việc cải thiện các triệu chứng của SLE. Mặc dù cơ chế của ghép MSC trong điều trị SLE chưa được hiểu biết đầy đủ, các nhà khoa học đã tập trung tìm hiểu về sự chuyển hóa các chất và tương tác của chúng trong cơ thể để tìm hiểu cơ chế bệnh sinh và điều trị bệnh trong ghép tế bào gốc. Trong một nghiên cứu mới công bố, các nhà khoa học ghép MSC từ dây rốn cho 20 người mắc SLE, với liều 1 triệu tế bào/kg cân nặng. Sau điều trị, các bệnh nhân được theo dõi chặt chẽ và các dấu hiệu cải thiện bệnh đã được chứng minh sau 180 ngày điều trị: giảm điểm hoạt động bệnh, giảm protein niệu và tốc độ lắng hồng cầu, tăng nồng độ bổ thể C3 và C4, tăng hemoglobin, tăng tiểu cầu. Khi thu thập và phân tích mẫu huyết tương trước và sau ghép MSC, nhóm nghiên cứu phát hiện 18.121 chất chuyển hóa (các phân tử nhỏ được tạo ra trong quá trình chuyển hóa), trong đó 1.152 chất thay đổi đáng kể sau điều trị. Nhìn chung, những thay đổi về từng chất chuyển hóa cụ thể có liên quan đến những cải thiện lâm sàng, đặc biệt là sự gia tăng nồng độ thiamine monophosphate (TMP) và asiaticoside. Sự thay đổi nồng độ TMP dự đoán thành công của điều trị ghép MSC, với mức tăng 35% cho thấy đáp ứng tốt với liệu pháp. Các nhà nghiên cứu kết luận rằng nồng độ thiamine monophosphate có thể là một dấu ấn sinh học tiềm năng để dự đoán hiệu quả của ghép MSC trong điều trị SLE. Kết quả này có thể giúp cải thiện việc chăm sóc bệnh nhân và định hướng cho các nghiên cứu trong tương lai, đưa đến những phương pháp điều trị SLE hiệu quả và cá nhân hóa hơn. --------- TÀI LIỆU THAM KHẢO Jiang X., et al. (2025). Metabolomic analysis suggests thiamine monophosphate as a potential marker for mesenchymal stem cell transplantation outcomes in patients with SLE. Lupus Science & Medicine, 12(1). DOI: 10.1136/lupus-2024-001197
23/01/2026
Ứng dụng tế bào gốc trung mô trong điều trị viêm khớp dạng thấp: đánh giá hiệu quả và tính an toàn từ một thử nghiệm giai đoạn I/II
Viêm khớp dạng thấp (Rheumatoid arthritis – RA) là bệnh lý mạn tính do rối loạn tự miễn trong cơ thể gây nên, bệnh xảy ra khi hệ thống miễn dịch tấn công nhầm vào các mô trong chính cơ thể. Khi bị hệ miễn dịch tấn công, trong màng hoạt dịch của các khớp sẽ xuất hiện tình trạng viêm, từ đó làm xuất hiện các biểu hiện đặc trưng như: Sưng, nóng, đỏ, đau, dần theo thời gian các khớp sẽ cứng lại thậm chí biến dạng khiến người bệnh mất khả năng vận động. Hiện tại chưa có phương pháp điều trị bệnh khỏi hoàn toàn, các biện pháp hiện tại nhắm cải thiện triệu chứng, duy trì cuộc sống bình thường. Cách thức điều trị hiện nay tập trung chủ yếu theo 2 cách: Điều trị triệu chứng để phục hồi cơ xương khớp và điều hòa miễn dịch để ngăn chặn sự tấn công của hệ thống miễn dịch. Điều hòa miễn dịch đang là phương pháp điều trị được quan tâm trên toàn thế giới, đặc biệt là phương pháp ghép tế bào gốc. Tế bào gốc trung mô (MSC) có khả năng ức chế miễn dịch và chống viêm, bao gồm ức chế sự tăng sinh của tế bào T (một nhóm tế bào miễn dịch của cơ thể) đối với các yếu tố gây dị ứng, ngăn chặn sự phát triển của các tế bào T gây độc tế bào. MSC có thể được thu nhận từ nhiều nguồn khác nhau như tủy xương, mô mỡ, dây rốn, nhau thai, dịch ối, răng sữa,... Bệnh nhân nam 68 tuổi, nhập viện điều trị sau 12 năm được chẩn đoán viêm khớp dạng thấp. Trước điều trị (A), bệnh nhân không thể giữ thẳng tay, nhưng sau 3 năm điều trị (B) đã có thể duỗi ra dễ dàng, các nốt thấp khớp quanh khớp dần mềm và mờ đi. Tế bào gốc trung mô mang lại những hi vọng lớn trong điều trị viêm khớp dạng thấp. Một nghiên cứu năm 2019 được thực hiện bởi Wang và cộng sự cho thấy liệu pháp tế bào gốc trung mô là một lựa chọn điều trị an toàn. 64 bệnh nhân viêm khớp dạng thấp ở độ tuổi 18-64 được truyền MSC dây rốn qua đường tĩnh mạch, sau đó theo dõi điều trị tới 3 năm. Trong vòng 8 tháng sau khi điều trị, tất cả các bệnh nhân đã cải thiện chế độ ăn ngủ và thể lực sau liệu pháp tế bào dựa trên các báo cáo của bệnh nhân. Sau 1 năm và 3 năm điều trị, các chỉ số huyết thanh đều cải thiện (chức năng gan, thận và xét nghiệm immunoglobulin không có bất thường; ESR, CRP, RF sau 1 năm và 3 năm điều trị và anti-CCP sau 3 năm điều trị đều thấp hơn so với trước điều trị). Chỉ số sức khỏe (HAQ) và chỉ số chức năng khớp (DAS28) giảm sau 1 năm và 3 năm điều trị so với trước điều trị. Những kết quả này đã cho thấy liệu pháp tế bào gốc trung mô dây rốn có tiềm năng là một lựa chọn điều trị an toàn, hiệu quả và khả thi cho bệnh nhân viêm khớp dạng thấp. --------- TÀI LIỆU THAM KHẢO Wang L., et al. (2019). Efficacy and safety of umbilical cord mesenchymal stem cell therapy for rheumatoid arthritis patients: a prospective phase I/II study. Drug design, development and therapy, 4331-4340.
23/01/2026
Trường hợp tiếp theo đẩy lùi HIV sau ghép tế bào gốc: tế bào NK có thể đóng vai trò then chốt
Tại Hội nghị bệnh AIDS châu Âu lần thứ 20 (EACS 2025) diễn ra tại Paris trong các ngày 15- 18/10/2025, các đại biểu đã nhận được thông tin cập nhật về một trường hợp chữa khỏi bệnh nhiễm HIV (trường hợp này đã được báo cáo tại hội nghị năm 2024 về tình trạng bệnh), trong đó có những phân tích đánh giá để đưa ra giả thuyết về cơ chế khỏi bệnh. Bệnh nhân này, được gọi là “bệnh nhân Berlin thứ hai” (phân biệt với “bệnh nhân Berlin” là người đầu tiên trên thế giới được chữa khỏi HIV), được ghép tế bào gốc vào cuối năm 2015 để điều trị bệnh bạch cầu dòng tủy cấp tính, đồng thời nhờ đó mà đã không tái phát HIV mặc dù đã ngừng điều trị 7 năm
23/01/2026
Liệu pháp tế bào gốc giúp đẩy lùi tình trạng đào thải miễn dịch sau ghép thận
Các nhà khoa học tại Mayo Clinic (Hoa Kỳ) đang thử nghiệm liệu pháp tế bào gốc để không dùng thuốc ức chế miễn dịch nhưng vẫn ngăn ngừa được tình trạng đào thải cơ quan sau cấy ghép thận. Nghiên cứu này sử dụng một sản phẩm tế bào đang được nghiên cứu (MDR-101), gồm các tế bào gốc tạo máu (Hematopoietic Stem Cell – HSC) đồng loại CD34+, kết hợp một lượng tế bào T CD3+ được hiến tặng từ người thân của người nhận cấy ghép thận, với mục tiêu cho phép bệnh nhân mang thể khảm hỗn hợp để ngăn ngừa tình trạng đào thải thông qua khả năng dung nạp miễn dịch đặc hiệu của người hiến, từ đó hướng tới giảm liều và cuối cùng ngừng sử dụng thuốc ức chế miễn dịch. Đây là một thử nghiệm lâm sàng đa trung tâm, giai đoạn 3, ngẫu nhiên có đối chứng để đánh giá sản phẩm tế bào MDR-101 có khả năng dung nạp miễn dịch so với chăm sóc tiêu chuẩn ở người nhận ghép thận. Những người trưởng thành nhận ghép thận từ anh chị em ruột còn sống phù hợp kháng nguyên bạch cầu người (Human Leukocyte Antigen – HLA), được phân ngẫu nhiên vào nhóm điều trị (n = 20) hoặc nhóm đối chứng (n = 10). Những người nhận điều trị được áp dụng phác đồ không gây hủy tủy và truyền MDR-101 (có nguồn gốc từ cùng người hiến thận) vào ngày 11, ngừng steroid vào ngày 10 và ngừng mycophenolate vào ngày 39, tiếp tục dùng thuốc ức chế miễn dịch tacrolimus cho đến ngày 180 và giảm dần đến 1 năm sau ghép thì ngừng hẳn nếu tỷ lệ tế bào khảm trong cơ quan tạo máu ≥5%. Nhóm đối chứng được ức chế miễn dịch theo chăm sóc tiêu chuẩn của cơ sở nghiên cứu. Kết quả cho thấy trong 20 người nhận thận ghép được truyền MDR-101, không có ai phát triển bệnh ghép chống chủ (Graft versus Host Disease – GvHD), với 19 người (95%) ngừng hoàn toàn việc sử dụng thuốc ức chế miễn dịch sau 1 năm, trong đó 15 người (75%) đạt được hiệu quả không phụ thuộc thuốc sau 2 năm ghép thận, chất lượng cuộc sống được cải thiện so với điều trị tiêu chuẩn. Kết quả nghiên cứu này đưa ra định hướng nhằm giảm nhu cầu sử dụng thuốc chống thải ghép suốt đời ở người được ghép thận, hứa hẹn một phương pháp điều trị an toàn và hiệu quả hơn cho các bệnh nhân ghép tạng, tiến tới loại bỏ gánh nặng dùng thuốc ức chế miễn dịch và cải thiện chất lượng của sống cho bệnh nhân. --------- TÀI LIỆU THAM KHẢO Kaufman D. B., et al. (2025). Induction of immune tolerance in living related human leukocyte antigen–matched kidney transplantation: A phase 3 randomized clinical trial. American Journal of Transplantation. DOI: 10.1016/j.ajt.2025.01.044.
23/01/2026
Công nghệ in 3D sinh học tạo nên bước tiến lớn hỗ trợ điều trị bệnh tiểu đường bằng liệu pháp tế bào gốc
Bệnh tiểu đường là một rối loạn chuyển hóa gây ra bởi sự rối loạn chức năng của tuyến tụy – cơ quan chịu trách nhiệm điều chỉnh lượng đường trong máu. Trong tuyến tụy, các tế bào đảo tụy tiết ra insulin để giảm lượng đường máu. Chúng điều chỉnh quá trình tiết insulin thông qua tương tác với các thành phần của chất nền ngoại bào (ECM) và tế bào mạch máu xung quanh. Trong trường hợp các tế bào đảo tụy bị tổn thương nghiêm trọng cần thay thế, việc sản xuất các tế bào này để sử dụng trong điều trị là điều rất khó khăn. Công nghệ tế bào gốc đã cung cấp một con đường đầy hứa hẹn để tạo ra các đảo tụy in vitro, tuy nhiên việc tái tạo chính xác môi trường vi mô và hốc mạch cần thiết để các đảo tụy này hoạt động giống như tuyến tụy thực sự là một trở ngại rất lớn. Trong một báo cáo công bố trên tạp chí Nature Communications tháng 3 năm 2025, các nhà khoa học tại Đại học Khoa học và Công nghệ Pohang (POSTECH) đã phát triển thành công một nền tảng cải tiến để điều trị bệnh tiểu đường bằng cách sử dụng công nghệ in sinh học 3D với mực in có nguồn gốc từ mô tụy. Loại mực in sinh học chuyên dụng này có tên PINE (Peri-islet Niche-like ECM), bao gồm ECM và các protein màng đáy (như laminin và collagen IV) được chiết xuất một phần từ mô tụy. Từ đó, nhóm nghiên cứu đã tạo nên nền tảng HICA-V (Human Islet-like Cellular Aggregates and Vasculature), sắp xếp chính xác các tế bào đảo tụy (được biệt hóa từ tế bào gốc) dọc theo cấu trúc mạch máu, mô phỏng cấu trúc của tuyến tụy trong cơ thể. Các tế bào đảo tụy được nuôi cấy trên nền tảng HICA-V này đã tăng cường sản xuất insulin và biểu hiện protein liên kết, thể hiện các đặc điểm chức năng tương đương với các đảo tụy trong cơ thể. Đồng thời, nền tảng này cũng đã mô phỏng thành công các phản ứng bệnh lý xảy ra ở bệnh nhân tiểu đường, ví dụ như biểu hiện gia tăng các gen gây viêm. (a) Sơ đồ minh họa quá trình phát triển mực sinh học PINE từ chất nền ngoại bào (ECM) có nguồn gốc từ mô tụy (pdECM) và các protein màng đáy (BM); (b) Sơ đồ minh họa quá trình in tổ chức tế bào đặc hiệu đảo tụy, sử dụng các tế bào đảo tụy có nguồn gốc từ tế bào gốc và tế bào nội mô (EC). Như vậy, sản phẩm của nhóm nghiên cứu đã thúc đẩy sự trưởng thành của các tiểu đảo tụy có nguồn gốc từ tế bào gốc – mang lại tiềm năng lớn để cải thiện hiệu quả của các liệu pháp cấy ghép đảo tụy điều trị bệnh tiểu đường, đồng thời tạo nên một công cụ hữu hiệu cho nghiên cứu bệnh và phát triển thuốc. --------- TÀI LIỆU THAM KHẢO Kim M., et al. (2025). Bioprinting of bespoke islet-specific niches to promote maturation of stem cell-derived islets. Nature Communications, 16(1), 1430. DOI: 10.1038/s41467-025-56665-5
23/01/2026
Hiểu rõ hơn về “chữa khỏi HIV do ghép tế bào gốc”
Các chuyên gia khẳng định ghép tế bào gốc không phải phương pháp chữa trị HIV và cơ chế đẩy lùi bệnh chưa được xác định
23/01/2026
Liệu pháp kháng thể có tiềm năng thay thế hóa – xạ trị trong phác đồ điều kiện hóa trước ghép tế bào gốc
Ghép tế bào gốc tạo máu (Hematopoietic Stem Cell Transplantation – HSCT) là quá trình cấy ghép tế bào gốc tạo máu từ tủy xương, máu ngoại vi, máu cuống rốn,… vào cơ thể người bệnh, để chữa các bệnh lý huyết học, miễn dịch, di truyền, ung thư,…
22/01/2026
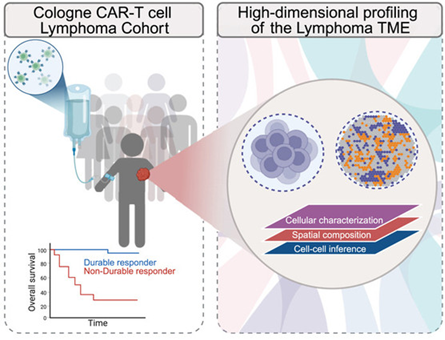
Phát hiện “hàng rào” tế bào làm giảm hiệu quả điều trị của liệu pháp CAR-T trong bệnh u lympho
Liệu pháp CAR-T sử dụng các tế bào T mang thụ thể kháng nguyên khảm (Chimeric Antigen Receptor – CAR) được thiết kế nhân tạo, nhờ đó chúng có thể phát hiện đặc hiệu và tiêu diệt các tế bào ung thư. CAR-T đã tạo nên bước đột phá trong điều trị nhiều bệnh lý huyết học ác tính, trong đó có u lympho tế bào B tái phát hoặc kháng trị - loại u lympho không Hodgkin phổ biến nhất. Tuy nhiên, có đến 50% số bệnh nhân được điều trị bằng liệu pháp này không duy trì khả năng đáp ứng ban đầu, hoặc tái phát sau điều trị, thậm chí tử vong. Cơ chế kháng CAR-T của bệnh này vẫn chưa được hiểu rõ hoàn toàn. Trong một nghiên cứu mới đăng trên tạp chí Cancer Cell tháng 5 năm 2025, các nhà khoa học đã phân tích sự khác biệt giữa những bệnh nhân có đáp ứng lâu dài so với nhóm kém đáp ứng với liệu pháp CAR-T. Nhóm tác giả đã phân tích mẫu u lympho của các bệnh nhân: giải trình tự RNA số lượng lớn để phân tích hoạt đột gen tổng thể của toàn bộ mẫu, giải trình tự RNA tế bào đơn để kiểm tra hoạt động gen của từng tế bào, tạo bản đồ vị trí các loại tế bào khác nhau và sự tương tác giữa chúng,… Mục tiêu cuối cùng là xác định các mục tiêu cụ thể trong môi trường vi mô của khối u có thể được điều chỉnh để cải thiện liệu pháp tế bào CAR-T. Nhóm nghiên cứu đã xác định được các tế bào đơn dòng tủy dương tính với CSF1R (một loại thụ thể có mặt trên bề mặt của các tế bào như microglia và đại thực bào, đóng vai trò quan trọng trong sự phát triển, sống sót và duy trì của microglia), còn gọi là tế bào LAMM, tăng đáng kể ở những bệnh nhân đáp ứng kém. Họ phát hiện ra rằng tế bào LAMM ức chế CAR-T thông qua con đường liên quan đến tín hiệu prostaglandin E2 (PGE2), sự tương tác giữa LAMM và một số thụ thể trên tế bào T làm vô hiệu hóa khả năng tăng sinh và tiêu diệt tế bào ung thư của CAR-T. Kết quả này cho thấy các tế bào LAMM hoạt động như một rào cản, bảo vệ khối u khỏi tế bào CAR-T. Tuy nhiên, hiện tại đã có thuốc được phê duyệt với tác dụng ức chế CSF1R (Sotuletinib hay BLZ-945), có thể phá vỡ hàng rào này, khi kết hợp với CAR-T trên mô hình chuột đã cải thiện hiệu quả điều trị một cách đáng kể. Đây có thể là bước đột phá trong chiến lược điều trị cho hàng nghìn bệnh nhân u lympho tế bào B kháng trị với liệu pháp CAR-T. TÀI LIỆU THAM KHẢO Stahl D., et al. (2025). CSF1R+ myeloid-monocytic cells drive CAR-T cell resistance in aggressive B cell lymphoma. Cancer cell. DOI: https://doi.org/10.1016/j.ccell.2025.05.013
22/01/2026
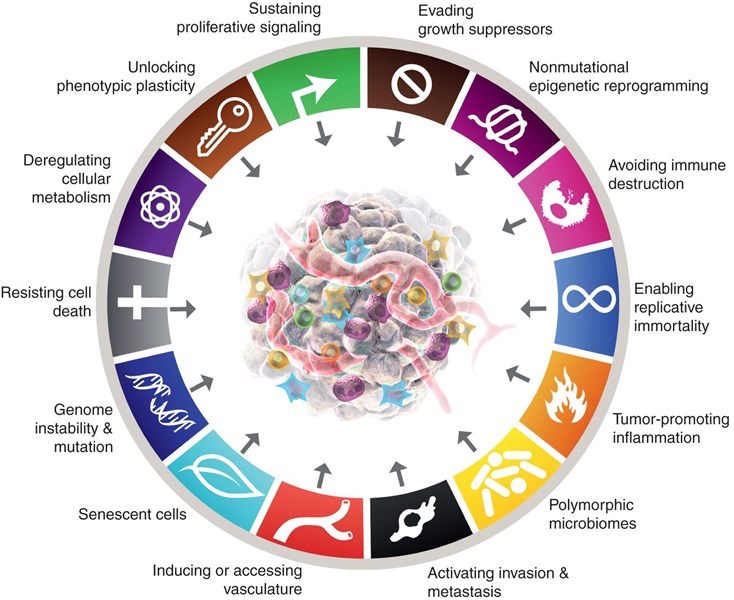
Những dấu hiệu đặc trưng của ung thư (The Hallmarks of Cancer)
1. Khái quát về ung thư Theo thống kê của Tổ chức Y tế Thế giới (WHO), ung thư là nguyên nhân gây tử vong đứng thứ hai trên toàn thế giới với khoảng 20 triệu ca mới mắc và gần 10 triệu người tử vong hằng năm, và có xu hướng ngày càng tăng trong những năm tiếp theo. Ung thư là tập hợp các bệnh lý liên quan đến việc tăng sinh tế bào mất kiểm soát, những tế bào đó có khả năng xâm lấn và phá hủy các mô khác trong cơ thể. Các tế bào ung thư có thể xuất hiện ở một khu vực sau đó lan ra các vùng khác, có thể tạo nên một khối u rõ ràng, nhưng đôi khi cũng có thể được phân bố đều (không tạo nên bướu rõ ràng). Có hơn 100 loại ung thư khác nhau, thường được gọi tên theo cơ quan mà nó phát sinh, ví dụ: ung thư đại trực tràng, ung thư tuyến giáp, ung thư tụy,… Ung thư cũng có thể được gọi theo loại tế bào hình thành chúng như ung thư biểu mô (carcinoma), ung thư mô liên kết (sarcoma), bệnh bạch cầu (leukemia),… Năm 2000, Robert Weinberg và Douglas Hanahan đã mô tả 6 đặc điểm mà hầu hết (nếu không muốn nói là tất cả) các loại ung thư ở người đều có, bên cạnh “đặc điểm hỗ trợ” các tế bào tiền ác tính có được 6 dấu hiệu đặc trưng đó, đây là bài viết gốc về “The Hallmarks of Cancer”. Những tiến bộ trong nghiên cứu ung thư đã thúc đẩy Weinberg và Hanahan cập nhật năm 2011, và gần nhất Hanahan đã xem xét lại danh sách này năm 2022. Những dấu hiệu đặc trưng của ung thư - mô tả mới nhất năm 2022 2. Mô tả đầu tiên năm 2000 về những dấu hiệu đặc trưng của ung thư - Tự cung cấp tín hiệu tăng trưởng: Khác với tế bào bình thường cần có tín hiệu tăng trưởng từ bên ngoài để nhân lên, các tế bào ung thư tự tạo ra hầu hết các tín hiệu tăng trưởng nhằm làm giảm đáng kể hoặc loại bỏ sự phụ thuộc của chúng vào các kích thích bên ngoài. - Không nhạy cảm với các tín hiệu ức chế tăng trưởng: Các tế bào bình thường được điều hòa bởi những tín hiệu kiểm soát, đẩy chúng ra khỏi chu kỳ tế bào và đi vào trạng thái nghỉ tạm thời hoặc biệt hóa sau lần nguyên phân cuối cùng. Các tế bào ung thư tránh các tín hiệu này bằng cách phá vỡ các điểm kiểm soát chu kỳ tế bào, giúp chúng có thể nhân lên vô hạn. - Tránh sự chết tế bào theo chương trình (Apoptosis): Apoptosis là một dạng chết tế bào theo chương trình đóng vai trò quan trọng trong việc loại bỏ các tế bào dư thừa, bị tổn thương hoặc những tế bào sai hỏng, bất thường. Những tế bào ung thư tránh được các cơ chế đưa chúng vào apoptosis và phát triển mất kiểm soát. - Tiềm năng sao chép vô hạn: Các tế bào bình thường sẽ ngừng phân chia tại một thời điểm nhất định do sự rút ngắn đầu mút nhiễm sắc thể (telomere). Các tế bào ung thư mất cơ chế kiểm soát đó nhờ sự kích hoạt enzyme telomerase để kéo dài đầu mút nhiễm sắc thế, giúp chúng phân chia vô hạn và trở thành tế bào bất tử. - Sự hình thành mạch máu: Khối u có thể giải phóng các tín hiệu kích thích tạo mạch máu, nhờ đó có nguồn cung cấp oxy và chất dinh dưỡng để chúng phát triển. - Xâm lấn mô và di căn: Tế bào ung thư có thể tách khỏi vị trí hoặc cơ quan ban đầu để xâm lấn các mô xung quanh và lan rộng (di căn) đến các bộ phận xa của cơ thể. Đây là yếu tố quyết định khối u lành tính hay ác tính, và là đặc tính cho phép chúng phát tán khắp cơ thể. Các tế bào ung thư phải trải qua vô số thay đổi để có được khả năng di căn, bắt đầu bằng sự xâm lấn cục bộ vào các mô xung quanh, sau đó xâm lấn các mạch máu, tồn tại trong môi trường khắc nghiệt của hệ tuần hoàn, thoát khỏi hệ thống này và bắt đầu phân chia trong mô mới. - Sự bất ổn của hệ gen (đặc điểm hỗ trợ): Các đặc điểm trên có được thông qua những thay đổi trong bộ gen của tế bào ung thư. Hiện nay người ta đã biết trong các tế bào ung thư có sự kích hoạt các gen gây ung thư (oncogene) và ức chế các gen kiềm chế khối u (tumor suppresor gene). Hiểu một cách đơn giản, một số kiểu gen đột biến mang lại lợi thế chọn lọc cho một số nhóm tế bào, và ung thư tiến triển trải qua nhiều bước là kết quả của một chuỗi những sự thích nghi được kích hoạt bởi sự tích lũy ngẫu nhiên các kiểu gen đột biến. Mô tả đầu tiên về những dấu hiệu đặc trưng của ung thư theo Hanahan và Weinberg năm 2000 3. Thế hệ tiếp theo về những dấu hiệu đặc trưng của ung thư (2011) - Thay đổi sự trao đổi chất của tế bào: Các tế bào bình thường sử dụng oxy để chuyển hóa glucose tạo ra năng lượng, còn các tế bào ác tính có xu hướng chuyển sang quá trình đường phân hiếu khí (được gọi là hiệu ứng Warburg), mặc dù hiệu quả tạo năng lượng thấp hơn nhưng nhanh hơn và tạo ra một số chất trung gian hỗ trợ quá trình tăng sinh nhanh chóng của tế bào ung thư. Ngoài ra, các tế bào ung thư có thể sử dụng lactate làm nguồn năng lượng chính của chúng. - Trốn tránh hệ thống miễn dịch: Các tế bào ung thư sử dụng nhiều chiến lược khác nhau cho phép chúng trốn tránh hệ thống miễn dịch của cơ thể. Một trong những cơ chế phổ biến nhất là biểu hiện protein PD-L1 và ức chế biểu hiện MHC I trên bề mặt khiến tế bào T không nhận diện được. - Phản ứng viêm thúc đẩy hình thành khối u (đặc điểm hỗ trợ): Viêm là phản ứng bảo vệ bình thường của cơ thể đối với những tác nhân gây bệnh hoặc tổn thương. Tuy nhiên, các bằng chứng đã cho thấy tác dụng ngược lại ở trong các khối u, phản ứng viêm là yếu tố tăng cường cho quá trình hình thành và tiến triển của khối u, có khả năng thúc đẩy sự phát triển của khối u mới phát triển thành ung thư hoàn chỉnh. Các tế bào viêm có thể giải phóng các chất hóa học có khả năng gây đột biến đối với các tế bào ung thư gần đó, đẩy nhanh quá trình chọn lọc di truyền của chúng theo hướng ác tính hóa cao hơn. Cập nhật về những dấu hiệu đặc trưng của ung thư theo Hanahan và Weinberg năm 2011 4. Những chiều hướng mới (2022) - Mở khóa tính mềm dẻo về kiểu hình: Các tế bào bình thường khi biệt hóa sẽ ngừng tăng sinh vĩnh viễn và chỉ thực hiện chức năng, ngược lại các tế bào ác tính tránh được sự biệt hóa và mở khóa cái được gọi là tính mềm dẻo kiểu hình để tiếp tục phát triển. Có nhiều cách để chúng làm điều này, ví dụ các tế bào đang tiến tới biệt hóa hoàn toàn sẽ giải biệt hóa để trở lại giống tế bào tiền thân, các tế bào ung thư có nguồn gốc từ tế bào chưa biệt hóa sẽ dừng quá trình biệt hóa, hoặc các tế bào đã được định hướng biệt hóa theo kiểu nhất định có thể chuyển chương trình (hoặc biệt hóa chéo) để hình thành những đặc điểm không liên quan đến định hướng biệt hóa ban đầu của chúng. - Các tế bào lão hóa: Lão hóa tế bào là một dạng ngừng tăng sinh thường không thể đảo ngược, bổ sung cho quá trình chết tế bào theo chương trình để vô hiệu hóa và loại bỏ kịp thời các tế bào bệnh, rối loạn chức năng hoặc không cần thiết. Tuy nhiên những bằng chứng hiện nay cho thấy các tế bào lão hóa là một thành phần quan trọng của vi môi trường khối u, trong một số bối cảnh nhất định chúng có thể kích thích sự phát triển của khối u và tiến triển ác tính. - Tái lập trình di truyền ngoại gen không đột biến (đặc điểm hỗ trợ): Di truyền ngoại gen (epigenetic) là thuật ngữ để chỉ những thay đổi về mặt di truyền trong kiểu hình tế bào nhưng không thay đổi về số lượng bản sao cũng như trình tự trong chuỗi DNA, bao gồm các cơ chế methyl hóa cytosine trên DNA, methyl hóa/acetyl hóa/phosphoryl hóa histone, hay RNA không mã hóa. Những cơ chế đó có thể điều hòa các gen để thay đổi biểu hiện gen, kích hoạt các gen chỉ hoạt động trong giai đoạn phôi sớm giúp tế bào liên tục phân chia, thay đổi vi môi trường khối u,… từ đó thúc đẩy sự phát triển của khối u. - Sự đa hình hệ vi sinh vật (đặc điểm hỗ trợ): Cơ thể chúng ta bị xâm chiếm bởi một lượng lớn các vi sinh vật (gần 40 nghìn tỷ tế bào) sống trong các cơ quan của cơ thể, gọi là microbiome, chúng đóng góp quan trọng đối với sức khỏe con người. Nhiều loài vi sinh vật trong số này gây nên những tác dụng chống lại hoặc thúc đẩy bệnh ung thư, cũng như phản ứng của cơ thể đối với các liệu pháp điều trị. Những bổ sung về những dấu hiệu đặc trưng của ung thư theo Hanahan năm 2022 5. Những thông tin trái chiều - Ngay sau phiên bản đầu tiên, Lazebnik đã có bài viết trên Nature Reviews Cancer năm 2010 chỉ ra rằng 5 trong số đó cũng là đặc điểm của khối u lành tính, chỉ có khả năng xâm lấn và di căn là đặc trưng cho các tế bào ác tính - Năm 2013, Sonnenschein và Soto cho rằng dữ liệu gốc cho hầu hết các dấu hiệu này còn thiếu, đồng thời chỉ ra ung thư là một căn bệnh ở cấp độ mô và các dấu hiệu ở cấp độ tế bào này gây nên những hiểu lầm về bản chất của ung thư. - Năm 2017, Fouad và Aanei cho rằng các dấu hiệu này có sự trùng lặp (tự cung cấp tín hiệu tăng trưởng và không nhạy cảm với tín hiệu ức chế tăng trưởng), hoặc chưa chính xác (apoptosis có xảy ra ở tế bào ung thư), các dấu hiệu đều được mổ xẻ kỹ và chỉ ra một số điểm bất hợp lý. TÀI LIỆU THAM KHẢO 1. Hanahan D., and Weinberg, R.A. (2000). The hallmarks of cancer. Cell, 100(1), 57-70. 2. Hanahan D., and Weinberg, R.A. (2011). Hallmarks of cancer: the next generation. Cell, 144(5), 646-674. 3. Hanahan D. (2022). Hallmarks of cancer: new dimensions. Cancer discovery, 12(1), 31-46. 4. Lazebnik Y. (2010). What are the hallmarks of cancer?. Nature Reviews Cancer, 10(4), 232-233. 5. Sonnenschein C., and Soto A.M. (2013). The aging of the 2000 and 2011 Hallmarks of Cancer reviews: a critique. Journal of biosciences, 38, 651-663. 6. Fouad Y. A., and Aanei C. (2017). Revisiting the hallmarks of cancer. American journal of cancer research, 7(5), 1016.
22/01/2026







