ỨNG DỤNG THEO BỆNH LÝ

Hướng đi mới của y học chính xác mở đường cho liệu pháp miễn dịch đối với bệnh nhi ung thư
Theo một nghiên cứu mới công bố trên tạp chí Cell, các nhà khoa học đã xác định hệ thống miễn dịch của trẻ em phản ứng như thế nào với các loại ung thư khác nhau tùy thuộc vào độ tuổi của chúng. Việc kích hoạt hệ thống miễn dịch đóng vai trò quan trọng đối với khả năng chống lại ung thư nhưng khác nhau giữa trẻ em và người lớn, sự hiểu biết về cách thức kích hoạt hệ thống miễn dịch ở trẻ em và sự điều chỉnh phản ứng miễn dịch ở bệnh nhi ung thư sẽ giúp các bác sỹ đưa ra hướng điều trị đúng cách.
22/01/2026
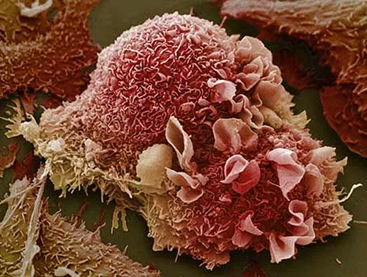
Tìm hiểu cách thức tế bào gốc khỏe mạnh tiến triển thành tế bào ung thư trên mô hình bệnh ung thư khoang miệng dương tính HPV
Ung thư khoang miệng (oral cancer) là loại ung thư tiến triển trong các mô ở vùng miệng như: môi, má, lợi, lưỡi, vòm miệng cứng hay mềm, sàn miệng, xoang và họng, trong đó lưỡi và môi là 2 cơ quan phổ biến nhất. Ung thư bắt nguồn từ các tế bào biểu mô, là lớp tế bào trên cùng lót khoang miệng. Khoảng 30% các trường hợp ung thư miệng là do virus u nhú ở người (Human Papilloma Virus – HPV) gây ra.
22/01/2026

Khám phá phương pháp tiềm năng ngăn chặn và điều trị hiệu quả u não ở trẻ em bằng cách ức chế tế bào gốc của nó
U não xuất hiện ở 2,5-4 trên 100.000 trẻ em có nguy cơ mỗi năm, trong đó khoảng 10-20% là u nguyên tủy bào (medulloblastoma). Đây là dạng u ác tính phổ biến ở trẻ em, xuất phát từ vùng tiểu não, phát triển từ các nguyên bào thần kinh có nguồn gốc từ ống thần kinh trong giai đoạn phôi thai. U nguyên tủy bào thường phát triển nhanh, lây lan sang các phần khác của não và tủy sống thông qua dịch não tủy, được WHO phân loại vào nhóm u ác tính độ IV.
22/01/2026
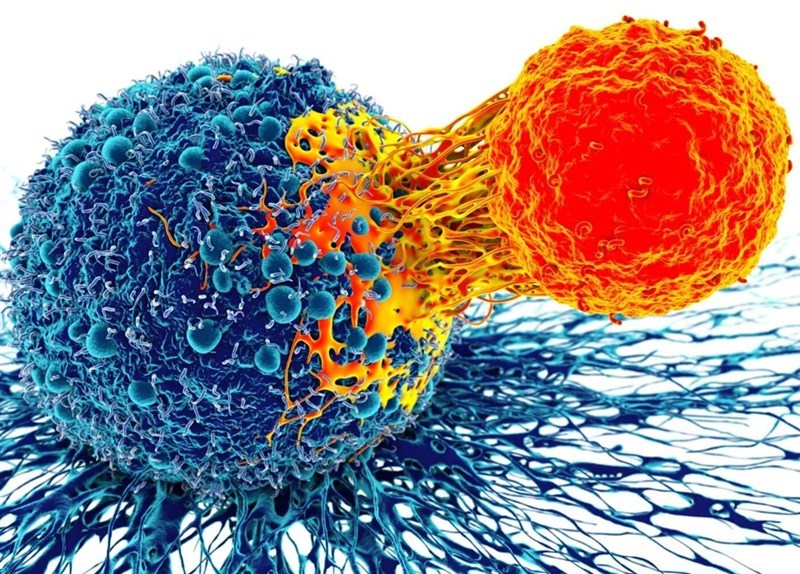
Liệu pháp tế bào cho các bệnh ung thư dạng u đặc đã đạt nhiều thành tựu đột phá trong năm 2024
Tháng 02/2024, FDA chấp thuận liệu pháp tế bào đầu tiên cho các khối u đặc tại Hoa Kỳ: tế bào lympho thâm nhiễm khối u (Tumor-infiltrating lymphocytes – TILs) để điều trị ung thư hắc tố. Các chuyên gia cho rằng đây chưa phải là đỉnh cao mà chỉ là bước khởi đầu quan trọng trong điều trị u đặc.
22/01/2026
Chỉ số lymphocyte giúp dự đoán khả năng đáp ứng với liệu pháp CAR-T trên bệnh nhân đa u tủy xương tái phát
Đa u tủy xương là ung thư của tương bào, những tế bào này sản xuất ra các globulin miễn dịch đơn dòng, xâm lấn và phá hủy xương lân cận. Phương pháp điều trị đa u tủy xương thường hóa trị thông thường, corticosteroid và một hoặc nhiều loại thuốc bổ sung như thuốc ức chế proteasome (ví dụ: bortezomib, carfilzomib, ixazomib), thuốc điều hòa miễn dịch (ví dụ: lenalidomide, thalidomide, pomalidomide) hoặc kháng thể đơn dòng (ví dụ: daratumumab, isatuximab, elotuzumab). Hầu như tất cả bệnh nhân mắc bệnh đa u tủy cuối cùng đều tái phát. Liệu pháp sử dụng tế bào T mang thụ thể kháng nguyên khảm (CAR-T) hướng đích kháng nguyên trưởng thành của tế bào B (BCMA) là một lựa chọn điều trị tiềm năng cho những bệnh nhân có bệnh tiến triển khi áp dụng các liệu pháp khác, tuy nhiên không phải tất cả bệnh nhân đều đáp ứng tốt với CAR-T. Một nghiên cứu tại New York (Hoa Kỳ) thực hiện trên 156 bệnh nhân mắc bệnh đa u tủy xương tái phát sau điều trị bằng ciltacabtagene autoleucel (Carvykti; Janssen, Legend Biotech) hoặc idecabtagene vicleucel (Abecma, Bristol Myers Squibb) đã chứng minh: xét nghiệm máu đơn giản đo số lượng tế bào lympho có thể dự đoán chính xác phản ứng với liệu pháp CAR-T. Theo đó, những bệnh nhân này được lấy máu xét nghiệm số lượng tế bào lympho tuyệt đối (ALC) ở thời điểm 5 ngày trước truyền và trong 15 ngày đầu tiên sau truyền BCMA CAR-T. Kết quả cho thấy những bệnh nhân có ALC cao hơn trong vòng 15 ngày sau truyền đạt được phản ứng tốt hơn đáng kể: những bệnh nhân có ALC tối đa trên 1,0×10^3/µL có sự cải thiện về thời gian sống thêm không bệnh tiến triển (PFS) cao hơn 5 lần so với những bệnh nhân dưới ngưỡng đó (trung bình 33,1 tháng so với 6 tháng). Những chỉ số về khả năng đáp ứng hoàn toàn hoặc một phần, thời gian đáp ứng cũng được cải thiện. Các yếu tố khác như độ tuổi, các liệu pháp trước đó, các đặc điểm có nguy cơ cao khác,… đã được xem xét đến nhưng ALC vẫn là yếu tố tiên lượng độc lập cho sự tiến triển của bệnh và tái phát sau CAR-T. Điều này có ý nghĩa quan trọng trong thực hành lâm sàng, giúp các bác sỹ có thể đưa ra nhận định về khả năng đáp ứng hay tái phát sớm của bệnh nhân, từ đó có quyết định điều trị hợp lý. Những bệnh nhân ALC tối đa ở mức thấp trong 15 ngày sau truyền sẽ đáp ứng kém với liệu pháp CAR-T, cần được lập kế hoạch điều trị tiếp theo – mặc dù những người này không có nhiều lựa chọn khác. Nhóm nghiên cứu đang tiếp tục nghiên cứu để tìm ra những dấu ấn có thể dự đoán khả năng đáp ứng ở thời điểm sớm hơn, hỗ trợ tốt hơn cho công tác điều trị. TÀI LIỆU THAM KHẢO Mejia Saldarriaga M., et al. (2024). Absolute lymphocyte count after BCMA CAR-T therapy is a predictor of response and outcomes in relapsed multiple myeloma. Blood Advances, 8(15), 3859-3869. DOI: https://doi.org/10.1182/bloodadvances.2023012470
22/01/2026
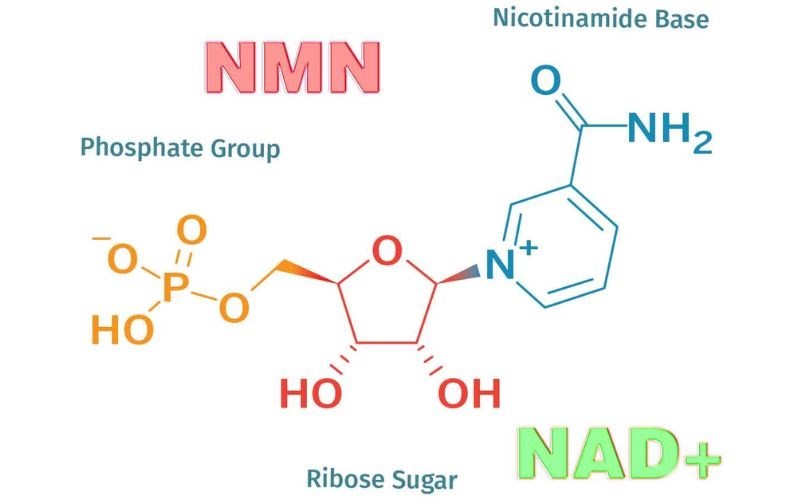
NAD thúc đẩy các tế bào miễn dịch phân chia nhanh hơn và có thể tăng cường hiệu quả của các liệu pháp tế bào miễn dịch chống ung thư
Nhóm nghiên cứu tại Bệnh viện Nhi Philadelphia (Hoa Kỳ) đã xác định được NAD (một chất chuyển hóa quan trọng trong tế bào) giúp định hướng phản ứng miễn dịch, đồng thời đưa ra triển vọng trong việc ứng dụng nó để cải thiện hiệu quả của liệu pháp miễn dịch cũng như tăng cường các chiến lược vaccine trong điều trị ung thư.
22/01/2026
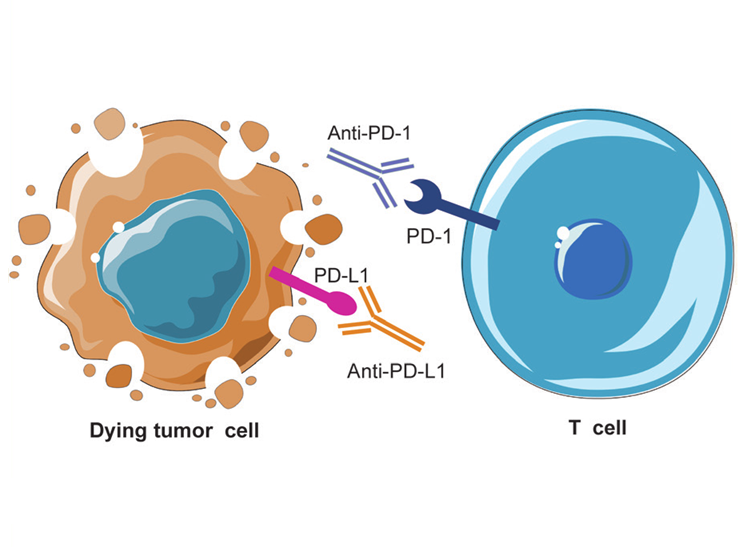
Hiệu quả điều trị ung thư của thuốc ức chế điểm kiểm soát miễn dịch được cải thiện khi kết hợp với xạ trị
Các tế bào miễn dịch như tế bào T, tế bào giết tự nhiên (NK) có khả năng nhận diện các tác nhân lạ và kích hoạt các phản ứng để tiêu diệt các tác nhân này, trong đó có tế bào ung thư. Trên bề mặt các tế bào miễn dịch có hiện diện các phân tử kiểm soát miễn dịch, sự tương tác giữa các phân tử này với nhau kích hoạt quá trình đáp ứng miễn dịch hoặc ức chế quá trình này như một cách bảo vệ cơ thể khỏi các bệnh tự miễn. Nhằm tránh bị tiêu diệt, tế bào ung thư cũng trình diện các phân tử kiểm soát miễn dịch tương ứng (ví dụ PD-L1 tương thích với PD-1, hình minh họa). Một chiến lược của liệu pháp miễn dịch hiện nay là những thuốc ức chế điểm kiểm soát miễn dịch, như các thuốc kháng PD-1 (Nivolumab, Pembrolizumab, Cemiplimab) hay kháng PD-L1 (Atezolimumab, Durvalumab, Avelumab) hoặc kháng CTLA-4 (Ipilimumab), nhằm ngăn chặn sự liên kết giữa các phân tử này, giúp tế bào miễn dịch nhận diện và tiêu diệt tế bào ung thư. Mặc dù vậy, tỷ lệ bệnh nhân đáp ứng với những thuốc này vẫn chưa được như kỳ vọng. Một thử nghiệm lâm sàng giai đoạn II tại Bệnh viện Đa khoa Massachusetts (Hoa Kỳ) trên 40 bệnh nhân ung thư đại trực tràng và 25 bệnh nhân ung thư tuyến tụy cho thấy: việc kết hợp bức xạ với các thuốc ức chế điểm kiểm soát miễn dịch có thể là một chiến lược để tăng hiệu quả điều trị. Khi được điều trị bằng bức xạ liều thấp kết hợp với Nivolumab và Ipilimumab (các thuốc miễn dịch có đích tác động khác nhau), 37% bệnh nhân ung thư đại trực tràng và 29% bệnh nhân ung thư tuyến tụy đã có đáp ứng điều trị (đáp ứng hoàn toàn hoặc một phần, hoặc bệnh ổn định không tiến triển). Kết quả lâm sàng này thực sự ấn tượng khi trước đây, tỷ lệ đáp ứng liệu pháp miễn dịch ở các loại ung thư này rất thấp. Phân tích chuyên sâu cho thấy, một số trình tự trong bộ gen người có nguồn gốc từ virus (HERV-K) có xu hướng được biểu hiện cao hơn ở các khối u đáp ứng với liệu pháp thử nghiệm. HERV-K có thể là dấu ấn được sử dụng cho các nghiên cứu trong tương lai để điều chỉnh phương pháp điều trị ung thư cá thể hóa. TÀI LIỆU THAM KHẢO Parikh A. R., et al. (2021). Radiation therapy enhances immunotherapy response in microsatellite stable colorectal and pancreatic adenocarcinoma in a phase II trial. Nature cancer, 2(11), 1124-1135.
22/01/2026
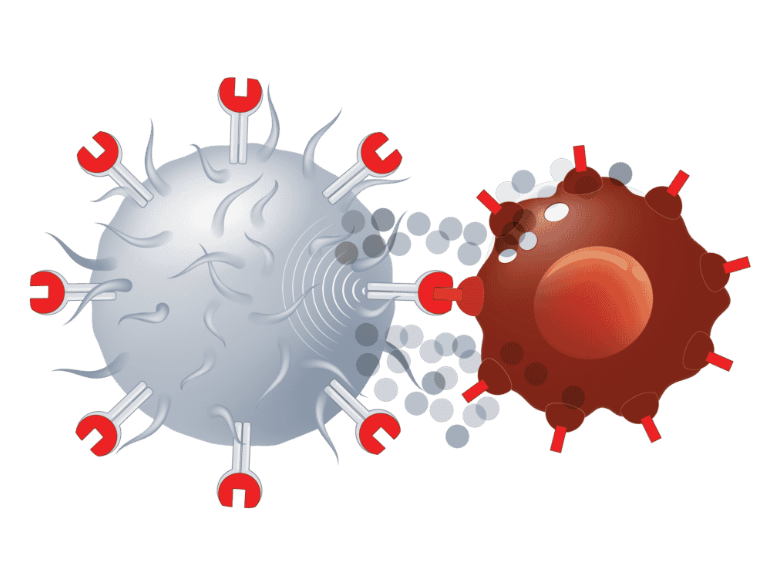
Loại bỏ CD5 trên tế bào CAR-T giúp tăng hiệu quả điều trị ung thư
Tế bào CAR-T là những tế bào miễn dịch lympho T đã được cải biến bằng cách gắn thêm vùng thụ thể kháng nguyên khảm (chimeric antigen receptors – CARs), vừa có khả năng nhận diện kháng nguyên ung thư nhất định, vừa có khả năng hoạt hóa tế bào T. Do đó, các tế bào CAR-T có thể chủ động tìm và tiêu diệt các tế bào ung thư một cách đặc hiệu với vùng CAR. Mặc dù vậy, tương tự đa số các phương pháp điều trị ung thư khác, hiệu quả của liệu pháp này bị giảm theo thời gian và phạm vi áp dụng hạn chế.
22/01/2026
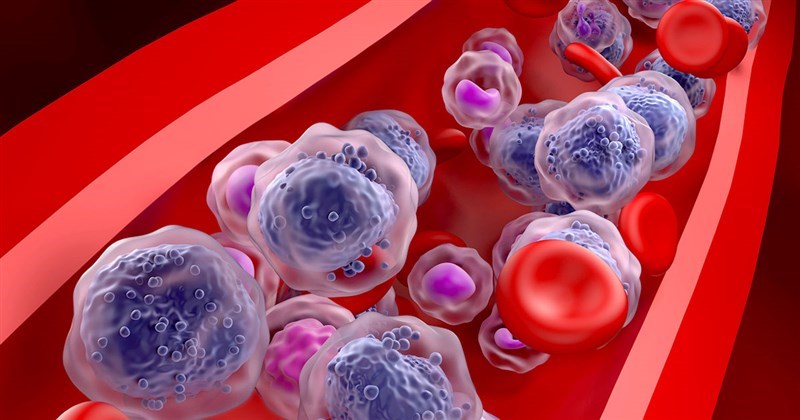
Triển vọng mới trong điều trị bệnh bạch cầu bằng cách hướng đến tế bào gốc của nó
Bệnh bạch cầu dòng tủy cấp tính (Acute myeloid leukemia – AML) là bệnh ung thư máu và tủy xương phổ biến nhất ở người lớn. Ở các bệnh nhân AML có sự tăng sinh mất kiểm soát của những tế bào chưa trưởng thành dẫn đến cạnh tranh thay thế các tế bào máu khỏe mạnh, làm rối loạn chức năng của các tế bào máu. AML là một trong những bệnh ung thư nguy hiểm nhất, gây tử vong cho khoảng 50% bệnh nhân dưới 60 tuổi và 85% bệnh nhân trên 60 tuổi, đồng thời gây gánh nặng kinh tế nặng nề cho gia đình và xã hội.
22/01/2026
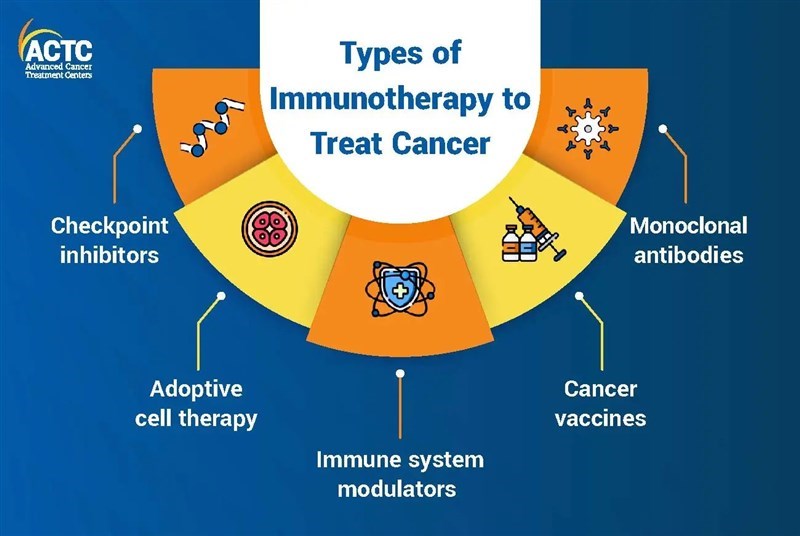
Liệu pháp miễn dịch trong điều trị ung thư
Liệu pháp miễn dịch (immunotherapy) là một phương pháp điều trị ung thư bằng cách kích thích và hoạt hoá hệ thống miễn dịch của con người chống lại ung thư. Đây là một loại liệu pháp sinh học, sử dụng các chất được tạo ra từ sinh vật sống để điều trị ung thư.
21/01/2026
Tế bào gốc có thể nắm giữ chìa khóa để chữa khỏi HIV
Tính đến cuối tháng 9/2025, đã có 10 trường hợp nhiễm HIV đã được chữa khỏi sau khi cấy ghép tế bào gốc, điều đó mang lại hy vọng về tác động toàn cầu đối với việc chăm sóc HIV.
21/01/2026

Hiệu quả tái tạo đối với lão hóa da mặt của tế bào gốc trung mô (MSC): nghiên cứu so sánh với phương pháp tiêm huyết tương giàu tiểu cầu (PRP)
Hiện nay, các phương pháp sử dụng tế bào gốc và huyết tương giàu tiểu cầu là những cách trẻ hóa da được quan tâm nhiều nhất. Nghiên cứu này so sánh hiệu quả của hai phương pháp đó trong tái tạo lão hóa da do ảnh hưởng của tia UV.
21/01/2026







