UNG THƯ VÀ HUYẾT HỌC
Kết quả cấy ghép tế bào gốc tạo máu ở 813 bệnh nhi thiếu máu Fanconi
Thiếu máu Fanconi là một bệnh di truyền hiếm gặp, không đồng nhất về mặt di truyền và lâm sàng, đặc trưng bởi các bất thường bẩm sinh và mắc phải, suy tủy xương và tăng nguy cơ mắc các bệnh ác tính. Thiếu máu Fanconi được công nhận là nguyên nhân phổ biến nhất gây ra suy tủy xương (bone marrow failure – BMF) di truyền hoặc thiếu máu bất sản (aplastic anemia – AA), có liên quan chặt chẽ với sự xuất hiện các bất thường tiền ác tính và có thể chuyển thành hội chứng loạn sản tủy (myelodysplastic syndrome – MDS) và bệnh bạch cầu dòng tủy cấp tính (acute myeloid leukemia – AML). Ghép tế bào gốc tạo máu (hematopoietic stem cell transplantation – HSCT) đồng loại được xác định là lựa chọn điều trị duy nhất cho bệnh nhân thiếu máu Fanconi liên quan đến BMF/AA và AML/MDS. Trong một báo cáo đăng trên tạp chí Blood (tạp chí thuộc Hiệp hội Huyết học Hoa Kỳ – American Society of Hematology – ASH), một nhóm nghiên cứu đã tiến hành phân tích hồi cứu đa trung tâm, trên 813 trẻ em mắc thiếu máu Fanconi ở 137 trung tâm, được ghép tế bào gốc tạo máu lần đầu trong giai đoạn năm 2010 – 2018, với 778 chỉ định suy tủy xương/thiếu máu bất sản (BMF/AA) và 35 chỉ định bệnh bạch cầu dòng tủy cấp tính/hội chứng loạn sản tủy (AML/MDS). Một số kết quả chính: - Thời gian mọc mảnh ghép (engraftment) trung bình với bạch cầu trung tính là 15 ngày, tỷ lệ tích lũy phục hồi bạch cầu trung tính ngày thứ 100 là 95%; thời gian mọc mảnh ghép trung bình với tiểu cầu là 20 ngày, tỷ lệ tích lũy phục hồi tiểu cầu ngày thứ 100 là 88%. - Tỷ lệ ghép thất bại (graft failure) nguyên phát là 2% (n = 17), thứ phát là 3% (n = 21). - Tỷ lệ sống tổng thể (overall survival – OS) sau 1 năm là 87%, sau 5 năm là 83%. OS thấp hơn đáng kể ở nhóm bệnh nhân ≥10 tuổi và nhóm ghép do AML/MDS so với các nhóm đối lập. OS tương đương giữa nhóm có người hiến phù hợp cùng hoặc không cùng huyết thống, đồng thời cao hơn nhóm có người hiến không phù hợp cùng hoặc không cùng huyết thống. - Tỷ lệ sống không biến cố (Event-free survival – EFS) sau 1 năm là 82%, sau 5 năm là 78%, cũng bị ảnh hưởng bởi các yếu tố tương tự như OS. - Tỷ lệ sống không GvHD và không tái phát (GVHD-free, relapse-free survival – GRFS) sau 1 năm là 73%, sau 5 năm là 70%, cũng bị ảnh hưởng bởi các yếu tố tương tự như OS và EFS. - Tổng cộng 123 ca tử vong trong quá trình theo dõi, với 93 trường hợp (76%) tử vong liên quan đến ghép: bệnh mảnh ghép chống chủ (Graft-versus-host disease – GvHD) n = 40 (33%), nhiễm trùng n = 34 (28%), suy cơ quan n = 7 (6%), tái phát n = 14 (11%),… - Bệnh mảnh ghép chống chủ (GvHD): tỷ lệ tích lũy GvHD cấp tính vào ngày thứ 100 sau ghép ở độ 2 – 4 là 23%, độ 3 – 4 là 12%, tỷ lệ tích lũy GvHD mạn tính sau 1 năm là 8%, sau 5 năm là 12%. - 16 bệnh nhân (2%) phát triển bệnh ác tính thứ phát (bệnh bạch cầu, hội chứng loạn sản tủy, bệnh u lympho,…) là điểm thường thấy ở bệnh nhân thiếu máu Fanconi. - Ảnh hưởng của liệu pháp huyết thanh: trong 441 bệnh nhân có người hiến phù hợp cùng huyết thống, các bệnh nhân sử dụng alemtuzumab có OS, EFS, GRFS cao hơn và tỷ lệ mắc GvHD thấp hơn, các bệnh nhân không sử dụng liệu pháp huyết thanh có OS, EFS, GRFS kém hơn và tỷ lệ mắc GvHD cao hơn (nhóm còn lại sử dụng Antithymocyte Globulin – ATG). Những dữ liệu này củng cổ thêm vai trò của ghép tế bào gốc tạo máu trong điều trị thiếu máu Fanconi, điển hình là các bệnh nhân suy tủy xương/thiếu máu bất sản (BMF/AA) và bệnh bạch cầu dòng tủy cấp tính/hội chứng loạn sản tủy (AML/MDS). Bệnh nhân nên được ghép sớm (<10 tuổi) nếu tìm được người hiến phù hợp, với người hiến phù hợp có hoặc không có quan hệ huyết thống, sử dụng alemtuzumab,… là một số yếu tố giúp tăng tỷ lệ thành công, giảm nguy cơ GvHD của ca ghép. Bệnh nhân thiếu máu Fanconi dường như có nguy cơ ung thư không thay đổi sau ghép tế bào gốc, dữ liệu này cần theo dõi lâu hơn để có đánh giá đầy đủ. TÀI LIỆU THAM KHẢO Lum S. H., et al. (2024). Outcomes of hematopoietic stem cell transplantation in 813 pediatric patients with Fanconi anemia. Blood, 144(12), 1329-1342. DOI: https://doi.org/10.1182/blood.2023022751
24/01/2026
Thảo luận về Orca-T, một liệu pháp tế bào mới có thể thay ghế ghép tế bào gốc tạo máu đồng loại (alloHSCT)
Ghép tế bào gốc tạo máu (Hematopoietic Stem Cell Transplantation – HSCT) là quá trình đưa các tế bào gốc tạo máu (HSC) (thường lấy từ tủy xương, máu ngoại vi hoặc máu cuống rốn) để nhân lên trong cơ thể bệnh nhân và sản xuất các tế bào máu bình thường. HSCT thường được thực hiện cho những bệnh nhân mắc một số bệnh về máu hoặc tủy xương, như đa u tủy xương, bệnh bạch cầu dòng tủy/dòng lympho cấp tính/mạn tính, một số loại u lympho,… HSCT có thể là tự thân (autologous HSCT – autoHSCT) trong đó sử dụng tế bào gốc của chính bệnh nhân, hoặc đồng loại (allogeneic HSCT – alloHSCT) với việc sử dụng tế bào gốc của người hiến, đôi khi một số tài liệu còn chia thêm nhóm “đồng gen” (syngeneic HSCT) là trường hợp sử dụng tế bào gốc của anh chị em song sinh cùng trứng. Trong thực hành alloHSCT, biến chứng nghiêm trọng được quan tâm nhất là bệnh mảnh ghép chống chủ (graft versus host disease – GvHD), xảy ra khi các tế bào lympho T có khả năng miễn dịch từ mô ghép của người hiến nhận diện các mô của người nhận là tác nhân lạ, và bắt đầu phản ứng miễn dịch chống lại chúng, dẫn đến tổn thương mô ở nhiều cơ quan khác nhau. GvHD có thể chia thành nhiều loại với những đặc điểm và chiến lược theo dõi, điều trị khác nhau: GvHD cấp tính cổ điển (xuất hiện trong vòng 100 ngày sau khi ghép với các triệu chứng lâm sàng điển hình của bệnh GVHD cấp tính); GVHD cấp tính dai dẳng, tái phát hoặc khởi phát muộn (biểu hiện các triệu chứng lâm sàng của GVHD cấp tính cổ điển nhưng sau 100 ngày kể từ ngày ghép); GvHD mạn tính cổ điển (xuất hiện sau 100 ngày ghép với các đặc điểm lâm sàng cổ điển của bệnh GVHD mạn tính), hội chứng chồng chéo (có thể xảy ra bất cứ lúc nào sau khi ghép với các đặc điểm của cả GVHD cấp tính và mạn tính). Trong nỗ lực hạn chế GvHD khi ghép đồng loại, Orca Bio đã phát triển liệu pháp Orca-T, được tạo ra từ các tế bào T điều hòa, tế bào gốc CD34+ và tế bào T thông thường thu nhận từ máu ngoại vi của người hiến phù hợp. Liệu pháp này đang được đánh giá trong thử nghiệm lâm sàng giai đoạn 3 Precision-T (NCT05316701) để đánh giá tính an toàn, hiệu quả và khả năng dung nạp so với alloHSCT thông thường ở những bệnh nhân mắc bệnh bạch cầu tủy cấp tính (AML), bệnh bạch cầu lympho cấp tính (ALL), hội chứng loạn sản tủy nguy cơ cao (MDS) và bệnh bạch cầu cấp tính kiểu hình hỗn hợp (MPAL). Trong một cuộc thảo luận trên OncLive, các khách mời là những nhà khoa học uy tín đã đưa ra những quan điểm về liệu pháp Orca-T, với những tính năng chính như: sự suy giảm tế bào T của người hiến giúp giảm thiểu nguy cơ mắc GVHD trong khi vẫn duy trì hiệu quả điều trị, phương pháp tiếp cận được cải biến để tăng cường khả năng mọc mảnh ghép và giảm các biến chứng do miễn dịch. Sử dụng Orca-T, bệnh nhân chỉ cần dùng một loại thuốc ức chế miễn dịch duy nhất là Tacrolimus thay vì dùng hỗn hợp nhiều thuốc như alloHSCT, giúp giảm độc tính liên quan đến các phác đồ ức chế miễn dịch rộng, đồng thời kiểm soát các phản ứng miễn dịch tốt hơn. Xem chi tiết bài thảo luận tại https://www.onclive.com/view/orca-t-a-new-allogeneic-cell-therapy---defining-orca-t-and-potential-advantages-compared-with-conventional-allohsct
24/01/2026
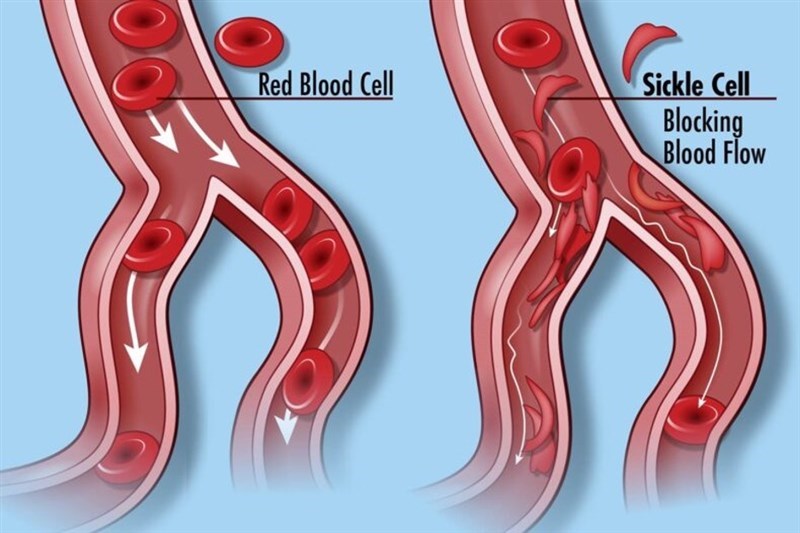
Hiệu quả điều trị bệnh hồng cầu hình liềm bằng phương pháp ghép tủy xương từ người hiến “phù hợp một nửa” (haploidentical)
Bệnh hồng cầu hình liềm (hay thiếu máu hồng cầu hình liềm – Sickle cell anemia) là một dạng thiếu máu di truyền do đột biến gen sản xuất hemoglobin – hợp chất không thể thiếu trong cấu trúc hồng cầu, dẫn đến không có đủ các tế bào hồng cầu khỏe mạnh để vận chuyển oxy trong cơ thể. Khác với người bình thường có các tế bào hồng cầu hình đĩa và linh hoạt, trong cơ thể người bệnh hồng cầu hình liềm, các tế bào hồng cầu trở nên cứng, dính và có hình dạng giống như lưỡi liềm hoặc mặt trăng khuyết, chúng không vận chuyển được oxy, đồng thời dễ bị mắc kẹt trong mạch máu làm chậm hoặc ngăn chặn các hồng cầu khác mang oxy đến các bộ phận của cơ thể. Liệu pháp tế bào và chỉnh sửa gen được kỳ vọng có thể điều trị bệnh một cách hiệu quả, trong đó một số sản phẩm đã được cấp phép chính thức, ví dụ Lyfgenia (lovotibeglogene autotemcel) và Casgevy (exagamglogene autotemcel) được FDA Hoa Kỳ phê duyệt cuối năm 2023. Theo một thử nghiệm được hoàn thành tại Anh mới đây, một quy trình cấy ghép tủy xương đã được chứng minh là an toàn và có thể chữa khỏi bệnh cho bệnh nhân mắc hồng cầu hình liềm, với chi phí thấp hơn so với các sản phẩm liệu pháp chỉnh sửa gen. Kết quả thử nghiệm mới được đăng tải trên tạp chí NEJM Evidence cuối tháng 02/2025. Đây là một thử nghiệm lâm sàng đa trung tâm giai đoạn II (mã số NCT03263559), nhãn mở, thử nghiệm phương pháp ghép tủy xương đơn bội cường độ giảm. Ghép tủy xương cung cấp cho bệnh nhân các tế bào gốc tạo máu được lấy từ người hiến khỏe mạnh, những tế bào này sẽ tạo ra những tế bào máu bình thường không mang đột biến gây ra hồng cầu hình liềm. Tủy xương được lấy từ người hiến tặng "phù hợp một nửa” (haploidentical) về các dấu hiệu miễn dịch với bệnh nhân để hạn chế sự đào thải miễn dịch, ví dụ như cha mẹ, con cái, anh chị em ruột, cháu trai/cháu gái, chú dì hoặc anh chị em họ của bệnh nhân. Điều này có nghĩa là các yếu tố miễn dịch có mặt và hoạt động trên các tế bào tủy của người hiến phải phù hợp với ít nhất một nửa các yếu tố đó trên các tế bào của người nhận. Trong số 54 người tham gia nghiên cứu (độ tuổi từ 15,5 đến 43,2), có 42 người được ghép tủy xương, trước khi ghép được hóa trị liều thấp và xạ trị toàn thân, sau ghép được dùng cyclophosphamide và một số loại thuốc khác (mycophenolate mofetil, sirolimus, fludarabine,…) để tránh mảnh ghép chống chủ (GvHD). Kết quả cho thấy sau 2 năm điều trị, 95% bệnh nhân vẫn còn sống sót, với 88% bệnh nhân sống sót không có biến cố bất lợi (chỉ có 2 người bị suy ghép nguyên phát, 1 người bị suy ghép thứ phát). Tỷ lệ mắc GvHD cấp tính độ 3-4 vào ngày 100 chỉ là 4,8%, trong khi tỷ lệ GvHD mạn tính sau 2 năm là 22,4%. Có 2 trong số 4 trường hợp tử vong được xác định do biến chứng nhiễm trùng sớm. Những kết quả trên chứng minh phương pháp này có tỷ lệ thành công rất cao, tương đương hoặc tốt hơn những sản phẩm liệu pháp gen đã được phê duyệt. Các nhà nghiên cứu cũng thực hiện so sánh phương pháp này và liệu pháp gen. Phương pháp ghép tủy xương có thể áp dụng với hầu hết các bệnh nhân hồng cầu hình liềm, trong khi liệu pháp gen đòi hỏi bệnh nhân cần trải qua hóa trị liều cao, có nguy cơ tổn thương một số cơ quan đích hoặc nguy cơ mắc bệnh bạch cầu, nên nhiều người không đủ điều kiện thực hiện. Một ca ghép tủy chỉ yêu cầu bệnh nhân nằm viện khoảng 8 ngày, còn đối với liệu pháp gen là 6-8. Số lần truyền máu trung bình sau khi ghép tủy xương là 6, thấp hơn nhiều con số 50 lần khi điều trị bằng liệu pháp gen. Tổng chi phí cho một ca ghép tủy xương thấp hơn 4-6 lần so với một ca điều trị bằng liệu pháp gen. Đây là một tín hiệu rất tích cực trong điều trị bệnh hồng cầu hình liềm, với tỷ lệ thành công cao, an toàn, chi phí thấp. Đồng thời, bệnh nhân được tăng cơ hội điều trị do không cần tìm người hiến hoàn toàn phù hợp miễn dịch mà chỉ cần cấy ghép phù hợp một nửa. TÀI LIỆU THAM KHẢO Kassim A. A., et al. (2025). Haploidentical bone marrow transplantation for sickle cell disease. NEJM evidence, 4(3). DOI: https://doi.org/10.1056/EVIDoa2400192.
24/01/2026

Thuốc điều trị ung thư cyclophosphamide giúp bệnh nhân ghép tế bào gốc tạo máu tránh được hiện tượng mảnh ghép chống vật chủ (GvHD)
Cấy ghép tế bào gốc tạo máu là phương pháp được áp dụng trong điều trị và hỗ trợ điều trị nhiều bệnh lý ung thư, nhằm khôi phục hệ thống tạo máu cho bệnh nhân. Độ tương thích của người hiến được xác định bằng tập hợp các dấu hiệu protein trên tế bào máu gọi là kháng nguyên bạch cầu người (Human Leukocyte Antigen – HLA), với 8 locus HLA–A, HLA–B, HLA–C, HLA–DR. Độ phù hợp hoàn toàn được xác định khi đạt điểm 8/8 (ngay cả trong những trường hợp anh chị em ruột, xác suất phù hợp hoàn toàn là 25%), còn độ phù hợp một phần được xác định khi đạt điểm 4/8 đến 7/8 (tỷ lệ gặp 50% ở anh chị em ruột). Khi ghép với độ phù hợp HLA thấp, các tế bào được ghép sẽ kích thích phản ứng miễn dịch trầm trọng ở bệnh nhân, gây nên tác dụng phụ nguy hiểm nhất (có thể gây chết người) của cấy ghép: mảnh ghép chống chủ (graft-versus-host disease – GvHD). Theo Viện Y tế Quốc gia Hoa Kỳ, GvHD thường xảy ra ở 60% đến 80% ca ghép mà người hiến tặng và người nhận không có quan hệ họ hàng. Theo một nghiên cứu được báo cáo tại Hội nghị 2024 của Hiệp hội Ung thư Lâm sàng Hoa Kỳ (ASCO), việc sử dụng một loại thuốc điều trị ung thư là cyclophosphamide vài ngày sau khi ghép tế bào gốc có thể giúp các trường hợp cấy ghép phù hợp một phần giảm thiểu hiện tượng GvHD. Khi theo dõi trên 70 bệnh nhân ung thư máu tiến triển được ghép phù hợp một phần có sử dụng cyclophosphamide, tỷ lệ bệnh nhân sống thêm toàn bộ (overall survival – OS) sau 1 năm là 79%, tương đương với những người được nhận sản phẩm cấy ghép từ người hiến phù hợp hoàn toàn. Sau một năm, 51% số bệnh nhân không còn phát hiện GvHD và không tái phát bệnh. Nhóm nghiên cứu mô tả dữ liệu này “rất ấn tượng”, đặc biệt là vì đã ghi nhận những bệnh nhân có nguy cơ cao và tuổi trung bình là 65. Những kết quả này đã mang lại cơ hội cho những bệnh nhân ung thư máu tìm được người hiến phù hợp hơn (đặc biệt là những người hiến trẻ, khỏe mạnh) và tỷ lệ ghép thành công cao hơn, khi mà sự phù hợp HLA không còn yêu cầu ở mức hoàn toàn. Ở mức độ phù hợp HLA ở mức 5/8 trở lên, trên 99% dân số sẽ tìm được người hiến tặng. Các nhà nghiên cứu cho biết cyclophosphamide ngày càng được sử dụng nhiều hơn trong thập kỷ qua để tăng cơ hội ghép tế bào gốc thành công từ người hiến tặng phù hợp HLA một phần. Hiện tại thử nghiệm lâm sàng giai đoạn II với hơn 300 bệnh nhân ở 30 cơ sở y tế tại Hoa Kỳ đang được thực hiện (mã số thử nghiệm NCT04904588, có thể tra cứu trên https://clinicaltrials.gov/). Những mục tiêu tiếp theo mà thử nghiệm hướng đến bao gồm tăng cường độ điều trị trước khi cấy ghép, áp dụng phác đồ cho các bệnh nhân nhi, tối ưu hóa việc sự dụng cyclophosphamide và kết hợp các phương pháp điều trị khác để giảm thiểu độc tính và nhiều vấn đề liên quan khác. TÀI LIỆU THAM KHẢO - Charlotte Schubert, “The Imperfect Match: Offering Transplants to More Blood Cancer Patients” (https://news.med.miami.edu/offering-transplants-to-more.../) - Al Malki M. M., et al. (2024). Post-transplant cyclophosphamide-based graft-versus-host disease prophylaxis following mismatched unrelated donor peripheral blood stem cell (PBSC) transplantation. Journal of Clinical Oncology 42 (16 suppl). Meeting Abstract: 2024 ASCO Annual Meeting I (https://ascopubs.org/doi/10.1200/JCO.2024.42.16_suppl.6503)
23/01/2026
Tình trạng kinh tế xã hội của người hiến tế bào ảnh hưởng đến kết quả cấy ghép tế bào gốc tạo máu (HSC) trong điều trị ung thư.
Theo một nghiên cứu mới công bố trên PNAS (Proceedings of the National Academy of Sciences) ngày 15/07/2024, tình trạng kinh tế xã hội của người hiến tế bào ảnh hưởng đến kết quả sức khỏe của bệnh nhân ung thư máu được ghép tế bào gốc tạo máu, bất kể tình trạng kinh tế xã hội của bệnh nhân ung thư. Nghiên cứu hồi cứu được thực hiện trên 2.005 bệnh nhân ung thư máu được điều trị bằng ghép tế bào gốc tạo máu ở 125 bệnh viện tại Hoa Kỳ, thời gian theo dõi là 120 tháng. Với việc phân tầng tương đối đồng đều các đối tượng nghiên cứu thành 4 nhóm, nghiên cứu đã chỉ ra những bệnh nhân được nhận tế bào từ người hiến có kinh tế xã hội ở nhóm khó khăn nhất đã giảm 9,7% tỷ lệ sống toàn trạng và tăng 6,6% tỷ lệ tử vong liên quan đến cấy ghép trong ba năm so với nhóm nhận tế bào từ người hiến có kinh tế xã hội ở nhóm tốt nhất. Kết quả này phù hợp với những nghiên cứu trước đây liên quan đến sự bất lợi về kinh tế xã hội với chức năng tế bào miễn dịch và quá trình tạo máu bị thay đổi, chúng thực sự tồn tại dai dẳng ngay cả khi tế bào được chuyển vào môi trường vật chủ mới (người được hiến tặng). Sự khác biệt về tỷ lệ sống sót toàn trạng (A), tỷ lệ tử vong liên quan đến điều trị (B), tỷ lệ sống thêm không bệnh (C) và tỷ lệ tái phát (D) được phân tầng theo tình trạng kinh tế xã hội của người hiến tặng (tình trạng kinh tế xã hội giảm dần từ Nhóm 1 đến Nhóm 4). Nhóm nghiên cứu mong muốn tiến hành những nghiên cứu sâu hơn để điều chỉnh các yếu tố sinh lý nhằm đưa ra những biện pháp giảm thiểu các kết quả bất lợi cho sức khỏe do tình trạng kinh tế xã hội gây ra. Đồng thời, phát hiện này cho thấy một trong những ảnh hưởng sâu sắc đến sức khỏe của sự bất bình đẳng xã hội và nêu bật nhu cầu cấp thiết về chăm sóc sức khỏe cộng đồng. TÀI LIỆU THAM KHẢO Turcotte L. M., et al. (2024). The health risk of social disadvantage is transplantable into a new host. Proceedings of the National Academy of Sciences, 121(30), e2404108121. DOI: https://doi.org/10.1073/pnas.240410812
23/01/2026
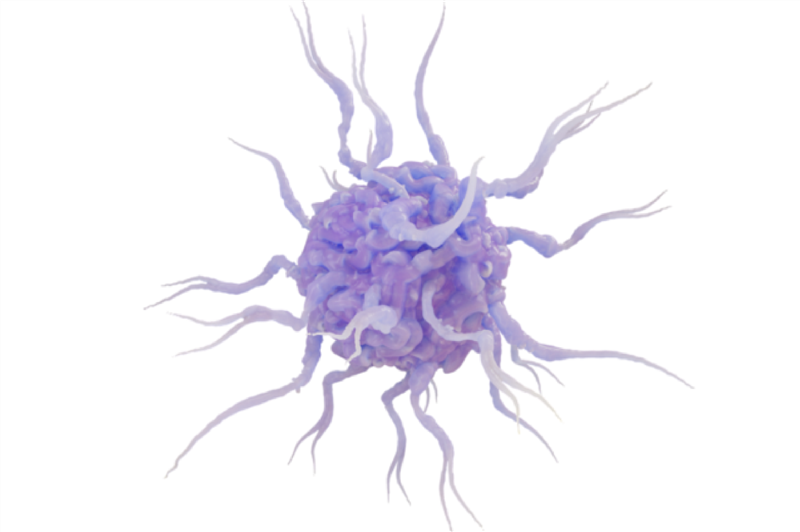
Tế bào đuôi gai biểu hiện CD5 đóng vai trò quan trọng đối với khả năng đáp ứng liệu pháp miễn dịch của bệnh nhân ung thư
Liệu pháp miễn dịch đã cho thấy hiệu quả đáng kinh ngạc trong điều trị ung thư. Ví dụ ở bệnh nhân ung thư hắc tố tiến triển (dạng ung thư da gây tử vong nhiều nhất), tỷ lệ sống sót sau năm năm đã tăng từ dưới 10% lên hơn 50% kể từ khi liệu pháp miễn dịch được áp dụng vào năm 2011. Tuy nhiên, tỷ lệ bệnh nhân ung thư đáp ứng với liệu pháp miễn dịch còn thấp. Hệ thống miễn dịch bảo vệ cơ thể chống ung thư bằng cách kích hoạt tế bào lympho T tiêu diệt tế bào khối u, nhưng không tấn công các tế bào khỏe mạnh nhờ hệ thống các điểm kiểm soát miễn dịch. Để đáp ứng lại, các tế bào khối u thao túng hệ thống điểm kiểm soát miễn dịch để tránh sự nhận diện bởi tế bào T. Một trong những hướng đi thành công nhất của liệu pháp miễn dịch ung thư là ức chế các điểm kiểm soát này để tế bào T nhận diện và tiêu diệt tế bào khối u, tuy nhiên tỷ lệ đáp ứng vẫn chưa được như kỳ vọng. Bằng cách phân tích dữ liệu từ The Cancer Genome Atlas - một cơ sở dữ liệu công khai với thông tin về 20.000 khối u đại diện cho 33 loại ung thư, các nhà khoa học Hoa Kỳ đã phát hiện ra rằng những bệnh nhân mắc các loại ung thư da, phổi, xương, mô mềm, vú và cổ tử cung sẽ có kết quả tốt hơn nếu họ có lượng tế bào đuôi gai biểu hiện CD5 cao hơn trong khối u. Tế bào đuôi gai là một thành phần của hệ thống miễn dịch trong cơ thể, giữ vai trò rất quan trọng với khả năng miễn dịch ung thư, có vai trò kích hoạt phản ứng của tế bào T để chống lại khối u ác tính, còn CD5 là một loại glycoprotein được biểu hiện trên bề mặt nhiều loại tế bào miễn dịch nhưng người ta chưa hiểu rõ về chức năng của nó. Các thí nghiệm tiếp theo với tế bào ung thư và mô hình chuột cho thấy tế bào đuôi gai biểu hiện CD5 cần thiết cho hoạt động chống lại tế bào ung thư, chúng kích thích tế bào T tăng sinh và thực hiện chức năng, từ đó làm tăng khả năng sống sót ở bệnh nhân và khả năng đào thải miễn dịch đối với khối u. Những tế bào này cũng đóng góp quan trọng vài việc phong tỏa điểm kiểm soát miễn dịch – một liệu pháp miễn dịch giúp tái kích hoạt phản ứng miễn dịch của chính cơ thể trong điều trị ung thư. IL-6 thúc đẩy sự gia tăng của các tế bào đuôi gai biểu hiện CD5, làm tăng khả năng kích hoạt tế bào T nhận diện và tiêu diệt tế bào khối u. Số lượng tế bào đuôi gai biểu hiện CD5 giảm ở các hạch bạch huyết làm giảm khả năng đáp ứng với các thuốc ức chế điểm kiểm soát miễn dịch, từ đó giảm hiệu quả tiêu diệt khối u của tế bào T. Nhóm nghiên cứu cũng phát hiện số lượng tế bào đuôi gai biểu hiện CD5 bên trong khối u có thể được sử dụng để đánh giá khả năng bệnh nhân nhận được lợi ích từ liệu pháp miễn dịch hay không. Việc làm tăng số lượng hoặc tăng cường hoạt động của tế bào đuôi gai biểu hiện CD5 có khả năng là giải pháp hỗ trợ hiệu quả trong điều trị ung thư bằng liệu pháp miễn dịch. Một trong những giải pháp để thực hiện điều này, các nhà khoa học đã chứng minh protein miễn dịch IL-6 giúp làm tăng lượng tế bào đuôi gai biểu hiện CD5. TÀI LIỆU THAM KHẢO He M., et al. (2023). CD5 expression by dendritic cells directs T cell immunity and sustains immunotherapy responses. Science, 379(6633), eabg2752. DOI: https://doi.org/10.1126/science.abg2752
23/01/2026
Tế bào NK có khả năng ghi nhớ và tấn công hiệu quả ung thư buồng trứng
Tế bào giết tự nhiên (natural killer – NK) là loại tế bào bạch cầu đóng vai trò quan trọng trong hệ miễn dịch bẩm sinh, có khả năng tiêu diệt các tế bào nhiễm virus và tế bào bất thường, bao gồm các tế bào có khả năng hình thành ung thư.
23/01/2026
Liệu pháp CAR-T đồng loại: Quy trình sản xuất với những triển vọng và thách thức để có thể ứng dụng lâm sàng
Liệu pháp CAR-T đồng loại mang đến hy vọng cho bệnh nhân ung thư về giải pháp dễ tiếp cận và chi phí thấp hơn so với CAR-T tự thân.
23/01/2026
Liệu pháp CAR-T đồng loại: giải pháp giúp bệnh nhân ung thư tăng khả năng tiếp cận phương pháp điều trị tiên tiến
1. Liệu pháp CAR-T tự thân cho các bệnh lý huyết học ác tính Bệnh lý huyết học ác tính là những bệnh lý ác tính bắt nguồn từ tủy xương và hệ bạch huyết, gồm 3 nhóm chính: bệnh bạch cầu (leukemia), u lympho (lymphoma) và đa u tủy xương (multiple myeloma). Các phương pháp điều trị như hóa trị, xạ trị, liệu pháp miễn dịch đang ngày càng có nhiều tiến bộ, tuy nhiên vẫn có tỷ lệ cao bệnh nhân tái phát hoặc kháng trị. Sự xuất hiện của liệu pháp tế bào T mang thụ thể kháng nguyên khảm (chimeric antigen receptor T-cell, CAR-T) đã tạo ra bước đột phá trong điều trị các bệnh lý huyết học ác tính. Những tế bào này mang cấu trúc CAR có khả năng nhắm đích vào một thụ thể xác định trên tế bào ung thư, nhờ đó mà phát hiện đặc hiệu và tiêu diệt hiệu quả tế bào ung thư. Từ năm 2017 đến nay, Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (the U.S. Food and Drug Administration – US FDA) và Cơ quan Dược phẩm Châu Âu (the European Medicines Agency – EMA) đã cấp phép cho 7 sản phẩm CAR-T tự thân (auto-CAR-T) trong điều trị các bệnh lý huyết học ác tính. Mặc dù vậy, chúng không phù hợp với tất cả các bệnh nhân, với 10-20% bệnh nhân không đáp ứng, trong khi quy trì sản xuất kéo dài không phù hợp với những bệnh nhân tiến triển nhanh, nguy cơ thất bại cao do giảm bạch cầu, chi phí lớn vì cần tối ưu cho từng bệnh nhân,… 2. Giải pháp CAR-T đồng loại Các tế bào CAR-T đồng loại (allo-CAR-T) đang được phát triển để giải quyết những thách thức liên quan đến liệu pháp CAR-T tự thân. Liệu pháp allo-CAR-T dựa trên việc sản xuất hàng loạt những tế bào CAR-T từ người hiến khỏe mạnh, nên có những lợi thế như: - Không gặp những hạn chế liên quan đến nguồn tế bào và độ khỏe mạnh của tế bào T: nguồn tế bào từ người hiến khỏe mạnh, tránh những bất thường về số lượng và chất lượng tế bào T ở các bệnh nhân mắc bệnh lý huyết học ác tính, không bị suy yếu bởi hóa – xạ trị ung thư,… - Sản xuất đồng loạt với quy mô lớn, sắp xếp với các liều điều trị xác định, nhờ đó sẵn sàng sử dụng ngay khi cần và chi phí sản xuất ở mức thấp - Kiểm soát chất lượng dễ dàng trước khi đóng gói sản phẩm, tăng hiệu quả của liệu pháp Trong thực hành lâm sàng, liệu pháp CAR-T đồng loại đã thể hiện những ưu điểm trong điều trị các bệnh ác tính về huyết học so với liệu pháp CAR-T tự thân như: - Hội chứng giải phóng cytokine (Cytokine Release Syndrome – CRS) ít nghiêm trọng hơn - Không cần các liệu pháp bắc cầu (được thực hiện giữa thời điểm gạn tách bạch cầu và truyền tế bào CAR-T) do không cần gạn tách tế bào từ bệnh nhân, nhờ đó giảm chi phí và tránh các tác dụng phụ trong quá trình điều trị - Loại bỏ nguy cơ biến đổi di truyền các tế bào của bệnh nhân trong quá trình sản xuất, tạo nên các nhóm tế bào kháng trị, đặc biệt ở các nhóm ung thư hung hãn như bệnh bạch cầu dòng lympho cấp tính tế bào B (B-cell Acute Lymphocytic Leukemia, B-ALL) Bệnh ghép chống chủ (Graft-versus-host disease, GvHD) và thải ghép đồng loại là những sự kiện đáng lo ngại khi ứng dụng allo-CAR-T. GvHD xảy ra khi tế bào T của người hiến xác định mô của người nhận là lạ và tấn công chúng, dẫn đến tình trạng viêm và tổn thương mô. Ngược lại, thải ghép đồng loại xảy ra khi hệ miễn dịch của vật chủ xác định tế bào T của người hiến là yếu tố lạ và tạo ra phản ứng miễn dịch để loại bỏ chúng. Khi sử dụng liệu pháp allo-CAR-T, các biện pháp hạn chế những biến chứng này cần được áp dụng, bao gồm xác định độ phù hợp miễn dịch, ức chế rộng rãi hệ miễn dịch của vật chủ (như sử dụng các thuốc kháng CD52 alemtuzumab, fingolimod), chỉnh sửa gen hoặc nguồn tế bào để loại bỏ GvHD và đào thải đồng loại,… 3. Triển vọng của liệu pháp allo-CAR-T Nhiều thử nghiệm lâm sàng áp dụng liệu pháp allo-CAR-T trong các bệnh lý ác tính huyết học như đa u tủy xương, lymphoma, bệnh bạch cầu và cho những kết quả khả quan. Trong hai thử nghiệm giai đoạn I mã số NCT02746952 và NCT02808442 sử dụng “UCART19” (tế bào CAR-T hướng đích CD19) trong điều trị bệnh bạch cầu dòng lympho cấp tính (ALL), kết quả cho thấy hiệu quả thu được rât khả quan, với tỷ lệ đáp ứng chung 48%, thời gian sống sót chung là 13,4 tháng. Trong thử nghiệm UNIVERSAL liên quan đến đa u tủy xương, 25% bệnh nhân đáp ứng hoàn toàn và 45,8% đáp ứng một phần. Những kết quả này cho thấy những tín hiệu lạc quan về hiệu quả của liệu pháp. Các tác dụng phụ được ghi nhận ở mức tương tự như CAR-T tự thân, cho thấy tính an toàn của CAR-T đồng loại trong các thử nghiệm lâm sàng. Trong điều trị các bệnh ung thư u đặc, liệu pháp CAR-T gặp nhiều hạn chế do tính chất của vi môi trường khối u. Việc sử dụng các công cụ chỉnh sửa gen, khả năng nhắm đích nhiều gen tế bào T mang lại cơ hội sản xuất CAR-T đồng loại có độ an toàn và hiệu quả cao hơn. Tiêu biểu trong số này có thể kể đến CYAD-01 kết hợp cùng thuốc kháng PD-1 (pembrolizumab) để tăng cường hiệu quả và độ bền đáp ứng ở bệnh nhân ung thư đại trực tràng di căn (thử nghiệm mã số NCT04991948). Sự kết hợp giữa sản phẩm CAR-T đồng loại và một tác nhân điều hòa miễn dịch khác (như thuốc ức chế điểm kiểm soát miễn dịch PD-1, CTLA-4) được coi là một chiến lược hiệu quả để ứng dụng liệu pháp này trong điều trị các dạng ung thư u đặc. TÀI LIỆU THAM KHẢO 1. Depil S., et al. (2020). ‘Off-the-shelf’ allogeneic CAR T cells: development and challenges. Nature reviews Drug discovery, 19(3), 185-199. DOI: https://doi.org/10.1038/s41573-019-0051-2 2. Bedoya M. D., Dutoit V., and Migliorini D. (2021). Allogeneic CAR T cells: an alternative to overcome challenges of CAR T cell therapy in glioblastoma. Frontiers in immunology, 12, 640082. DOI: https://doi.org/10.3389/fimmu.2021.640082 3. Chen S., and van den Brink M. R. (2024). Allogeneic “Off-the-Shelf” CAR T cells: Challenges and advances. Best Practice & Research Clinical Haematology, 37(3), 101566. DOI: https://doi.org/10.1016/j.beha.2024.101566 4. Sasu B. J., et al. (2024). Allogeneic CAR T cell therapy for cancer. Annual Review of Cancer Biology, 8(2024), 227-243. DOI: https://doi.org/10.1146/annurev-cancerbio-062822-023316 5. Mansoori S., et al. (2024). Recent updates on allogeneic CAR-T cells in hematological malignancies. Cancer Cell International, 24(1), 304. DOI: https://doi.org/10.1186/s12935-024-03479-y XEM THÊM - Cải biến di truyền giúp tăng cường hiệu quả liệu pháp tế bào miễn dịch trong điều trị ung thư: TCR-T và CAR-T https://www.facebook.com/share/p/18mRyiUvJb/ - Liệu pháp CAR-T – bước đột phá của liệu pháp tế bào trong điều trị ung thư https://www.facebook.com/share/p/1ACHF2K2wY/ - Một số giải pháp giảm chi phí cho liệu pháp CAR-T trong điều trị ung thư https://www.facebook.com/share/p/1AAvzahvNA/ - Liệu pháp CAR-T đồng loại cho thấy tính an toàn và hiệu quả trong điều trị ung thư huyết học https://www.facebook.com/share/p/1APRfhAno5/
23/01/2026
CAR-T mục tiêu kép: Một hướng đi tiềm năng của liệu pháp tế bào CAR-T
1. Một số hạn chế của liệu pháp CAR-T truyền thống (mục tiêu đơn) Liệu pháp tế bào T với thụ thể kháng nguyên khảm (chimeric antigen receptor T cell, CAR-T) là một liệu pháp miễn dịch mang tính cách mạng được sử dụng trong điều trị ung thư và một số bệnh lý khác. Phương pháp điều trị này bao gồm việc thu thập các tế bào T tự thân, chuyển gen mã hóa một thụ thể được biến đổi nhân tạo (cấu trúc CAR) để các tế bào T mang thụ thể này, nuôi cấy tăng sinh tế bào CAR-T thu được, truyền lại vào bệnh nhân để chúng nhận diện các kháng nguyên khối u cụ thể và tiêu diệt khối u hiệu quả với độ đặc hiệu cao. Mặc dù hiệu quả của liệu pháp CAR-T đã được chứng minh, nó vẫn có những hạn chế đáng kể như: - Hiệu quả: Tế bào CAR-T nhắm vào một kháng nguyên cụ thể trên tế bào ung thư, gây áp lực chọn lọc mạnh lên khối u, dẫn đến sự tái phát của các khối u không biểu hiện kháng nguyên này. Sự không đồng nhất đáng kể của khối u khiến CAR-T đơn mục tiêu khó đạt được hiệu quả ở nhiều loại tế bào khác nhau trong khối u. - Tính an toàn: Do tính không đồng nhất của khối u và sự chồng chéo kháng nguyên giữa tế bào ung thư và tế bào gốc tạo máu, CAR-T không phân biệt được hai loại tế bào này, nên có thể tấn công nhầm tế bào lành. Quy trình sản xuất CAR-T sử dụng vector chuyển gen là virus cũng mang đến những lo ngại. Nhiều tác dụng phụ của liệu pháp CAR-T cũng đã được ghi nhận trong các thử nghiệm lâm sàng, như bão cytokine, độc tính thần kinh trung ương,... 2. Liệu pháp CAR-T mục tiêu kép mang lại những lợi thế tiềm năng Liệu pháp CAR-T mục tiêu kép (dual-target CAR-T) nổi lên như một phương án tiềm năng để giảm thiểu một số nhược điểm hoặc tăng cường những lợi thế nhất định của liệu pháp CAR-T truyền thống. Việc nhắm mục tiêu vào đồng thời hai kháng nguyên có thể ngăn chặn hiệu quả sự tái phát, khi đó các nhà nghiên cứu có thêm cơ hội lựa chọn thêm một kháng nguyên phổ rộng trên các tế bào ung thư. Một số chiến lược thiết kế CAR-T mục tiêu kép phổ biến bao gồm: - Hỗn hợp hai sản phẩm CAR-T mục tiêu đơn: quá trình sản xuất riêng biệt với hai vector mang cấu trúc CAR khác nhau, tạo nên hai sản phẩm CAR-T khác nhau, được truyền cho bệnh nhân đồng thời hoặc truyền vào các ngày liên tiếp nhau - Tế bào T mang hai cấu trúc CAR riêng biệt (bicistronic): Sản phẩm tế bào CAR-T mang hai cấu trúc CAR riêng biệt đặc hiệu cho hai kháng nguyên khác nhau - Tế bào T mang cấu trúc CAR song song (tandem): Tế bào CAR-T mang hai cấu trúc CAR nối trực tiếp với nhau, với vùng nhận diện kháng nguyên nằm liên tiếp nhau trên cùng một vùng xuyên màng tế bào - Ngoài ra, một số chiến lược nâng cao để để tăng cường hiệu quả hoặc tính an toàn: cổng logic “OR” (tế bào CAR-T được hoạt hóa bởi một trong hai kháng nguyên trên tế bào khối u), “AND” (được kích hoạt khi nhận ra cả hai kháng nguyên), “NOT” (bị bất hoạt khi gặp một kháng nguyên trên tế bào bình thường),... 3. Một số kết quả thử nghiệm về CAR-T mục tiêu kép Nhiều liệu pháp CAR-T mục tiêu kép để điều trị các bệnh lý ác tính tế bào B và đa u tủy xương đã tiến đến giai đoạn tử nghiệm lâm sàng - Thử nghiệm lâm sàng giai đoạn I mã số NCT04007029 với tế bào CAR-T nhắm đến CD19 và CD20 để điều trị u lympho không Hodgkin cho thấy tỷ lệ đáp ứng tổng thể (overall response rate - ORR) 90%, tỷ lệ đáp ứng hoàn toàn (complete response - CR) là 70%, không ghi nhận sự phát triển độc tính toàn thân và hội chứng giải phóng cytokine (cytokine release syndrome – CRS) cao hơn cấp độ I, trái ngược đáng kể với hồ sơ an toàn của một số liệu pháp CAR-T mục tiêu đơn CD19 trong nhiều thử nghiệm lâm sàng khác. - Một nghiên cứu phân tích tổng cộng 219 bệnh nhân mắc bệnh bạch cầu cấp dòng lympho (Acute Lymphoblastic Leukemia – ALL) tế bào B tham gia vào thử nghiệm lâm sàng sửu dụng CAR-T mục tiêu đơn CD19 (NCT03919240) hoặc mục tiêu kép CD19 và CD22 (NCT03614858) cho thấy: những bệnh nhân được điều trị bằng liệu pháp CAR-T mục tiêu kép đạt tỷ lệ đáp ứng hoàn toàn cao hơn so với những bệnh nhân được điều trị bằng liệu pháp mục tiêu đơn (98% so với 83%). - Nhiều thử nghiệm lâm sàng khác đang thực hiện cho thấy liệu pháp CAR-T mục tiêu kép đã chứng minh hiệu quả và tính an toàn trong bệnh bạch cầu, u lympho, đa u tủy xương,… 4. Hướng đi trong tương lai, triển vọng và thách thức Mặc dù vậy, liệu pháp CAR-T mục tiêu kép vẫn có một số hạn chế chính: - Vấn đề kháng trị: chưa hoặc không giải quyết được các cơ chế kháng điều trị khác ngoài cơ chế mất kháng nguyên đã nêu ở phần 1 (tái phát ung thư với các tế bào ác tính không biểu hiện kháng nguyên đích của CAR-T) - Chưa có đủ bằng chứng về tính an toàn và khả năng hoạt động trong cơ thể của CAR-T mục tiêu kép (đặc biệt là một số nghiên cứu cho thấy CAR-T mục tiêu kép gây nên những độc tính về huyết học khi điều trị đa u tủy xương, ví dụ giảm tiểu cầu) Kích thước của hai cấu trúc CAR lớn hơn nên sản xuất khó khăn hơn so với CAR-T truyền thống, bao gồm những khó khăn trong lựa chọn và thiết kế vector chuyển gen, hiệu quả chuyển gen thấp hơn,… Vì vậy, để có thể ứng dụng cho lâm sàng, những hướng đi sắp tới của CAR-T mục tiêu kép bao gồm tối ưu hóa cấu trúc và quy trình sản xuất, lựa chọn các mục tiêu kháng nguyên phù hợp cho từng chỉ định bệnh, đánh giá chi tiết về hồ sơ an toàn và hiệu quả của liệu pháp,… Để thực hiện được những mục tiêu đó đòi hỏi sự hợp tác của các nhóm nghiên cứu khác nhau, nhằm phát triển những giải pháp hiệu quả mang lại lợi ích cho cộng đồng toàn cầu. TÀI LIỆU THAM KHẢO 1. Xie B, et al. (2022). Current Status and Perspectives of Dual-Targeting Chimeric Antigen Receptor T-Cell Therapy for the Treatment of Hematological Malignancies. Cancers (Basel) 14(13): 3230. DOI: https://doi.org/10.3390/cancers14133230 2. Yang J., et al. (2024). Dual-targeted CAR T-cell immunotherapies for hematological malignancies: latest updates from the 2023 ASH annual meeting. Experimental Hematology & Oncology 13, 25. DOI: https://doi.org/10.1186/s40164-024-00485-8 3. Zhang C, et al. (2025). Advancements and Future Directions of Dual-Target Chimeric Antigen Receptor T-Cell Therapy in Preclinical and Clinical Studies. Journal of Immunology Research 2025: 5845167. https://doi.org/10.1155/jimr/5845167 XEM THÊM - Cải biến di truyền giúp tăng cường hiệu quả liệu pháp tế bào miễn dịch trong điều trị ung thư: TCR-T và CAR-T https://www.facebook.com/share/p/18mRyiUvJb/ - Liệu pháp CAR-T – bước đột phá của liệu pháp tế bào trong điều trị ung thư https://www.facebook.com/share/p/1ACHF2K2wY/ - FDA loại bỏ các chiến lược đánh giá và giảm thiểu rủi ro cho liệu pháp CAR-T tự thân trong điều trị ung thư https://www.facebook.com/share/p/19ZgegsBHs/ - CAR-T in vivo: chiến lược mới với tế bào CAR-T được sản xuất ngay trong cơ thể bệnh nhân https://www.facebook.com/share/p/1BJoWi2Kgp/ - Một số giải pháp giảm chi phí cho liệu pháp CAR-T trong điều trị ung thư https://www.facebook.com/share/p/1AAvzahvNA/
23/01/2026

Một số giải pháp giảm chi phí cho liệu pháp CAR-T
Liệu pháp CAR-T được coi là bước đột phá của liệu pháp tế bào trong điều trị ung thư, mang đến giải pháp điều trị hiệu quả cho một số bệnh ung thư máu, ngoài ra cũng có những tiến bộ tích cực đối với u đặc và các bệnh tự miễn. Tính đến thời điểm hiện tại, đã có 7 sản phẩm được Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (The U. S. Food And Drug Administration – US FDA) và Cơ quan Dược phẩm Châu Âu (European Medicines Agency – EMA) phê duyệt, bao gồm Kymriah, Yescarta, Tecartus, Breyanzi, Aucatzyl, Abecma, Carvykti. Ngoài ra, một số sản phẩm khác được cấp phép ở Trung Quốc (Relma-cel, Yuanruida, Fucaso, Zevor-cell), Ấn Độ (NexCAR19, Qartemi),… đều thuộc các công ty ở quốc gia sở tại. Tuy nhiên, chi phí của phương pháp điều trị này khá cao, chỉ riêng quy trình điều chế CAR-T tại Hoa Kỳ đã tiêu tốn khoảng 300.000 USD trở lên và tăng theo từng năm theo giá nguyên liệu, nếu tính thêm các chi phí khác trong suốt quá trình nằm viện và theo dõi bệnh nhân thì sức ép kinh tế trở nên rất nặng nề. Để giải quyết vấn đề này, nhiều chiến lược đã được đề ra, sau đây là một số giải pháp chính. 1. Phát triển liệu pháp CAR-T in vivo Quy trình CAR-T thông thường (ex vivo) được thực hiện qua nhiều bước phức tạp: thu thập tế bào T từ bệnh nhân, biến đổi gen của chúng để biểu hiện cấu trúc CAR, nuôi cấy tăng sinh tế bào CAR-T, kiểm tra chất lượng và truyền sản phẩm trở lại bệnh nhân. Tổng thời gian thường mất 2–4 tuần, đòi hỏi những yêu cầu đặc biệt về cơ sở vật chất và trang thiết bị, dẫn đến chi phí khá lớn. Đối với CAR-T in vivo, các tế bào CAR-T được tạo ra trực tiếp trong cơ thể bệnh nhân, bằng cách đưa vào trong người bệnh các hạt nano hoặc vector virus nhắm trúng đích tế bào T, chúng sẽ chuyển gen và biểu hiện cấu trúc CAR, tạo nên tế bào CAR-T có thể nhân lên tự nhiên trong cơ thể. Phương pháp này có thể làm giảm chi phí và độ phức tạp so với CAR-T ex vivo, đồng thời có những ưu thế tiềm năng như tránh nguy cơ nhiễm trùng cơ hội và độc tính toàn thân cho người bệnh. 2. Phát triển các liệu pháp CAR-T đồng loại Tất cả các liệu pháp CAR-T được phê duyệt hiện tại đều là tự thân (nghĩa là tế bào T được lấy từ bệnh nhân để sau đó điều trị cho chính họ), đa số các sản phẩm thử nghiệm cũng đều như vậy. Vì thế, mỗi lô sản xuất CAR-T mang một đặc điểm riêng được cá nhân hóa cho từng bệnh nhân, và chỉ sử dụng được cho chính người bệnh đó, làm tăng chi phí sản xuất. Các nhà khoa học đã và đang thực hiện những chiến lược để sản xuất CAR-T đồng loại (“off-the-shelf” allogeneic CAR-T), trong đó tế bào T được lấy từ người hiến khỏe mạnh, hoặc từ máu cuống rốn, hoặc được biệt hóa từ tế bào gốc, sau đó cải biến và nuôi cấy tăng sinh và lưu trữ đông lạnh, sẵn sàng truyền cho bệnh nhân khi cần. Quá trình sản xuất hàng loạt với số lượng lớn giúp giảm chi phí đáng kể, đồng thời mang đến những lợi thế khác như chất lượng đồng nhất, sẵn sàng sử dụng ngay cho bệnh nhân khi có chỉ định mà không cần chờ đợi quá trình cải biến trong phòng thí nghiệm. 3. Sản xuất CAR-T tại các quốc gia có chi phí thấp Trong các sản phẩm CAR-T được cấp phép trên thế giới, 7 sản phẩm được phê duyệt tại Hoa Kỳ và Châu Âu có chi phí khá cao, ngược lại những sản phẩm tại Ấn Độ và Trung Quốc ở mức giá được coi là thấp hơn nhiều. Ví dụ, Relma-cel khoảng 1 triệu Nhân dân tệ (khoảng 140.000 USD), Zevor-cel khoảng 160.000 USD, NexCAR19 khoảng 50.000 USD. Mức chi phí thấp do nhiều nguyên nhân, bao gồm chi phí xây dựng cơ sở sản xuất, trang thiết bị, nguyên liệu, và đặc biệt là chi phí nhân công cũng như công nghệ tạo vector chuyển gen của từng công ty. 4. Chuyển giao công nghệ và sản xuất tại chỗ Đây là giải pháp đầy hứa hẹn, cho phép các bệnh viện có thể sản xuất liệu pháp CAR-T tại chỗ để sử dụng cho bệnh nhân, tránh việc phải vận chuyển mẫu đến phòng thí nghiệm sản xuất, hoặc vận chuyển bệnh nhân đến cơ sở y tế thuận tiện (thường các phòng thí nghiệm hoặc cơ sở y tế này ở nước ngoài) làm tăng chi phí cho quá trình điều trị. Ví dụ, hãng Miltenyi Biotec có trụ sở tại Đức đã triển khai nhà máy và chuyển giao công nghệ (gồm hệ thống sản xuất CAR-T là CliniMACS Prodigy và hệ thống vector chuyển gen) đến nhiều quốc gia như Áo, Anh, Ireland, Hàn Quốc, Ấn Độ,… (tại Việt Nam, Hệ thống Y tế Vinmec cũng tiếp nhận chuyển giao công nghệ này). Về lâu dài, việc sản xuất tại chỗ sẽ giúp giảm đáng kể chi phí sản xuất CAR-T, khi lượng bệnh nhân đủ lớn. Tuy nhiên ở thời điểm ban đầu, chiến lược này còn gặp nhiều thách thức, bao gồm quy định triển khai liệu pháp ở quốc gia sở tại, thử nghiệm đánh giá hiệu quả trên bệnh nhân của từng công nghệ/giải pháp (ngược lại với các sản phẩm CAR-T thương mại đã có dữ liệu lâm sàng đủ tin cậy trước khi được cấp phép), chi phí nguyên liệu và nhân công tại quốc gia sở tại,… 5. Một số giải pháp khác Một số giải pháp chuyên sâu khác vẫn đang được các nhà khoa học nghiên cứu, bao gồm cải tiến quy trình (tìm vector thay thế vector virus, tăng hiệu suất để giảm thời gian nuôi cấy tế bào), chuyên môn hóa quá trình sản xuất đến nhiều công ty thay vì tập trung như hiện tại, tìm các dấu ấn sinh học để nâng cao hiệu quả của CAR-T,…
23/01/2026
Liệu pháp CAR-T đồng loại cho thấy tính an toàn và hiệu quả trong điều trị ung thư huyết học
Liệu pháp tế bào T mang thụ thể kháng nguyên khảm (chimeric antigen receptor T-cell, CAR-T) đã khẳng định được hiệu quả trong điều trị các bệnh lý huyết học ác tính, với 7 sản phẩm CAR-T tự thân được cấp phép tại Hoa Kỳ và Châu Âu để điều trị y lympho, bệnh bạch cầu, đa u tủy xương. Quy trình liệu pháp CAR-T tự thân thường bao gồm các bước chính: thu thập tế bào T từ máu của chính bệnh nhân và chuyển gen để biểu hiện cấu trúc CAR trên tế bào T, nuôi cấy tăng sinh tế bào CAR-T thu được và truyền cho bệnh nhân. Ngoài ra, các nhà khoa học đã và đang thực hiện các chiến lược để sản xuất sản phẩm đồng loại (“off-the-shelf” allogeneic CAR-T), với nhiều lợi thế như sản xuất đồng loạt giúp giảm chi phí, chất lượng đồng nhất, không cần chờ đợi quá trình cải biến và nuôi cấy tăng sinh như phương pháp tự thân,... Không giống như phương pháp truyền thống, những tế bào T trong sản phẩm đồng loại được thu nhận từ người hiến khỏe mạnh, hoặc máu cuống rốn, hoặc biệt hóa từ tế bào gốc đa tiềm năng, sau đó cải biến để biểu hiện cấu trúc CAR trên bề mặt tế bào, nuôi cấy tăng sinh CAR-T và lưu trữ đông lạnh, sẵn sàng truyền cho bệnh nhân khi cần. Ngày 03 tháng 11 năm 2025, Công ty Công nghệ sinh học Caribou Biosciences đã công bố những dữ liệu lâm sàng về hai sản phẩm CAR-T đồng loại đang được họ phát triển: Vispa-cel trong điều trị u lympho không Hodgkin tế bào B tái phát hoặc kháng trị (thử nghiệm lâm sàng ANTLER), và CB-011 trong điều trị đa u tủy xương (thử nghiệm lâm sàng CaMMouflage). Vispacabtagene regedleucel (Vispa-cel, trước đây là CB-010), là sản phẩm CAR-T đồng loại kháng CD19, đồng thời chỉnh sửa PD-1 là một điểm kiểm soát miễn dịch nhằm hạn chế sự suy giảm sớm của những tế bào này tỏng cơ thể. Vispa-cel được sử dụng trong thử nghiệm lâm sàng giai đoạn 1 có tên ANTLER để điều trị u lympho không Hodgkin tế bào B tái phát hoặc kháng trị. Theo kết quả thử nghiệm, Vispa-cel có độ bền tương tự CAR-T tự thân, khả năng dung nạp tốt và chứng minh được hiệu quả đáng khích lệ: ở nhóm phù hợp HLA một phần (n = 22), tỷ lệ đáp ứng tổng thể (Overall response rate – ORR) đạt 82%, tỷ lệ đáp ứng hoàn toàn (Complete Response – CR) đạt 64%, tỷ lệ sống không bệnh tiến triển (Progression-free survival – PFS) sau 12 tháng đạt 51%; ở nhóm được tối ưu hóa (n = 35), các tỷ lệ này tương ứng là 86%, 63% và 53%. Tính an toàn của liệu pháp cũng được khẳng định, với các tác dụng phụ không nghiêm trọng, và không có trường hợp nào mắc bệnh ghép chống chủ (GvHD). CB-011 là sản phẩm đồng loại kháng BCMA trong điều trị đa u tủy xương, được đánh giá an toàn và hiệu quả thông qua thử nghiệm lâm sàng giai đoạn 1 có tên CaMMouflage (NCT05722418). Trong thử nghiệm này, nhóm nghiên cứu đã quan sát được những phản ứng sâu sắc và lâu dài ở nhóm bệnh nhân được điều trị. Tỷ lệ đáp ứng tổng thể đạt 92%, với 75% đáp ứng hoàn toàn và 83% đáp ứng ít nhất một phần hoặc giảm ung thư. Hầu hết các bệnh nhân (91%) đều âm tính với bệnh tồn dư tối thiểu (số lượng rất nhỏ các tế bào ung thư còn lại trong cơ thể sau khi điều trị), ngoài ra ít gặp các tác dụng phụ khác. Những kết quả này đánh dấu một bước tiến đáng khích lệ trong liệu pháp tế bào miễn dịch chống ung thư. Các đặc tính sinh học của Vispa-cell và CB-011 tương đương với CAR-T tự thân, đồng thời tính sẵn có và khả năng dung nạp tốt khiến nó phù hợp để sử dụng ngoại trú tại các trung tâm y tế lớn và các bệnh viện cộng đồng, mở rộng đáng kể khả năng tiếp cận với bệnh nhân. Những yếu tố chính liên quan đến kết quả thành công của bệnh nhân bao gồm tuổi của người hiến tặng (người hiến tặng trẻ có kết quả tốt hơn so với người lớn tuổi) và sự phù hợp HLA một phần (sự phù hợp của hai hay nhiều alen tương quan với kết quả tương đương đương với CAR-T tự thân). Công ty Caribou Biosciences tin rằng những sản phẩm này sẽ trở thành liệu pháp tế bào CAR-T đồng loại tiềm năng tốt nhất cho bệnh nhân, đồng thời sẽ tiến hành các thử nghiệm lâm sàng giai đoạn sau để đánh giá kỹ hơn về hiệu quả của chúng. TÀI LIỆU THAM KHẢO 1. Thông cáo báo chí ngày 02 tháng 11 năm 2025 của Caribou Biosciences, Inc. https://www.globenewswire.com/news-release/2025/11/02/3178810/0/en/Caribou-Biosciences-to-Host-Webcast-to-Report-New-Data-Updates-from-Two-Allogeneic-CAR-T-Cell-Therapy-Programs-in-Lymphoma-and-Multiple-Myeloma.html 2. Thông tin dữ liệu nghiên cứu của thử nghiệm ANTLER trên Mạng lưới Tin tức Đầu tư https://investingnews.com/caribou-biosciences-announces-positive-data-from-antler-phase-1-trial-demonstrating-efficacy-and-durability-of-vispa-cel-an-allogeneic-car-t-cell-therapy-on-par-with-autologous-car-t-cell-therapies/ 3. Thông tin về thử nghiệm lâm sàng NCT05722418 trên trang cơ sở dữ liệu các nghiên cứu lâm sàng của Thư Viện Y khoa Quốc gia Hoa Kỳ https://clinicaltrials.gov/study/NCT05722418 XEM THÊM - Cải biến di truyền giúp tăng cường hiệu quả liệu pháp tế bào miễn dịch trong điều trị ung thư: TCR-T và CAR-T https://www.facebook.com/share/p/18mRyiUvJb/ - Liệu pháp CAR-T – bước đột phá của liệu pháp tế bào trong điều trị ung thư https://www.facebook.com/share/p/1ACHF2K2wY/ - CAR-E: Giải pháp tăng cường hiệu quả và tạo trí nhớ miễn dịch cho liệu pháp CAR-T, giúp ngăn ngừa khả năng tái phát ung thư sau điều trị bằng phương pháp này https://www.facebook.com/share/p/1BJvL3gP4L/ - CAR-T in vivo: chiến lược mới với tế bào CAR-T được sản xuất ngay trong cơ thể bệnh nhân https://www.facebook.com/share/p/19Yrq5KFJ2/
23/01/2026







