UNG THƯ VÀ HUYẾT HỌC

Chỉnh sửa vùng khởi động của gen HBG1 và HBG2 trên tế bào gốc tạo máu để điều trị bệnh thiếu máu hồng cầu hình liềm
Thử nghiệm lâm sàng RUBY (https://clinicaltrials.gov/study/NCT04853576) cho thấy phương pháp điều trị đầy hứa hẹn bằng cách chỉnh sửa gen trên tế bào gốc tạo máu đối với bệnh hồng cầu hình liềm, một rối loạn di truyền có rất ít lựa chọn chữa khỏi.
06/04/2026
Liệu pháp CAR-NKT mang lại hiệu quả vượt trội khi điều trị ung thư nội mạc tử cung trong nghiên cứu tiền lâm sàng
Trong một nghiên cứu mới công bố, các nhà khoa học cho thấy liệu pháp tế bào CAR-NKT hiệu quả hơn các liệu pháp miễn dịch hiện tại như CAR-T, CAR-NK trong điều trị ung thư nội mạc tử cung.
26/03/2026
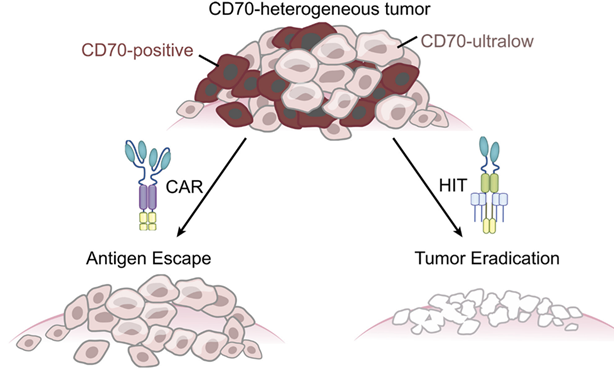
Liệu pháp CAR-T có độ nhạy cao với CD70 mang lại triển vọng loại bỏ hoàn toàn tế bào ung thư trong khối u đặc
Liệu pháp CAR-T đã chứng minh hiệu quả trong điều trị nhiều bệnh huyết học ác tính, nhưng lại gặp rất nhiều hạn chế với các khối u đặc. Một nghiên cứu một công bố trên tạp chí Science cho thấy liệu pháp CAR-T có độ nhạy cao hướng đích CD70 có thể loại bỏ hoàn toàn tế bào ung thư thận, tuyến tụy và buồng trứng ở chuột.
23/03/2026
Liệu pháp tế bào miễn dịch mang cấu trúc CAR: so sánh CAR-T, CAR-NK và CAR-M
Cấu trúc CAR có thể được thiết kế cho nhiều loại tế bào miễn dịch khác nhau, như tế bào T (CAR-T), tế bào giết tự nhiên (CAR-NK), đại thực bào (CAR-M) - mỗi loại đều có những ưu điểm để mang lại tiềm năng điều trị, và có những rào cản cần vượt qua để ứng dụng lâm sàng.
16/03/2026
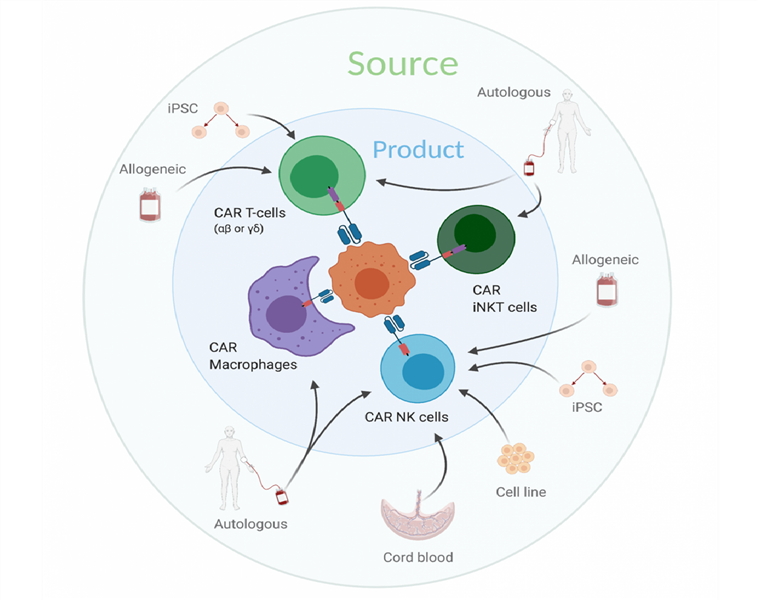
Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh (P4)
Phần 4: Liệu pháp CAR cho các loại tế bào miễn dịch bẩm sinh và những chiến lược kết hợp khi sử dụng lâm sàng
05/03/2026
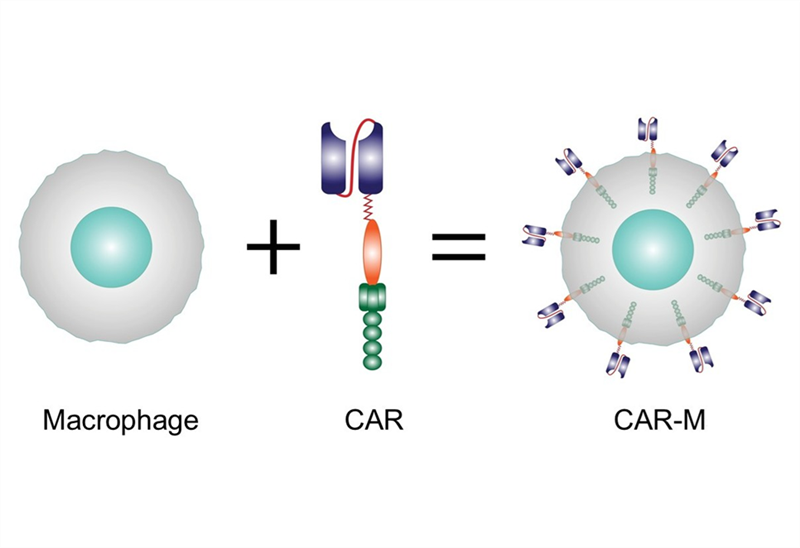
Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh (P3)
Phần 3. Liệu pháp CAR-M – giải pháp đến từ các đại thực bào
26/02/2026
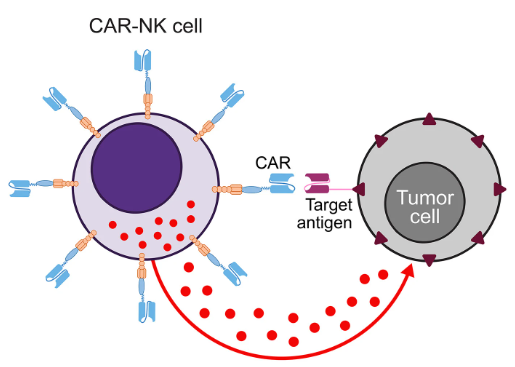
Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh (P2)
Phần 2. Liệu pháp CAR-NK – hiện trạng, thách thức và triển vọng tương lai
15/02/2026
Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh (P1)
Phần 1 - Các tế bào miễn dịch bẩm sinh và lợi thế trong điều trị ung thư u đặc
12/02/2026
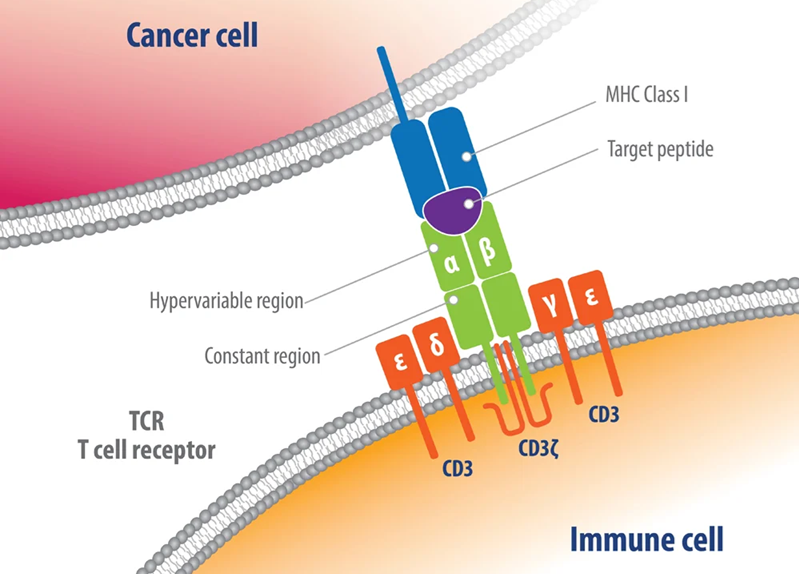
Liệu pháp tế bào T tự thân nhắm đích nhiều kháng nguyên cho thấy triển vọng trong điều trị ung thư tuyến tụy
Một bài báo gần đây trên tạp chí Nature Medicine về thử nghiệm lâm sàng giai đoạn I/II có tên TACTOPS, nghiên cứu về tính an toàn và hiệu quả lâm sàng của liệu pháp tế bào T tự thân nhắm vào nhiều kháng nguyên liên quan đến khối u (Tumor-Associated Antigen, TAA) của ung thư tuyến tụy, đã cho thấy kết quả đầy hứa hẹn.
25/01/2026
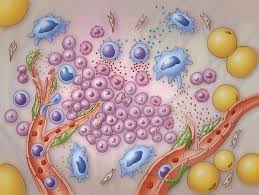
Vai trò của tương tác giữa đại thực bào liên quan đến khối u và nguyên bào sợi liên quan đến ung thư trong môi trường vi mô của sarcoma mô mềm
Sarcoma là một loại ung thư hiếm gặp phát triển từ các mô liên kết của cơ thể như xương, cơ, mỡ, dây thần kinh, mạch máu,… Sarcoma mô mềm (soft tissue sarcoma – STS) phát triển ở cơ, mỡ, gân, dây chằng, mô xơ, mạch máu, chiếm khoảng 80% các trường hợp sarcoma, là loại ung thư nguy hiểm, với tỷ lệ sống thêm 5 năm chỉ khoảng 15% nếu đã di căn và khoảng 81% nếu chưa lan rộng. Trong STS, vi môi trường khối u (tumor microenvironment – TME) không chỉ hoạt động như một chất nền tăng trưởng cho tế bào ung thư mà còn là một yếu tố quan trọng ảnh hưởng đến hành vi của khối u và đáp ứng điều trị. TME chứa hai thành phần tế bào trung tâm là đại thực bào liên quan đến khối u (tumor-associated macrophage – TAM) và nguyên bào sợi liên quan đến ung thư (cancer-associated fibroblast – CAF), sự tương tác giữa các tế bào và các phân tử tín hiệu giúp điều chỉnh sự tăng sinh, xâm lấn và di căn của khối u. CAF giải phóng nhiều phân tử tín hiệu như IL-6, TGF-β, PDGF, HIF-1α và SPP1, kích hoạt và thu hút TAM, đồng thời thúc đẩy sự phân cực của chúng về phía kiểu hình M2, được biết đến với hoạt động tiền ung thư. Các cytokine này kích thích sự hình thành mạch máu bất thường, tái cấu trúc chất nền ngoại bào (extracellular matrix – ECM) và cơ chế thoát miễn dịch. Đồng thời, TAM tiết ra IL-34, CSF1R, VEGF và MMP, giúp tăng cường hoạt hóa CAF và thúc đẩy sự tăng sinh và di cư của tế bào khối u. Tương tác hai chiều này tạo ra một vòng lặp: TAM kích hoạt CAF thông qua các yếu tố như SPP1, MMP2/9 và EGF, tăng cường khả năng tái cấu trúc ECM và hỗ trợ khối u xâm lấn của CAF. Ngược lại, CAF tiết ra các chất hoạt hóa PDGF và IL-6/STAT3, thúc đẩy sự tuyển dụng, sự sống sót và sự phân cực của TAM. Hơn nữa, trục này ức chế các phản ứng miễn dịch chống khối u: CAF sản xuất axit lactic và TGF-β, ức chế sự tăng sinh tế bào T, trong khi TAM biểu hiện PD-L1, ngăn chặn hoạt động của tế bào T thông qua con đường PD-1/PD-L1. Nhìn chung, mạng lưới kết hợp TAM-CAF tổ chức lại vi môi trường khối u theo hướng ủng hộ xơ hóa, ức chế miễn dịch và ủng hộ sinh mạch, tăng cường sự tăng sinh, di cư và trốn tránh miễn dịch của tế bào khối u trong các khối u mô mềm. TÀI LIỆU THAM KHẢO Zhou J., et al. (2025). The prognostic role of tumor-associated macrophage and cancer-associated fibroblast interactions in soft tissue sarcoma microenvironments. iScience 28(11): 113851. DOI: https://doi.org/10.1016/j.isci.2025.113851
24/01/2026
Ghép tế bào gốc tạo máu đồng loại: người hiến trẻ tuổi mặc dù không cùng huyết thống nên được ưu tiên hơn người hiến cùng huyết thống nhưng lớn tuổi
Các nhà nghiên cứu đã chứng minh rằng tuổi người hiến đóng vai trò quan trọng trong sự thành công của ghép tế bào gốc tạo máu đồng loại.
24/01/2026
Liệu pháp tế bào gốc chỉnh sửa gen cho bệnh lý huyết sắc tố
Chỉnh sửa tế bào gốc tạo máu sau đó ghép cho bệnh nhân được xác nhận là phương pháp điều trị hiệu quả cho bệnh lý huyết sắc tố.
24/01/2026






