UNG THƯ VÀ HUYẾT HỌC

FDA bổ sung cảnh báo tác dụng phụ viêm ruột liên quan đến sản phẩm CAR-T Carvykti
Carvykti (ciltacabtagene autoleucel) là một loại liệu pháp tế bào CAR-T được phát triển bởi hãng Janssen Biotech, sử dụng trong điều trị bệnh đa u tủy xương. Đây là những tế bào lympho T của chính bệnh nhân được cải biến di truyền để mang thụ thể nhân tạo đặc hiệu với kháng nguyên trưởng thành tế bào B (B-cell maturation antigen –– BCMA) có mặt trên bề mặt tế bào đa u tủy xương, nhờ đó có thể phát hiện dễ dàng hơn và tiêu diệt những tế bào ác tính này. Carvykti là một trong hai sản phẩm CAR-T hướng đích BCMA, và là một trong bảy sản phẩm CAR-T nói chung đã được Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (US Food and Drug Administration – US FDA) phê duyệt. Ngày 10 tháng 10 năm 2025, FDA đã phê duyệt nhãn thuốc Carvykti được cập nhật bao gồm cảnh báo đặc biệt (cảnh báo được đóng khung – Boxed Warning) về bệnh viêm ruột liên quan đến tế bào hiệu lực miễn dịch (immune effector cell-associated enterocolitis –– IEC-EC). Việc thay đổi nhãn được thực hiện sau những báo cáo từ thử nghiệm lâm sàng và tác dụng phụ ghi nhận được khi sản phẩm lưu hành trên thị trường. IEC-EC là tình trạng viêm ruột nghiêm trọng có thể xảy ra sau một số liệu pháp miễn dịch, bao gồm liệu pháp tế bào CAR-T. Bệnh nhân mắc IEC-EC sau khi điều trị bằng Carvykti có biểu hiện tiêu chảy kéo dài hoặc nghiêm trọng , đau bụng và sụt cân, một số trường hợp mất khả năng tiêu hóa mà cần truyền dinh dưỡng qua đường tĩnh mạch. Trong những trường hợp nghiêm trọng, tác dụng phụ này có liên quan đến tử vong do thủng ruột và nhiễm trùng huyết. Việc quản lý IEC-EC thường bao gồm chăm sóc hỗ trợ, dinh dưỡng qua đường tiêm truyền nếu cần và liệu pháp ức chế miễn dịch, chẳng hạn như corticosteroid. FDA cho biết IEC-EC đã được ghi nhận sau vài tuần đến vài tháng kể từ khi truyền. Đối với những bệnh nhân mắc tình trạng này mà không đáp ứng điều trị, cần cân nhắc thực hiện thêm các xét nghiệm để loại trừ u lympho tế bào T đường tiêu hóa, căn bệnh đã được báo cáo trong quá trình đưa thuốc ra thị trường. Ngoài cảnh báo đặc biệt trên, những thay đổi về nhãn còn mở rộng sang các cảnh báo, biện pháp phòng ngừa và phản ứng có hại – phần kinh nghiệm sau khi đưa thuốc ra thị trường trong thông tin kê đơn và hướng dẫn dùng thuốc. Mặc dù vậy, FDA nhấn mạnh rằng lợi ích tổng thể của Carvykti vẫn lớn hơn những rủi ro tiềm ẩn đối với mục đích sử dụng đã được phê duyệt, bao gồm cả lợi ích sống sót tổng thể ở những bệnh nhân được điều trị bằng Carvykti. Dữ liệu sống sót tổng thể từ thử nghiệm CARTITUDE-4 đã được cập nhật vào thông tin kê đơn, với kết quả Carvykti mang lại lợi ích đáng kể về mặt thống kê so với điều trị tiêu chuẩn ở bệnh nhân đa u tủy tái phát và kháng lenalidomide (với thời gian theo dõi trung bình khoảng 33,6 tháng). TÀI LIỆU THAM KHẢO - “FDA bổ sung cảnh báo đặc biệt về viêm ruột liên quan đến tế bào miễn dịch vào thuốc CAR-T”, bản tin Medscape ngày 13/10/2025 https://www.medscape.com/viewarticle/fda-adds-boxed-warning-immune-effector-cell-associated-2025a1000rkg - “FDA chấp thuận thay đổi nhãn bao gồm cảnh báo đặc biệt về bệnh viêm ruột liên quan đến tế bào miễn dịch sau khi điều trị bằng Ciltacabtagene Autoleucel (CARVYKTI, Janssen Biotech, Inc.)”, thông báo của FDA ngày 10/10/2025 https://www.fda.gov/safety/medical-product-safety-information/fda-approves-labeling-changes-include-boxed-warning-immune-effector-cell-associated-enterocolitis XEM THÊM - Cải biến di truyền giúp tăng cường hiệu quả liệu pháp tế bào miễn dịch trong điều trị ung thư: TCR-T và CAR-T https://www.facebook.com/share/p/18mRyiUvJb/ - Liệu pháp CAR-T – bước đột phá của liệu pháp tế bào trong điều trị ung thư https://www.facebook.com/share/p/1ACHF2K2wY/ - FDA loại bỏ các chiến lược đánh giá và giảm thiểu rủi ro cho liệu pháp CAR-T tự thân trong điều trị ung thư https://www.facebook.com/share/p/19ZgegsBHs/
23/01/2026
Phương pháp cải tiến giúp nâng cao hiệu quả của liệu pháp tế bào CAR-T trong điều trị ung thư u đặc
1. Liệu pháp tế bào CAR-T: thành tựu lớn trong điều trị các bệnh lý huyết học ác tính Các tế bào T có khả năng nhận diện các tác nhân vi khuẩn, virus, tế bào ung thư,… nhờ các thụ thể có trên bề mặt của chúng. Để phát hiện dễ dàng và đặc hiệu hơn đối với các tế bào ung thư, các nhà khoa học đã thiết kế thụ thể kháng nguyên khảm (Chimeric Antigen Receptor, CAR) có khả năng liên kết với kháng nguyên nhất định trên tế bào ung thư. Những tế bào T mang cấu trúc CAR (tế bào CAR-T) khi được truyền vào cơ thể bệnh nhân sẽ đi tìm và tiêu diệt tế bào ác tính, đồng thời có khả năng nhân lên trong cơ thể để duy trì hoạt động lâu dài. Liệu pháp CAR-T đã khẳng định được hiệu quả trong điều trị các bệnh lý huyết học ác tính. Hiện đã có 7 sản phẩm được cấp phép tại Hoa Kỳ và châu Âu, gồm 5 sản phẩm được thiết kế CAR đặc hiệu CD19 trong điều trị bệnh bạch cầu và u lympho (KYMRIAH – Tisagenlecleucel, YESCARTA – Axicabtagene ciloleucel, TECARTUS – Brexucabtagene autoleucel, BREYANZI – Lisocabtagene maraleucel, AUCATZYL – Obecabtagene autoleucel) và 2 sản phẩm hướng đích kháng nguyên trưởng thành tế bào B (BCMA) trong điều trị đa u tủy xương (ABECMA – Idecabtagene vicleucel, CARVYKTI – Ciltacabtagene autoleucel). Tại nhiều quốc gia khác như Nhật Bản, Trung Quốc, Ấn Độ,… một số sản phẩm khác cũng đã được phê duyệt trong điều trị các bệnh lý huyết học ác tính. Bên cạnh đó, hàng trăm thử nghiệm lâm sàng ở khắp nơi trên thế giới hứa hẹn sẽ có thêm những liệu pháp CAR-T khác được cấp phép ở nhiều quốc gia trong thời gian tới. (A) PD-L1 trên tế bào ung thư kết hợp với PD-1 trên tế bào T là một điểm kiểm soát miễn dịch, khiến tế bào T không nhận diện được tế bào ung thư; các thuốc ức chế PD-1 và PD-L1 ngăn chặn sự liên kết giữa hai phân tử này, giúp tế bào T nhận diện và tiêu diệt tế bào ung thư. (B) Chiến lược biến đổi tế bào CAR-T để có khả năng tiết ra protein dung hợp IL-12 và chất ức chế PD-L1, protein này vừa có khả năng chặn PD-L1 khiến tế bào ung thư không trốn tránh được tế bào miễn dịch, vừa có khả năng kích thích phản ứng miễn dịch tại chỗ giống như hoạt tính của IL-12. 2. Liệu pháp tế bào CAR-T cải tiến nâng cao hiệu quả điều trị ung thư u đặc Trái với những tiến bộ của CAR-T trong điều trị các bệnh lý huyết học ác tính, việc nghiên cứu và thử nghiệm liệu pháp này trên các dạng u đặc gặp rất nhiều hạn chế, trong khi nhóm này chiếm trên 90% các trường hợp ung thư. Nguyên nhân có thể do tính không đồng nhất của kháng nguyên, vi môi trường khối u ức chế miễn dịch nên ức chế hoặc bất hoạt CAR-T, rào cản vật lý và mô đệm ngăn chặn tế bào CAR-T xâm nhập,… Tuy vậy, trong những năm gần đây, các nhà nghiên cứu ung thư đã phát triển nhiều phương pháp để khắc phục tình trạng này. Trong một nghiên cứu mới công bố, các nhà khoa học Hoa Kỳ đã đưa ra một chiến lược mới để tăng cường hiệu quả của CAR-T trong điều trị u rắn. Họ đã biến đổi tế bào CAR-T để tiết ra protein dung hợp, kết hợp giữa interleukin 12 (IL-12) và chất ức chế protein PD-L1, nhờ đó những tế bào này tấn công miễn dịch mạnh mẽ, vượt qua môi trường khối u để phát huy hiệu quả. IL-12 là một cytokine có khả năng hoạt hóa miễn dịch, trong khi chất ức chế PD-L1 làm bất hoạt PD-L1 (là một điểm kiểm soát miễn dịch giúp tế bào ung thư tránh được sự tấn công của tế bào miễn dịch), khiến tế bào ung thư dễ dàng bị phát hiện và tiêu diệt. Việc dung hợp 2 protein này với nhau giúp tế bào CAR-T nhận diện tế bào ác tính tốt hơn, được hoạt hóa bởi IL-12 ngay tại vị trí khối u khi có mặt PD-L1, đồng thời hạn chế độc tính toàn thân của IL-12 đối với bệnh nhân. Những tế bào CAR-T này đã thể hiện hoạt động hiệu quả khi nuôi cấy với tế bào ung thư ở người trong phòng thí nghiệm. Khi thử nghiệm trên mô hình chuột ung thư tuyến tiền liệt và ung thư buồng trứng, chúng đã có thể thâm nhâp sâu vào khối u, tác động làm giảm đáng kể kích thước khối u mà không phát hiện độc tính ở cơ quan khác, tình trạng viêm toàn thân giảm đáng kể, cho thấy hiệu quả và tính an toàn của phương pháp này. Từ những kết quả trên, nhóm nghiên cứu đang đặt mục tiêu thử nghiệm lâm sàng trong vòng 1-2 năm tới, ban đầu tập trung vào ung thư tuyến tiền liệt và ung thư buồng trứng, đồng thời có thể mở rộng sang ung thư tuyến tụy, đại trực tràng và u não. Nhóm nghiên cứu cũng cho rằng chiến lược trên có thể hữu ích không chỉ với CAR-T, mà còn áp dụng được với các liệu pháp tế bào miễn dịch khác, như TIL và TCR-T. TÀI LIỆU THAM KHẢO Murad J. P., et al. (2025). Solid tumor CAR T cells engineered with fusion proteins targeting PDL1 for localized IL-12 delivery. Nature Biomedical Engineering. DOI: https://doi.org/10.1038/s41551-025-01509-2 XEM THÊM - Liệu pháp miễn dịch trong điều trị ung thư https://ysinhtebao.com/ung-thu-va-huyet-hoc/lieu-phap-mien-dich-trong-dieu-tri-ung-thu - Cải biến di truyền giúp tăng cường hiệu quả liệu pháp tế bào miễn dịch trong điều trị ung thư: TCR-T và CAR-T https://ysinhtebao.com/lieu-phap-cart-tcrt/cai-bien-di-truyen-giup-tang-cuong-hieu-qua-lieu-phap-te-bao-mien-dich-trong-dieu-tri-ung-thu-tcr-t-va-car-t - Liệu pháp CAR-T – bước đột phá của liệu pháp tế bào trong điều trị ung thư https://ysinhtebao.com/lieu-phap-te-bao-mien-dich/lieu-phap-car-t-buoc-dot-pha-cua-lieu-phap-te-bao-trong-dieu-tri-ung-thu - CAR-E: Giải pháp tăng cường hiệu quả và tạo trí nhớ miễn dịch cho liệu pháp CAR-T, giúp ngăn ngừa khả năng tái phát ung thư sau điều trị bằng phương pháp này https://ysinhtebao.com/lieu-phap-tb-mien-dich-khac/car-e-giai-phap-tang-cuong-hieu-qua-va-tao-tri-nho-mien-dich-cho-lieu-phap-car-t-giup-ngan-ngua-kha-nang-tai-phat-ung-thu - Liệu pháp tế bào cho các bệnh ung thư dạng u đặc đã đạt nhiều thành tựu đột phá trong năm 2024 https://ysinhtebao.com/ung-thu-va-huyet-hoc/lieu-phap-te-bao-cho-cac-benh-ung-thu-dang-u-dac-da-dat-nhieu-thanh-tuu-dot-pha-trong-nam-2024
23/01/2026
Liệu pháp CAR-T và sự liên quan đến ung thư thứ phát – kết quả phân tích trên 783 bệnh nhân
1. CAR-T – bước đột phá của liệu pháp tế bào trong điều trị ung thư Các tế bào T mang thụ thể kháng nguyên khảm (Chimeric Antigen Receptor T Cell – CAR-T) mang đến một giải pháp đầy hứa hẹn để điều trị một số bệnh ung thư máu, và các thử nghiệm lâm sàng hiện tại chủ yếu tập trung CAR-T đến các bệnh lý huyết học ác tính. Tính đến hết tháng 6 năm 2025, đã có 7 sản phẩm CAR-T được FDA Hoa Kỳ phê duyệt, bao gồm 5 sản phẩm trong điều trị u lympho và bệnh bạch cầu, 2 sản phẩm trong điều trị đa u tủy xương. Ngược lại với những tiến bộ của CAR-T trong điều trị các bệnh lý huyết học ác tính, việc nghiên cứu và thử nghiệm liệu pháp này trên u đặc gặp rất nhiều hạn chế. Nguyên nhân có thể do tính không đồng nhất của kháng nguyên, vi môi trường khối u đặc ức chế miễn dịch nên ức chế hoặc bất hoạt CAR-T, rào cản vật lý và mô đệm ngăn cản tế bào CAR-T xâm nhập,… Tuy nhiên hiện nay, nhiều thử nghiệm đã có những chiến lược khắc phục hiện tượng trên, và cho thấy những tín hiệu tích cực về liệu pháp này trong điều trị u thần kinh đệm, sarcoma, ung thư biểu mô tế bào thận,… 2. Quy trình thực hiện liệu pháp CAR-T và những nghi ngại về khả năng gây ung thư thứ phát Quy trình thực hiện liệu pháp tế bào CAR-T thường bao gồm các bước chính: (1) thu thập tế bào T từ máu của chính bệnh nhân, (2) chuyển gen mã hóa thụ thể kháng nguyên khảm (CAR) để tế bào T có thể sản xuất cấu trúc CAR trên bề mặt của nó, cấu trúc này cho phép tế bào T nhận diện các protein đặc hiệu trên tế bào ung thư, (3) nuôi cấy tăng sinh tế bào CAR-T để nhân lên đủ số lượng cần thiết, (4) điều trị điều kiện hóa bệnh nhân bằng hóa/xạ trị để giảm số lượng tế bào T hiện có, tạo chỗ trống và chuẩn bị cho hệ miễn dịch tiếp nhận tế bào CAR-T, (5) truyền sản phẩm CAR-T cho bệnh nhân, các tế bào này đi khắp cơ thể và tìm những tế bào ác tính biểu hiện kháng nguyên mà CAR nhận diện để tiêu diệt chúng, (6) theo dõi bệnh nhân sau điều trị để đánh giá, kiểm soát tính an toàn và hiệu quả của liệu pháp. Trong quy trình trên, giai đoạn thiết kế gen mã hóa CAR và chuyển gen này vào tế bào T đóng vai trò chìa khóa. Các nhà khoa học cần xác định dấu hiệu (kháng nguyên) đặc hiệu trên tế bào ung thư (ví dụ CD19 đối với bệnh bạch cầu/u lympho, hay BCMA đối với tế bào đa u tủy xương), sau đó thiết kế cấu trúc CAR nhận diện được kháng nguyên này. Đoạn ADN mã hóa cấu trúc đó được đưa vào tế bào T của bệnh nhân, thường bằng vector virus, là công cụ chuyển gen dựa trên cơ chế xâm nhập vào tế bào của một số loại virus. Vì các vector virus chèn ADN ngẫu nhiên chứ không nhắm trúng đích vào một vùng xác định của bộ gen, nên về lý thuyết sẽ có nguy cơ việc chèn ngẫu nhiên đó có thể phá vỡ các gen kiềm chế khối u chính, dẫn đến bệnh nhân mắc loại ung thư khác sau khi sử dụng liệu pháp CAR-T. Những nghi vấn này càng trở nên đáng lo ngại khi đầu năm 2024, Verdun và cộng sự công bố: tính đến 31/12/2023, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (US-FDA) đã ghi nhận 22 trường hợp phát hiện các tế bào T ác tính ở những bệnh nhân trước đây được điều trị bằng tế bào T biến đổi gen, dường như đây là tác dụng phụ hiếm gặp do chính liệu pháp CAR-T gây nên. FDA khi phê duyệt các liệu pháp CAR-T đều áp dụng các chiến lược đánh giá và giảm thiểu rủi ro (Risk Evaluation and Mitigation Strategies – REMS), mặc dù chính sách này mới được gỡ bỏ cuối tháng 06/2025, nhưng FDA tiếp tục yêu cầu các nhà sản xuất tiến hành các nghiên cứu quan sát đánh giá độ an toàn trong quá trình sử dụng (bao gồm cả nguy cơ mắc ung thư thứ phát) với việc theo dõi bệnh nhân trong 15 năm sau khi điều trị. 3. Nghiên cứu hồi cứu chứng minh CAR-T không liên quan đến ung thư thứ phát Để đánh giá những rủi ro này, một nhóm nghiên cứu Hoa Kỳ đã phân tích dữ liệu từ 783 bệnh nhân trong 38 thử nghiệm lâm sàng khác nhau sử dụng liệu pháp tế bào T diễn ra từ nă 2001 đến 2023. Theo kết quả đánh giá với thời gian theo dõi trung bình 1,56 năm, họ chỉ xác định được 1 trường hợp có tế bào T ác tính – một tỷ lệ rất hiếm. Điều quan trọng là khi giải trình tự ADN từ u lympho tế bào T này, chúng không chứa trình tự gen được sử dụng trong liệu pháp CAR-T, cho thấy đó không phải là nguyên nhân gây nên tình trạng ung thư thứ phát đó. Theo nhóm nghiên cứu, nguyên nhân gây nên ung thư thứ phát khả năng cao nhất đến từ các liệu pháp hóa trị gây độc tế bào, gây tổn thương ADN. Những bệnh nhân sau khi trải qua các đợt hóa trị và được sử dụng liệu pháp CAR-T một cách hiệu quả, các tế bào ung thư bị tiêu diệt, tình trạng bệnh được cải thiện, tuy nhiên những tế bào T mang tổn thương ADN trong cơ thể bệnh nhân không được loại bỏ, khiến họ có khả năng bị ung thư tế bào T thứ phát trong những năm tiếp theo. Trong 783 bệnh nhân được hồi cứu, 176 bệnh nhân vẫn còn mẫu máu lưu trữ trong quá trình thử nghiệm lâm sàng. Nhóm nghiên cứu đã giải trình tự ADN từ những mẫu này, kết quả cho thấy trong một số tế bào (đặc biệt là những tế bào tồn tại trong máu vài tháng sau điều trị) có phát hiện vị trí tích hợp nằm trong hoặc gần các gen liên quan đến ung thư, tuy nhiên ngay cả khi đó các tế bào không có dấu hiệu ác tính. Để những tế bào này trở thành tế bào ung thư cần có nhiều sự kiện phức tạp, rất khó để một sự kiện chuyển gen bằng vector virus có thể biến một tế bào T bình thường thành tế bào T ác tính. Kết quả phân tích này đặc biệt quan trọng, giúp đẩy lùi những lo ngại về nguy cơ ung thư thứ phát xảy ra do liệu pháp CAR-T, đặc biệt khi hiện tại các nhà khoa học đang mở rộng thử nghiệm CAR-T trong nhiều bệnh lý khác, bao gồm cả các bệnh ung thư u đặc và các bệnh tự miễn. Đồng thời, những chiến lược chuyển gen an toàn hơn trong quá trình sản xuất CAR-T cũng đang được nghiên cứu rộng rãi trong thời gian gần đây. TÀI LIỆU THAM KHẢO 1. Jadlowsky J. K., et al. (2025). Long-term safety of lentiviral or gammaretroviral gene-modified T cell therapies. Nature Medicine, 31(4), 1134-1144. DOI https://doi.org/10.1038/s41591-024-03478-6 2. Verdun N., and Marks P. (2024). Secondary cancers after chimeric antigen receptor T-cell therapy. New England Journal of Medicine, 390(7), 584-586. DOI https://doi.org/10.1056/NEJMp2400209 3. Xiao K., et al. (2024). mRNA‐based chimeric antigen receptor T cell therapy: Basic principles, recent advances and future directions. Interdisciplinary Medicine, 2(1), e20230036. DOI https://doi.org/10.1002/INMD.20230036 XEM THÊM - Cải biến di truyền giúp tăng cường hiệu quả liệu pháp tế bào miễn dịch trong điều trị ung thư: TCR-T và CAR-T https://www.facebook.com/share/p/18mRyiUvJb/ - Liệu pháp CAR-T – bước đột phá của liệu pháp tế bào trong điều trị ung thư https://www.facebook.com/share/p/1ACHF2K2wY/ - FDA loại bỏ các chiến lược đánh giá và giảm thiểu rủi ro cho liệu pháp CAR-T tự thân trong điều trị ung thư https://www.facebook.com/share/p/171ZGTP5uq/ - CAR-T in vivo: chiến lược mới với tế bào CAR-T được sản xuất ngay trong cơ thể bệnh nhân https://www.facebook.com/share/p/19Yrq5KFJ2/ - CAR-E: Giải pháp tăng cường hiệu quả và tạo trí nhớ miễn dịch cho liệu pháp CAR-T, giúp ngăn ngừa khả năng tái phát ung thư sau điều trị bằng phương pháp này https://www.facebook.com/share/p/1BJvL3gP4L/
23/01/2026
CAR-E: Giải pháp tăng cường hiệu quả và tạo trí nhớ miễn dịch cho liệu pháp CAR-T, giúp ngăn ngừa khả năng tái phát ung thư
Các nhà khoa học đề xuất giải pháp tăng cường để khắc phụ vấn đề tái phát ung thư khi điều trị CAR-T.
23/01/2026
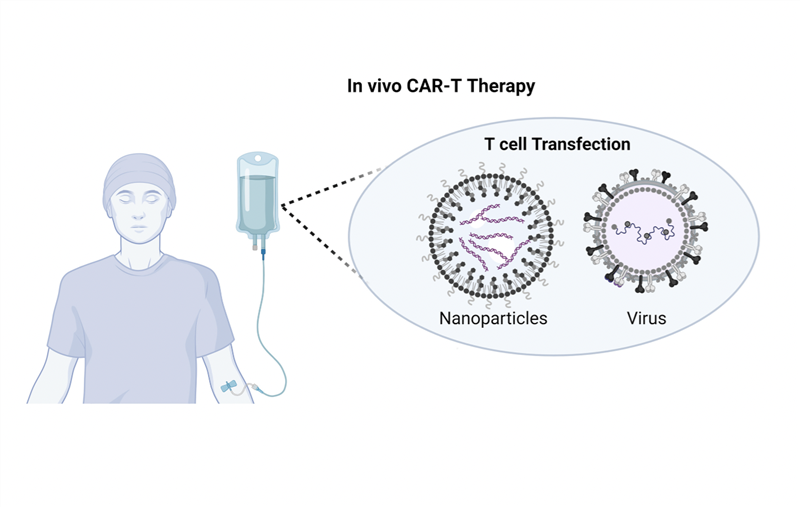
CAR-T in vivo: chiến lược mới với tế bào CAR-T được sản xuất ngay trong cơ thể bệnh nhân
Trong những năm gần đây, liệu pháp tế bào T với thụ thể kháng nguyên khảm (chimeric antigen receptor T-cell –– CAR-T) đã nổi lên như một phương pháp miễn dịch mang tính cách mạng trong điều trị ung thư, với những hiệu quả đáng kể trong điều trị các bệnh huyết học ác tính và đang được thử nghiệm trong các bệnh u đặc (https://ysinhtebao.com/lieu-phap-tb-mien-dich/lieu-phap-car-t-buoc-dot-pha-cua-lieu-phap-te-bao-trong-dieu-tri-ung-thu). Quy trình CAR-T thông thường (ex vivo) được thực hiện qua nhiều bước phức tạp: thu thập tế bào T từ bệnh nhân, biến đổi gen của chúng để biểu hiện thụ thể kháng nguyên khảm (cấu trúc CAR) có khả năng nhận diện tế bào ung thư, nuôi cấy tăng sinh tế bào CAR-T, kiểm tra chất lượng để đảm bảo tính an toàn và hiệu quả, truyền sản phẩm trở lại bệnh nhân để tìm kiếm và tiêu diệt tế bào ung thư. Tổng thời gian thường mất 2–4 tuần và đòi hỏi những yêu cầu đặc biệt về cơ sở vật chất, trang thiết bị, dẫn đến chi phí khá lớn và độ phức tạp cao của quy trình sản xuất, hạn chế khả năng tiếp cận liệu pháp này. Những thách thức này thúc đẩy các nhà khoa học thử nghiệm các chiến lược cải thiện liệu pháp này, trong đó một phương pháp đầy hứa hẹn là liệu pháp CAR-T in vivo, với các tế bào CAR-T được tạo ra trực tiếp trong cơ thể bệnh nhân thay vì thông qua các quy trình sản xuất ex vivo truyền thống. Quá trình này được thực hiện bằng cách đưa vào trong cơ thể các hạt nano hoặc vector virus nhắm trúng đích tế bào T, chúng sẽ chuyển gen và biểu hiện cấu trúc CAR, tạo nên tế bào CAR-T có thể nhân lên tự nhiên trong cơ thể bệnh nhân. Phương pháp này khắc phục được những nhược điểm đã nêu như thời gian kéo dài, độ phức tạp và chi phí cao của CAR-T ex vivo, đồng thời có những ưu thế tiềm năng liên quan đến việc chuẩn bị bệnh nhân, chẳng hạn như nguy cơ nhiễm trùng cơ hội và độc tính toàn thân. Tuy nhiên, liệu pháp CAR-T in vivo cũng đối mặt với nhiều thách thức. Mối quan tâm lớn nhất là sự phát triển độc tính toàn thân do hoạt hóa quá mức CAR-T, gây ra bởi sự tương tác giữa CAR và các phân tử trên bề mặt tế bào ung thư (phân tử đồng kích thích được chọn cho thiết kế CAR). Việc sử dụng các vector virus (tiêu chuẩn vàng trong sản xuất CAR-T hiện tại) mang đến những lo ngại về việc chèn gen mất kiểm soát, hoặc phản ứng miễn dịch bẩm sinh chống lại các virus đó. Những khó khăn này đã và đang được các nhà khoa học đề ra những chiến lược khắc phục hiệu quả, để mang lại liệu pháp an toàn cho bệnh nhân. Như vậy, việc sản xuất CAR-T in vivo là một giải pháp thay thế sáng tạo và đầy tiềm năng cho sản xuất ex vivo, giúp nhiều bệnh nhân ung thư và các bệnh lý khác có cơ hội tiếp cận với liệu pháp điều trị tiên tiến này. Những kết quả thử nghiệm tiền lâm sàng và một số thử nghiệm lâm sàng gần đây đã thu được những kết quả tích cực để đưa CAR-T in vivo đến gần hơn tới ứng dụng rộng rãi. Đồng thời, chiến lược này cũng giúp thúc đẩy những ứng dụng tương tự đối với các loại tế bào miễn dịch khác, như tế bào giết tự nhiên (CAR-NK, với nguy cơ mắc bệnh ghép chống chủ (GvHD) và độc tính toàn thân thấp hơn), hay đại thực bào (CAR-M, có khả năng xâm nhập vào khối u rắn, chịu được môi trường vi mô ức chế miễn dịch của khối u). TÀI LIỆU THAM KHẢO 1. Bui Thuy Anh, et al. (2024). Advancements and challenges in developing in vivo CAR T cell therapies for cancer treatment. EBioMedicine, 106. https://doi.org/10.1016/j.ebiom.2024.105266 2. Pinto E., et al. (2025). From ex vivo to in vivo chimeric antigen T cells manufacturing: new horizons for CAR T-cell based therapy. Journal of translational medicine, 23(1), 10. https://doi.org/10.1186/s12967-024-06052-3 3. Song Z., et al. (2025). In vivo production of CAR T cell: Opportunities and challenges. Genes & Diseases, 101612. https://doi.org/10.1016/j.gendis.2025.101612
23/01/2026
Liệu pháp tế bào CAR-T điều trị ung thư gây ra “sương mù não” ở bệnh nhân và hướng khắc phục
Thụ thể kháng nguyên khảm (Chimeric Antigen Receptor – CAR) là các protein thụ thể được thiết kế giúp cho tế bào miễn dịch nhận diện tế bào ác tính và kích hoạt phản ứng tiêu diệt chúng. Liệu pháp sử dụng tế bào T mang cấu trúc CAR (CAR-T) mang đến một phương pháp đầy hứa hẹn để điều trị ung thư, trong đó có 7 sản phẩm đã được FDA Hoa Kỳ phê duyệt cho các tình trạng huyết học ác tính, cùng với hàng nghìn thử nghiệm lâm sàng trên nhiều bệnh lý khác nhau. Tuy nhiên, sau khi điều trị bằng CAR-T, một số bệnh nhân phản ánh với bác sỹ điều trị rằng họ cảm thấy khó tập trung và hay quên, được gọi là hiện tượng “sương mù não”. Suy giảm nhận thức sau liệu pháp CAR-T thường nhẹ, bệnh nhân không phát triển chứng mất trí nhở, nhưng gây tình trạng rất khó chịu và không tự khỏi, ảnh hưởng đến chất lượng cuộc sống. Ngoài ra, tình trạng này rất được quan tâm ở trẻ em vì não bộ của trẻ em vẫn đang phát triển. Trong một nghiên cứu được thực hiện trên chuột, các nhà khoa học Hoa Kỳ đã cho thấy liệu pháp CAR-T gây ra suy giảm nhận thức nhẹ, độc lập với các phương pháp điều trị ung thư khác, đồng thời xác định được các loại thuốc cải thiện tình trạng này. Họ đã đánh giá trên những con chuột bị khối u ở não, máu, da và xương, được điều trị bằng tế bào CAR-T, trước và sau điều trị đều trải qua các bài kiểm tra nhận thức tiêu chuẩn, đo lường phản ứng với vật thể mới và cách di chuyển trong một mê cung đơn giản. Nhóm nghiên cứu nhận thấy CAR-T gây suy giảm nhận thức nhẹ ở chuột với các vị trí khối u khác nhau (khối u bắt nguồn từ não, di căn đến não hoặc nằm ngoài não), những trường hợp duy nhất không bị hiện tượng này là chuột ung thư xương. Các tế bào miễn dịch ở não có tên gọi microglia đóng vai trò then chốt trong vấn đề này. Microglia bị kích hoạt bởi phản ứng miễn dịch của tế bào CAR-T, sản sinh ra các phân tử miễn dịch gây viêm (cytokine và chemokine) tác động lên toàn não bộ, đặc biệt có hại cho các tế bào thần kinh đệm oligodendrocyte, có vai trò tạo ra myelin để cách ly các sợi thần kinh và giúp các dây thần kinh truyền tín hiệu tốt hơn. Sự suy giảm khả năng cách ly của các dây thần kinh dẫn đến sự suy giảm nhận thức. Kiểm chứng trên mẫu mô não từ những người tham gia thử nghiệm lâm sàng về CAR-T đối với u tủy sống và thân não, các nhà khoa học xác nhận rằng các tế bào microglia và oligodendrocyte dường như bị rối loạn điều hòa tương tự như ở những con chuột nêu trên. Nhằm giải quyết tình trạng “sương mù não”, nhóm nghiên cứu cho chuột sử dụng hợp chất làm suy giảm tế bào microglia trong 2 tuần, kết quả là những tế bào này trở lại trạng thái không bị kích hoạt, chuột không còn bị suy giảm nhận thức. Kết quả tương tự cũng thu được khi cho chuột sử dụng các thuốc ức chế phân tử cụ thể để can thiệp vào những tín hiệu từ các chemikine gây hại đến não. Những kết quả này đã chứng minh được nguyên nhân nền tảng của hội chứng “sương mù não” xảy ra ở các bệnh nhân ung thư được điều trị bằng liệu pháp CAR-T. Không chỉ vậy, nghiên cứu này đã đưa ra được hai chiến lược khắc phục tình trạng đó, mai gồm làm suy giảm tạm thời tế bào miễn dịch microglia trong não, hoặc ngắt tín hiệu chemokine. Điều này rất có ý nghĩa trong việc cải thiện chất lượng cuộc sống cho bệnh nhân sử dụng CAR-T, đưa đến giải pháp điều trị ung thư an toàn hơn. TÀI LIỆU THAM KHẢO Geraghty A. C., et al. (2025). Immunotherapy-related cognitive impairment after CAR T cell therapy in mice. Cell, 188(12), 3238-3258. DOI: https://doi.org/10.1016/j.cell.2025.03.041.
23/01/2026
Biểu hiện TCR trên tế bào CAR-T giúp cải thiện tính an toàn và hiệu quả trong điều trị ung thư
Liệu pháp tế bào T đã mang lại những cải thiện đáng kể về khả năng điều trị ung thư, đặc biệt với sự phát triển của công nghệ chỉnh sửa gen giúp cải biến đặc tính vốn có của tế bào miễn dịch. Đối với liệu pháp CAR-T, tế bào T biểu hiệu thụ thể kháng nguyên khảm (chimeric antigen receptor – CAR) được thiết kế để nhận diện và tiêu diệt tế bào ung thư. CAR-T cho những kết quả đầy hứa hẹn trong điều trị ung thư máu, nhưng gặp nhiều cản trở ở u đặc bởi nhiều nguyên nhân, trong đó có việc tấn công cả tế bào khỏe mạnh có cùng protein đích với tế bào ung thư. Ngược lại, liệu pháp TCR-T sử dụng các thụ thể tế bào T (T cell receptor – TCR) có nguồn gốc tự nhiên, khả năng phân biệt tốt hơn giữa tế bào khối u và tế bào bình thường, nhưng hiệu quả có nhiều hạn chế. Một nhóm nghiên cứu tại Đại học Oxford và Viện Ung thư Quốc gia (Hoa Kỳ), hợp tác với Đại học Montréal (Canada) đã tìm giải pháp khắc phục các nhược điểm trên bằng cách tạo ra các tế bào biểu hiện cả CAR và TCR. Họ đã kiểm chứng trên nền tảng robot IMMUNOtron thông lượng cao và mô hình động vật, kết quả cho thấy tín hiệu TCR hoạt động như một cái phanh để giảm thiểu phản ứng quá mức của CAR, thay vì kích hoạt chúng. Mô hình toán học lý thuyết đã xác định việc điều chỉnh phản ứng miễn dịch bằng cách sử dụng các TCR tự nhiên, và chứng minh được sự điều hòa phản ứng miễn dịch với khả năng cân bằng giữa “bàn đạp phanh” và “bàn đạp ga” của tế bào T. Từ đó, nhóm nghiên cứu phát triển sản phẩm CAR-T mới với Hệ thống phanh chống đối kháng (Antagonism-Enforced Braking System – AEBS), bằng cách thêm một TCR có nhiệm vụ ức chế CAR-T hoạt động trên mô khỏe mạnh bởi các protein trên tế bào bình thường, nhưng khi gặp phiên bản đột biến của các protein này trên tế bào ung thư thì kích thích hoạt động mạnh mẽ. Chiến lược này giúp AEBS CAR-T ít gây hại với tế bào khỏe mạnh, đồng thời tăng hiệu quả kháng u. Thành công này đã mở đường cho một chiến lược mới trong liệu pháp miễn dịch điều trị ung thư. Định hướng tiếp theo của nhóm nghiên cứu là tập trung vào việc tăng cường tương tác giữa các thụ thể và tế bào AEBS CAR-T, nhằm tạo ra sản phẩm miễn dịch chống ung thư an toàn hơn, hiệu quả hơn trong những năm tới trên nhiều loại bệnh ung thư. TÀI LIỆU THAM KHẢO Kondo T., et al. (2025). Engineering TCR-controlled fuzzy logic into CAR T cells enhances therapeutic specificity. Cell, 188(9), 2372-2389. DOI: https://doi.org/10.1016/j.cell.2025.03.017
23/01/2026
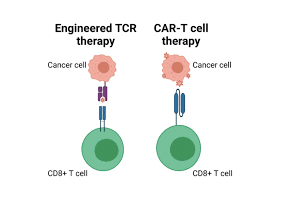
Cải biến di truyền giúp tăng cường hiệu quả liệu pháp tế bào miễn dịch trong điều trị ung thư: TCR-T và CAR-T
1. Liệu pháp miễn dịch tế bào T Các liệu pháp miễn dịch tế bào T khác nhau tùy thuộc vào nguồn gốc tế bào, cách thức xử lý ngoài cơ thể và phương thức tế bào T nhận diện mục tiêu khi được truyền cho bệnh nhân. Các chiến lược khai thác liệu pháp miễn dịch tế bào T bao gồm: - Liệu pháp tế bào lympho thâm nhiễm khối u (Tumor-Infiltrating Lymphocyte, TIL): sử dụng các tế bào T trong khối u, với thụ thể tế bào T tự nhiên nhận diện các mục tiêu trên tế bào ung thư (xem bài viết về liệu pháp TIL tại https://ysinhtebao.com/lieu-phap-tb-mien-dich-khac/lieu-phap-til-trong-dieu-tri-u-dac-trien-vong-va-thach-thuc). - Liệu pháp thụ thể tế bào T (T Cell Receptor-Engineered T Cell, TCR-T): Sử dụng các kỹ thuật di truyền để thiết kế các thụ thể tế bào T, bổ sung cho tế bào T giúp chúng nhận diện mục tiêu trên tế bào ung thư. - Liệu pháp tế bào T với thụ thể kháng nguyên khảm (Chimeric Antigen Receptor T cell, CAR-T): sử dụng kỹ thuật di truyền để tạo ra các thụ thể nhân tạo, cung cấp cho tế bào T giúp chúng phát hiện các mục tiêu trên tế bào ung thư mà thụ thể tự nhiên không nhận diện được. 2. Liệu pháp TCR-T: biến đổi di truyền thụ thể tế bào T Nhờ thụ thể tế bào T (T Cell Receptor – TCR), tế bào T có khả năng nhận biết tự nhiên đối với các mục tiêu như vi khuẩn, virus, tế bào ung thư,... và tiêu diệt chúng. Đối với liệu pháp TCR-T, các nhà nghiên cứu ung thư đã xác định một dấu hiệu trên các tế bào ung thư, thiết kế một TCR nhận dạng được dấu hiệu đó, sau đó tách tế bào T từ bệnh nhân và thêm vào đó gen mã hóa TCR đã thiết kế để tạo nên TCR-T phát hiện tốt các tế bào ung thư. Liệu pháp TCR-T đã được thử nghiệm lâm sàng để điều trị nhiều loại ung thư khác nhau, trong đó thu được những tín hiệu tích cực đối với u đặc. Tháng 08/2024, Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (US FDA) đã chấp thuận sản phẩm TECELRA (Afamitresgene autoleucel), là sản phẩm TCR-T tự thân hướng đến kháng nguyên A4 liên quan đến ung thư hắc tố (MAGE-A4) dùng trong điều trị sarcoma hoạt dịch. Các chiến lược hiện nay về TCR-T đang hướng đến khắc phục những nhược điểm khiến bệnh nhận hưởng những lợi ích hạn chế lâm sàng, bao gồm giảm độc tính trên bệnh nhân, tăng cường các dấu hiệu nhận diện khối u – đặc biệt là các tân kháng nguyên – để cải thiện hiệu quả và ngăn ngừa tổn thương cho các tế bào và mô khỏe mạnh. 3. Liệu pháp CAR-T: thụ thể nhân tạo nhận diện tế bào ung thư CAR-T là liệu pháp tế bào miễn dịch trong đó tế bào T được biến đối với một thụ thể nhân tạo, được gọi là thụ thể kháng nguyên khảm (Chimeric Antigen Receptor – CAR), để nhận diện tế bào ung thư. Tế bào T tự nhiên có TCR cho phép chúng phát hiện nhiều phân tử mà chúng xác định là tế bào ung thư, nhưng không phải tất cả các kháng nguyên, do đó các nhà nghiên cứu thiết kế nên CAR để phát hiện những thụ thể bề mặt mà TCR không nhận diện được. Liệu pháp CAR-T đã chứng minh hiệu quả trong điều trị các bệnh lý ác tính huyết học. Hiện tại đã có 7 sản phẩm được US FDA cấp phép: 5 sản phẩm nhận diện CD19 trong điều trị u lympho và bệnh bạch cầu, gồm KYMRIAH (Tisagenlecleucel, được cấp phép tháng 08/2017), YESCARTA (Axicabtagene ciloleucel, 10/2017), TECARTUS (Brexucabtagene autoleucel, 07/2020), BREYANZI (Lisocabtagene maraleucel, 02/2021), AUCATZYL (Obecabtagene autoleucel, 11/2024); 2 sản phẩm nhận diện kháng nguyên trưởng thành tế bào B trong điều trị đa u tủy xương, gồm ABECMA (Idecabtagene vicleucel, được cấp phép tháng 03/2021), CARVYKTI (Ciltacabtagene autoleucel, 02/2022). 4. Những khác biệt giữa liệu pháp TCR-T và CAR-T Cả hai liệu pháp này đều sử dụng các kỹ thuật di truyền để biến đổi tế bào T, khai thác sức mạnh của hệ thống miễn dịch nhằm điều trị ung thư, nhưng có một số khác biệt chính. Về mặt cấu trúc: TCR là các thụ thể tự nhiên hoặc được biến đổi hạn chế để nhận diện các kháng nguyên khối u. CAR được thiết kế nhân tạo để nhận diện kháng nguyên cụ thể, đồng thời người ta có thể bổ sung trên cấu trúc CAR các vùng giúp tăng cường hoạt động cũng như duy trì sự hoạt hóa và sống còn của tế bào T. Về khả năng nhận diện kháng nguyên: TCR nhận diện các kháng nguyên có trên bề mặt và bên trong tế bào, được trình diện trên bề mặt qua kháng nguyên bạch cầu người (HLA), cần có sự tương thích HLA giữa bệnh nhân và TCR. CAR nhận diện các kháng nguyên trên bề mặt tế bào và không phụ thuộc HLA. Vì thế, TCR có thể nhận diện kháng nguyên phổ rộng hơn CAR. Về ứng dụng lâm sàng: TCR-T có nhiều hứa hẹn với các dạng ung thư u đặc như u hắc tố, ung thư phổi, ung thư cổ tử cung,… CAR-T chủ yếu điều trị các bệnh lý ác tính về máu như bệnh bạch cầu cấp/mạn dòng lympho (ALL/CLL), u lympho tế bào B lớn (LBCLu lympho tế bào B lớn (LBCL), u lympho dòng lympho nhỏ (SLL), u lympho nang (FL), u lympho tế bào màng ngoài (MCL), đa u tủy xương,… và khó hiệu quả với u đặc do hàng rào mô, môi trường vi mô ức chế. TÀI LIỆU THAM KHẢO 1. Shafer P., et al. (2022). Cancer therapy with TCR-engineered T cells: current strategies, challenges, and prospects. Frontiers in immunology, 13, 835762. DOI: 10.3389/fimmu.2022.835762 2. Baulu E., et al. (2023). TCR-engineered T cell therapy in solid tumors: State of the art and perspectives. Science Advances, 9(7), eadf3700. DOI: 10.1126/sciadv.adf3700 3. Sterner R. C., et al. (2021). CAR-T cell therapy: current limitations and potential strategies. Blood cancer journal, 11(4), 69. DOI: 10.1038/s41408-021-00459-7 4. Chen Y. J., et al. (2023). CAR-T: what is next?. Cancers, 15(3), 663. DOI: 10.3390/cancers15030663 5. Haanen J., et al. (2024). Adoptive cell therapy for solid tumors: current status in melanoma and next-generation therapies. American Society of Clinical Oncology Educational Book, 44(3), e431608. DOI: 10.1200/EDBK_431608 6. https://www.fda.gov/vaccines-blood-biologics/cellular-gene-therapy-products/approved-cellular-and-gene-therapy-products
23/01/2026
Nguy cơ ung thư thứ phát sau điều trị bằng liệu pháp CAR-T: kết luận của Cơ quan Dược phẩm Châu Âu (EMA) dựa trên đánh giá 38 trường hợp nghi ngờ
Liệu pháp tế bào T mang thụ thể kháng nguyên khảm (chimeric antigen receptor T-cell, CAR-T) là liệu pháp điều trị ung thư và một số bệnh lý khác, sử dụng các tế bào T chứa thụ thể có khả năng nhận diện một yếu tố nhất định trên tế bào đích để tiêu diệt chúng. Tính đến nay, Cơ quan Dược phẩm Châu Âu (the European Medicines Agency, EMA) đã khuyến cáo lưu hành 6 sản phẩm CAR-T để điều trị các bệnh lý ung thư huyết học, bao gồm tisagenlecleucel (Kymriah), lisocabtagene maraleucel (Breyanzi), axicabtagene ciloleucel (Yescarta), brexucabtagene autoleucel (Tecartus), idecabtagene vicleucel (Abecma) và ciltacabtagene autoleucel (Carvykti). Quy trình sản xuất CAR-T thường sử dụng vector lentivirus để chuyển gen vào tế bào T, mang đến những lo ngại về việc chèn trình tự DNA vào gen hoạt động, có thể góp phần gây ung thư. Rủi ro này được nêu rõ trong thông tin sản phẩm và khuyến nghị cần theo dõi bệnh nhân suốt đời, kết hợp đánh giá chặt chẽ những phản ứng bất lợi sau khi sử dụng sản phẩm. Cuối năm 2023, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (the United States Food and Drug Administration, US FDA) đã thông báo ghi nhận nhiều trường hợp bệnh nhân được phát hiện bệnh lý ác tính tế bào T sau khi sử dụng liệu pháp CAR-T. Trong nghiên cứu này, các nhà nghiên cứu của EMA kết hợp nhiều đơn vị trên toàn châu Âu đã phân tích các trường hợp mắc bệnh ác tính tế bào T sau sử dụng liệu pháp CAR-T, nhằm đánh giá sự rủi ro của liệu pháp này trong khía cạnh gây ung thư thứ phát. Tính đến ngày 11/04/2024, đã có 38 trường hợp bệnh nhân 29-80 tuổi mắc bệnh ác tính tế bào T (trong tổng số khoảng 42.500 bệnh nhân sử dụng) sau khi điều trị với 1 trong 6 sản phẩm CAR-T được EMA khuyến nghị cấp phép (tỷ lệ khoảng 1/1.000). Hầu hết các trường hợp này được chẩn đoán trong vòng 12 tháng sau điều trị. Trong 38 bệnh nhân này, 19 bệnh nhân được xét nghiệm sự hiện diện của gen chuyển CAR trong mẫu khối u, và phát hiện ở 7 trường hợp, số lượng bản sao thấp ở 5 trường hợp, và 7 trường hợp còn lại âm tính. Không có dữ liệu cho thấy bất kỳ trường hợp nào có dòng tế bào CAR chiếm ưu thế ở thời điểm đánh giá, chưa phát hiện loại virus nào liên quan đến vector chuyển gen có khả năng nhân lên ở bất cứ thời điểm nào được khảo sát. Nhóm nghiên cứu nhận định: nguy cơ mắc bệnh ác tính thứ phát có nguồn gốc từ tế bào T dường như thấp (tỷ lệ khoảng 1/1.000), và "có khả năng" các bệnh này có liên quan đến liệu pháp CAR-T. Dựa trên những dữ liệu hiện có, kết hợp xem xét cơ chế và tác dụng của liệu pháp CAR-T, EMA kết luận rằng đây là tác dụng chung của nhóm sản phẩm, ngay cả khi không phải tất cả các sản phẩm đều có trường hợp mắc bệnh lý ác tính tế bào T được báo cáo. Kết luận này đã dẫn đến các hành động quản lý tập trung vào các biện pháp giảm thiểu rủi ro, bao gồm cập nhật thông tin sản phẩm, kế hoạch quản lý rủi ro, tài liệu giáo dục, tăng cường xét nghiệm di truyền trên các mẫu khối u còn lại sau điều trị,… Các cơ chế cơ bản dẫn đến sự phát triển của các bệnh ung thư thứ phát có nguồn gốc từ tế bào T ở bệnh nhân sau sử dụng CAR-T vẫn chưa được làm rõ. Những khía cạnh được cân nhắc đến bao gồm nguy cơ đột biến chèn khi chuyển gen, quá trình sản xuất ảnh hưởng đến điều hòa biểu hiện gen, điều trị điều kiện hóa trước truyền CAR-T làm suy yếu khả năng loại bỏ các tế bào tiền ác tính,… Mắc dù vậy, vẫn cần có những quan sát tích lũy trong quá trình thử nghiệm và lưu hành sản phẩm CAR-T để theo dõi được số lượng bệnh nhân lớn hơn để đưa ra được những kết luận chính xác. TÀI LIỆU THAM KHẢO Berg P., et al. (2025). Secondary malignancy of T-cell origin after CAR T-cell therapy: EMA’s conclusions from the evaluation of 38 suspected cases. Gene Therapy, 1-6. DOI: https://doi.org/10.1038/s41434-025-00586-x
23/01/2026
Liệu pháp kháng thể có tiềm năng thay thế hóa – xạ trị trong phác đồ điều kiện hóa trước ghép tế bào gốc
Ghép tế bào gốc tạo máu (Hematopoietic Stem Cell Transplantation – HSCT) là quá trình cấy ghép tế bào gốc tạo máu từ tủy xương, máu ngoại vi, máu cuống rốn,… vào cơ thể người bệnh, để chữa các bệnh lý huyết học, miễn dịch, di truyền, ung thư,…
22/01/2026
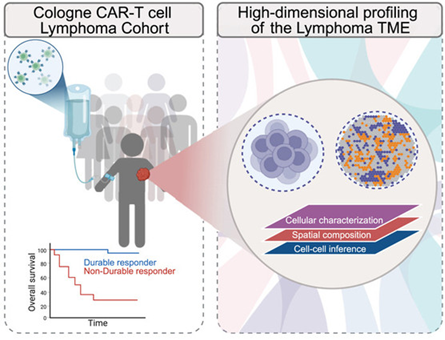
Phát hiện “hàng rào” tế bào làm giảm hiệu quả điều trị của liệu pháp CAR-T trong bệnh u lympho
Liệu pháp CAR-T sử dụng các tế bào T mang thụ thể kháng nguyên khảm (Chimeric Antigen Receptor – CAR) được thiết kế nhân tạo, nhờ đó chúng có thể phát hiện đặc hiệu và tiêu diệt các tế bào ung thư. CAR-T đã tạo nên bước đột phá trong điều trị nhiều bệnh lý huyết học ác tính, trong đó có u lympho tế bào B tái phát hoặc kháng trị - loại u lympho không Hodgkin phổ biến nhất. Tuy nhiên, có đến 50% số bệnh nhân được điều trị bằng liệu pháp này không duy trì khả năng đáp ứng ban đầu, hoặc tái phát sau điều trị, thậm chí tử vong. Cơ chế kháng CAR-T của bệnh này vẫn chưa được hiểu rõ hoàn toàn. Trong một nghiên cứu mới đăng trên tạp chí Cancer Cell tháng 5 năm 2025, các nhà khoa học đã phân tích sự khác biệt giữa những bệnh nhân có đáp ứng lâu dài so với nhóm kém đáp ứng với liệu pháp CAR-T. Nhóm tác giả đã phân tích mẫu u lympho của các bệnh nhân: giải trình tự RNA số lượng lớn để phân tích hoạt đột gen tổng thể của toàn bộ mẫu, giải trình tự RNA tế bào đơn để kiểm tra hoạt động gen của từng tế bào, tạo bản đồ vị trí các loại tế bào khác nhau và sự tương tác giữa chúng,… Mục tiêu cuối cùng là xác định các mục tiêu cụ thể trong môi trường vi mô của khối u có thể được điều chỉnh để cải thiện liệu pháp tế bào CAR-T. Nhóm nghiên cứu đã xác định được các tế bào đơn dòng tủy dương tính với CSF1R (một loại thụ thể có mặt trên bề mặt của các tế bào như microglia và đại thực bào, đóng vai trò quan trọng trong sự phát triển, sống sót và duy trì của microglia), còn gọi là tế bào LAMM, tăng đáng kể ở những bệnh nhân đáp ứng kém. Họ phát hiện ra rằng tế bào LAMM ức chế CAR-T thông qua con đường liên quan đến tín hiệu prostaglandin E2 (PGE2), sự tương tác giữa LAMM và một số thụ thể trên tế bào T làm vô hiệu hóa khả năng tăng sinh và tiêu diệt tế bào ung thư của CAR-T. Kết quả này cho thấy các tế bào LAMM hoạt động như một rào cản, bảo vệ khối u khỏi tế bào CAR-T. Tuy nhiên, hiện tại đã có thuốc được phê duyệt với tác dụng ức chế CSF1R (Sotuletinib hay BLZ-945), có thể phá vỡ hàng rào này, khi kết hợp với CAR-T trên mô hình chuột đã cải thiện hiệu quả điều trị một cách đáng kể. Đây có thể là bước đột phá trong chiến lược điều trị cho hàng nghìn bệnh nhân u lympho tế bào B kháng trị với liệu pháp CAR-T. TÀI LIỆU THAM KHẢO Stahl D., et al. (2025). CSF1R+ myeloid-monocytic cells drive CAR-T cell resistance in aggressive B cell lymphoma. Cancer cell. DOI: https://doi.org/10.1016/j.ccell.2025.05.013
22/01/2026
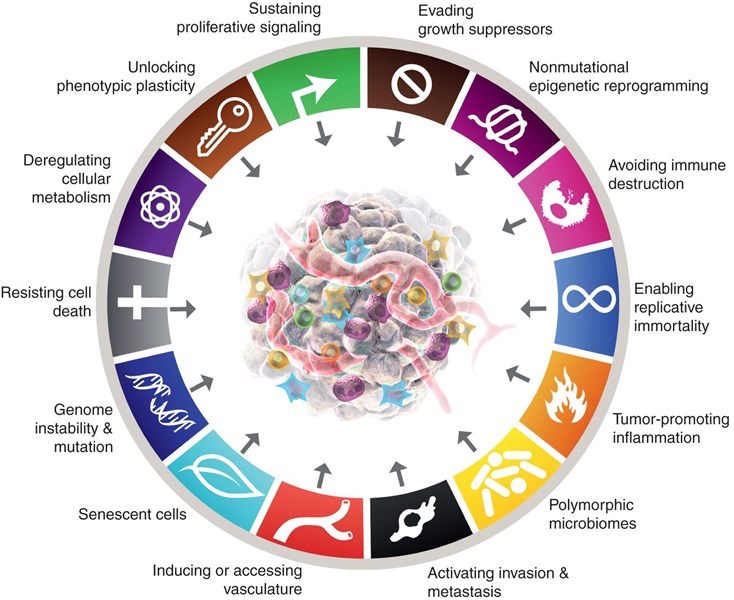
Những dấu hiệu đặc trưng của ung thư (The Hallmarks of Cancer)
1. Khái quát về ung thư Theo thống kê của Tổ chức Y tế Thế giới (WHO), ung thư là nguyên nhân gây tử vong đứng thứ hai trên toàn thế giới với khoảng 20 triệu ca mới mắc và gần 10 triệu người tử vong hằng năm, và có xu hướng ngày càng tăng trong những năm tiếp theo. Ung thư là tập hợp các bệnh lý liên quan đến việc tăng sinh tế bào mất kiểm soát, những tế bào đó có khả năng xâm lấn và phá hủy các mô khác trong cơ thể. Các tế bào ung thư có thể xuất hiện ở một khu vực sau đó lan ra các vùng khác, có thể tạo nên một khối u rõ ràng, nhưng đôi khi cũng có thể được phân bố đều (không tạo nên bướu rõ ràng). Có hơn 100 loại ung thư khác nhau, thường được gọi tên theo cơ quan mà nó phát sinh, ví dụ: ung thư đại trực tràng, ung thư tuyến giáp, ung thư tụy,… Ung thư cũng có thể được gọi theo loại tế bào hình thành chúng như ung thư biểu mô (carcinoma), ung thư mô liên kết (sarcoma), bệnh bạch cầu (leukemia),… Năm 2000, Robert Weinberg và Douglas Hanahan đã mô tả 6 đặc điểm mà hầu hết (nếu không muốn nói là tất cả) các loại ung thư ở người đều có, bên cạnh “đặc điểm hỗ trợ” các tế bào tiền ác tính có được 6 dấu hiệu đặc trưng đó, đây là bài viết gốc về “The Hallmarks of Cancer”. Những tiến bộ trong nghiên cứu ung thư đã thúc đẩy Weinberg và Hanahan cập nhật năm 2011, và gần nhất Hanahan đã xem xét lại danh sách này năm 2022. Những dấu hiệu đặc trưng của ung thư - mô tả mới nhất năm 2022 2. Mô tả đầu tiên năm 2000 về những dấu hiệu đặc trưng của ung thư - Tự cung cấp tín hiệu tăng trưởng: Khác với tế bào bình thường cần có tín hiệu tăng trưởng từ bên ngoài để nhân lên, các tế bào ung thư tự tạo ra hầu hết các tín hiệu tăng trưởng nhằm làm giảm đáng kể hoặc loại bỏ sự phụ thuộc của chúng vào các kích thích bên ngoài. - Không nhạy cảm với các tín hiệu ức chế tăng trưởng: Các tế bào bình thường được điều hòa bởi những tín hiệu kiểm soát, đẩy chúng ra khỏi chu kỳ tế bào và đi vào trạng thái nghỉ tạm thời hoặc biệt hóa sau lần nguyên phân cuối cùng. Các tế bào ung thư tránh các tín hiệu này bằng cách phá vỡ các điểm kiểm soát chu kỳ tế bào, giúp chúng có thể nhân lên vô hạn. - Tránh sự chết tế bào theo chương trình (Apoptosis): Apoptosis là một dạng chết tế bào theo chương trình đóng vai trò quan trọng trong việc loại bỏ các tế bào dư thừa, bị tổn thương hoặc những tế bào sai hỏng, bất thường. Những tế bào ung thư tránh được các cơ chế đưa chúng vào apoptosis và phát triển mất kiểm soát. - Tiềm năng sao chép vô hạn: Các tế bào bình thường sẽ ngừng phân chia tại một thời điểm nhất định do sự rút ngắn đầu mút nhiễm sắc thể (telomere). Các tế bào ung thư mất cơ chế kiểm soát đó nhờ sự kích hoạt enzyme telomerase để kéo dài đầu mút nhiễm sắc thế, giúp chúng phân chia vô hạn và trở thành tế bào bất tử. - Sự hình thành mạch máu: Khối u có thể giải phóng các tín hiệu kích thích tạo mạch máu, nhờ đó có nguồn cung cấp oxy và chất dinh dưỡng để chúng phát triển. - Xâm lấn mô và di căn: Tế bào ung thư có thể tách khỏi vị trí hoặc cơ quan ban đầu để xâm lấn các mô xung quanh và lan rộng (di căn) đến các bộ phận xa của cơ thể. Đây là yếu tố quyết định khối u lành tính hay ác tính, và là đặc tính cho phép chúng phát tán khắp cơ thể. Các tế bào ung thư phải trải qua vô số thay đổi để có được khả năng di căn, bắt đầu bằng sự xâm lấn cục bộ vào các mô xung quanh, sau đó xâm lấn các mạch máu, tồn tại trong môi trường khắc nghiệt của hệ tuần hoàn, thoát khỏi hệ thống này và bắt đầu phân chia trong mô mới. - Sự bất ổn của hệ gen (đặc điểm hỗ trợ): Các đặc điểm trên có được thông qua những thay đổi trong bộ gen của tế bào ung thư. Hiện nay người ta đã biết trong các tế bào ung thư có sự kích hoạt các gen gây ung thư (oncogene) và ức chế các gen kiềm chế khối u (tumor suppresor gene). Hiểu một cách đơn giản, một số kiểu gen đột biến mang lại lợi thế chọn lọc cho một số nhóm tế bào, và ung thư tiến triển trải qua nhiều bước là kết quả của một chuỗi những sự thích nghi được kích hoạt bởi sự tích lũy ngẫu nhiên các kiểu gen đột biến. Mô tả đầu tiên về những dấu hiệu đặc trưng của ung thư theo Hanahan và Weinberg năm 2000 3. Thế hệ tiếp theo về những dấu hiệu đặc trưng của ung thư (2011) - Thay đổi sự trao đổi chất của tế bào: Các tế bào bình thường sử dụng oxy để chuyển hóa glucose tạo ra năng lượng, còn các tế bào ác tính có xu hướng chuyển sang quá trình đường phân hiếu khí (được gọi là hiệu ứng Warburg), mặc dù hiệu quả tạo năng lượng thấp hơn nhưng nhanh hơn và tạo ra một số chất trung gian hỗ trợ quá trình tăng sinh nhanh chóng của tế bào ung thư. Ngoài ra, các tế bào ung thư có thể sử dụng lactate làm nguồn năng lượng chính của chúng. - Trốn tránh hệ thống miễn dịch: Các tế bào ung thư sử dụng nhiều chiến lược khác nhau cho phép chúng trốn tránh hệ thống miễn dịch của cơ thể. Một trong những cơ chế phổ biến nhất là biểu hiện protein PD-L1 và ức chế biểu hiện MHC I trên bề mặt khiến tế bào T không nhận diện được. - Phản ứng viêm thúc đẩy hình thành khối u (đặc điểm hỗ trợ): Viêm là phản ứng bảo vệ bình thường của cơ thể đối với những tác nhân gây bệnh hoặc tổn thương. Tuy nhiên, các bằng chứng đã cho thấy tác dụng ngược lại ở trong các khối u, phản ứng viêm là yếu tố tăng cường cho quá trình hình thành và tiến triển của khối u, có khả năng thúc đẩy sự phát triển của khối u mới phát triển thành ung thư hoàn chỉnh. Các tế bào viêm có thể giải phóng các chất hóa học có khả năng gây đột biến đối với các tế bào ung thư gần đó, đẩy nhanh quá trình chọn lọc di truyền của chúng theo hướng ác tính hóa cao hơn. Cập nhật về những dấu hiệu đặc trưng của ung thư theo Hanahan và Weinberg năm 2011 4. Những chiều hướng mới (2022) - Mở khóa tính mềm dẻo về kiểu hình: Các tế bào bình thường khi biệt hóa sẽ ngừng tăng sinh vĩnh viễn và chỉ thực hiện chức năng, ngược lại các tế bào ác tính tránh được sự biệt hóa và mở khóa cái được gọi là tính mềm dẻo kiểu hình để tiếp tục phát triển. Có nhiều cách để chúng làm điều này, ví dụ các tế bào đang tiến tới biệt hóa hoàn toàn sẽ giải biệt hóa để trở lại giống tế bào tiền thân, các tế bào ung thư có nguồn gốc từ tế bào chưa biệt hóa sẽ dừng quá trình biệt hóa, hoặc các tế bào đã được định hướng biệt hóa theo kiểu nhất định có thể chuyển chương trình (hoặc biệt hóa chéo) để hình thành những đặc điểm không liên quan đến định hướng biệt hóa ban đầu của chúng. - Các tế bào lão hóa: Lão hóa tế bào là một dạng ngừng tăng sinh thường không thể đảo ngược, bổ sung cho quá trình chết tế bào theo chương trình để vô hiệu hóa và loại bỏ kịp thời các tế bào bệnh, rối loạn chức năng hoặc không cần thiết. Tuy nhiên những bằng chứng hiện nay cho thấy các tế bào lão hóa là một thành phần quan trọng của vi môi trường khối u, trong một số bối cảnh nhất định chúng có thể kích thích sự phát triển của khối u và tiến triển ác tính. - Tái lập trình di truyền ngoại gen không đột biến (đặc điểm hỗ trợ): Di truyền ngoại gen (epigenetic) là thuật ngữ để chỉ những thay đổi về mặt di truyền trong kiểu hình tế bào nhưng không thay đổi về số lượng bản sao cũng như trình tự trong chuỗi DNA, bao gồm các cơ chế methyl hóa cytosine trên DNA, methyl hóa/acetyl hóa/phosphoryl hóa histone, hay RNA không mã hóa. Những cơ chế đó có thể điều hòa các gen để thay đổi biểu hiện gen, kích hoạt các gen chỉ hoạt động trong giai đoạn phôi sớm giúp tế bào liên tục phân chia, thay đổi vi môi trường khối u,… từ đó thúc đẩy sự phát triển của khối u. - Sự đa hình hệ vi sinh vật (đặc điểm hỗ trợ): Cơ thể chúng ta bị xâm chiếm bởi một lượng lớn các vi sinh vật (gần 40 nghìn tỷ tế bào) sống trong các cơ quan của cơ thể, gọi là microbiome, chúng đóng góp quan trọng đối với sức khỏe con người. Nhiều loài vi sinh vật trong số này gây nên những tác dụng chống lại hoặc thúc đẩy bệnh ung thư, cũng như phản ứng của cơ thể đối với các liệu pháp điều trị. Những bổ sung về những dấu hiệu đặc trưng của ung thư theo Hanahan năm 2022 5. Những thông tin trái chiều - Ngay sau phiên bản đầu tiên, Lazebnik đã có bài viết trên Nature Reviews Cancer năm 2010 chỉ ra rằng 5 trong số đó cũng là đặc điểm của khối u lành tính, chỉ có khả năng xâm lấn và di căn là đặc trưng cho các tế bào ác tính - Năm 2013, Sonnenschein và Soto cho rằng dữ liệu gốc cho hầu hết các dấu hiệu này còn thiếu, đồng thời chỉ ra ung thư là một căn bệnh ở cấp độ mô và các dấu hiệu ở cấp độ tế bào này gây nên những hiểu lầm về bản chất của ung thư. - Năm 2017, Fouad và Aanei cho rằng các dấu hiệu này có sự trùng lặp (tự cung cấp tín hiệu tăng trưởng và không nhạy cảm với tín hiệu ức chế tăng trưởng), hoặc chưa chính xác (apoptosis có xảy ra ở tế bào ung thư), các dấu hiệu đều được mổ xẻ kỹ và chỉ ra một số điểm bất hợp lý. TÀI LIỆU THAM KHẢO 1. Hanahan D., and Weinberg, R.A. (2000). The hallmarks of cancer. Cell, 100(1), 57-70. 2. Hanahan D., and Weinberg, R.A. (2011). Hallmarks of cancer: the next generation. Cell, 144(5), 646-674. 3. Hanahan D. (2022). Hallmarks of cancer: new dimensions. Cancer discovery, 12(1), 31-46. 4. Lazebnik Y. (2010). What are the hallmarks of cancer?. Nature Reviews Cancer, 10(4), 232-233. 5. Sonnenschein C., and Soto A.M. (2013). The aging of the 2000 and 2011 Hallmarks of Cancer reviews: a critique. Journal of biosciences, 38, 651-663. 6. Fouad Y. A., and Aanei C. (2017). Revisiting the hallmarks of cancer. American journal of cancer research, 7(5), 1016.
22/01/2026







