Liệu pháp CAR-T đồng loại: Quy trình sản xuất với những triển vọng và thách thức để có thể ứng dụng lâm sàng
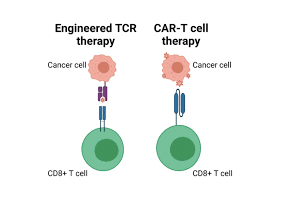
Liệu pháp tế bào T mang thụ thể kháng nguyên khảm (chimeric antigen receptor T-cell, CAR-T) đã tạo nên bước ngoặt trong điều trị ung thư, với khả năng nhắm đích vào một thụ thể xác định trên tế bào ác tính để phát hiện đặc hiệu và tiêu diệt hiệu quả những tế bào đó. So với CAR-T tự thân đang được sử dụng phổ biến hiện nay, liệu pháp CAR-T đồng loại (allo-CAR-T) có chi phí sản xuất thấp hơn, sẵn sàng sử dụng cho bệnh nhân ngay khi cần, đã được chuẩn hóa quy trình sản xuất, nguồn tế bào phù hợp hơn,… nên có triển vọng giúp bệnh nhân ung thư có thể tiếp cận nhanh chóng, dễ dàng hơn với giá thấp hơn.
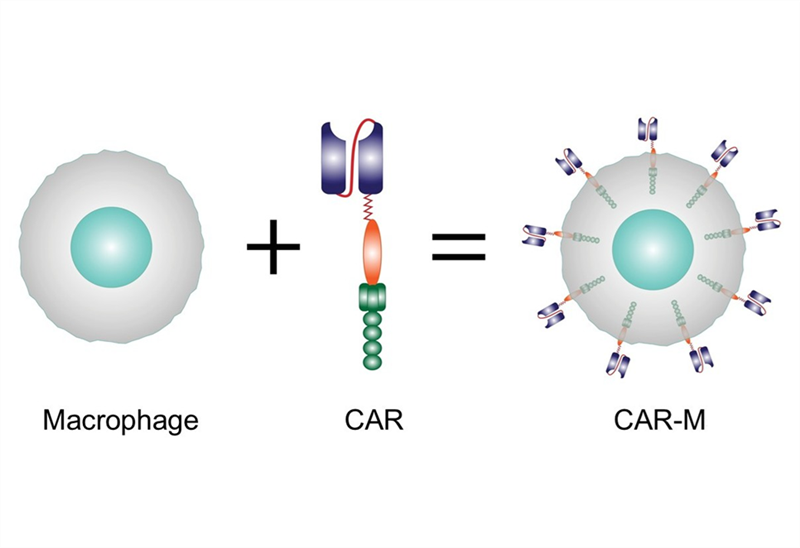
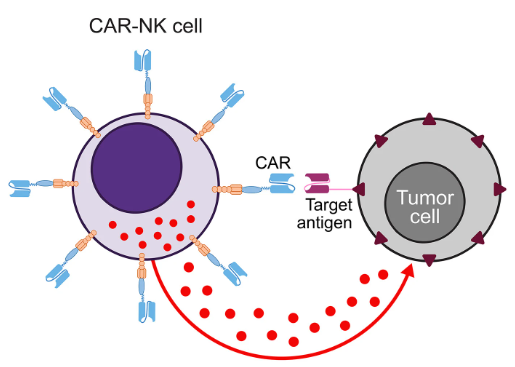
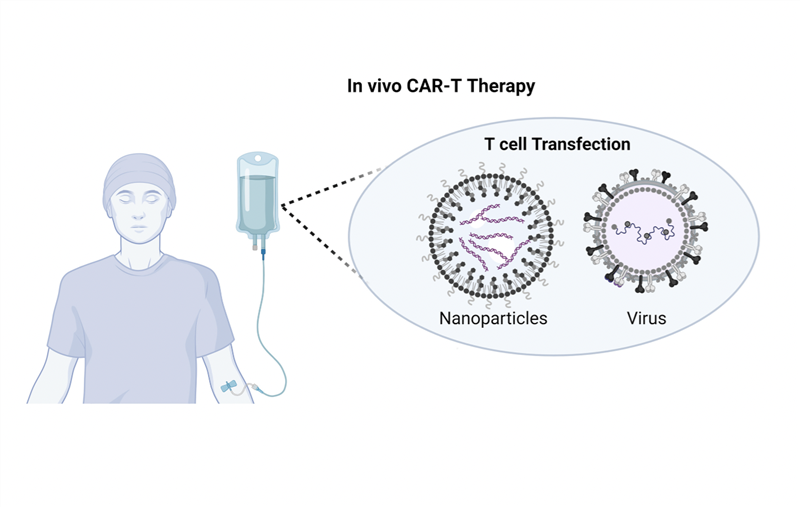
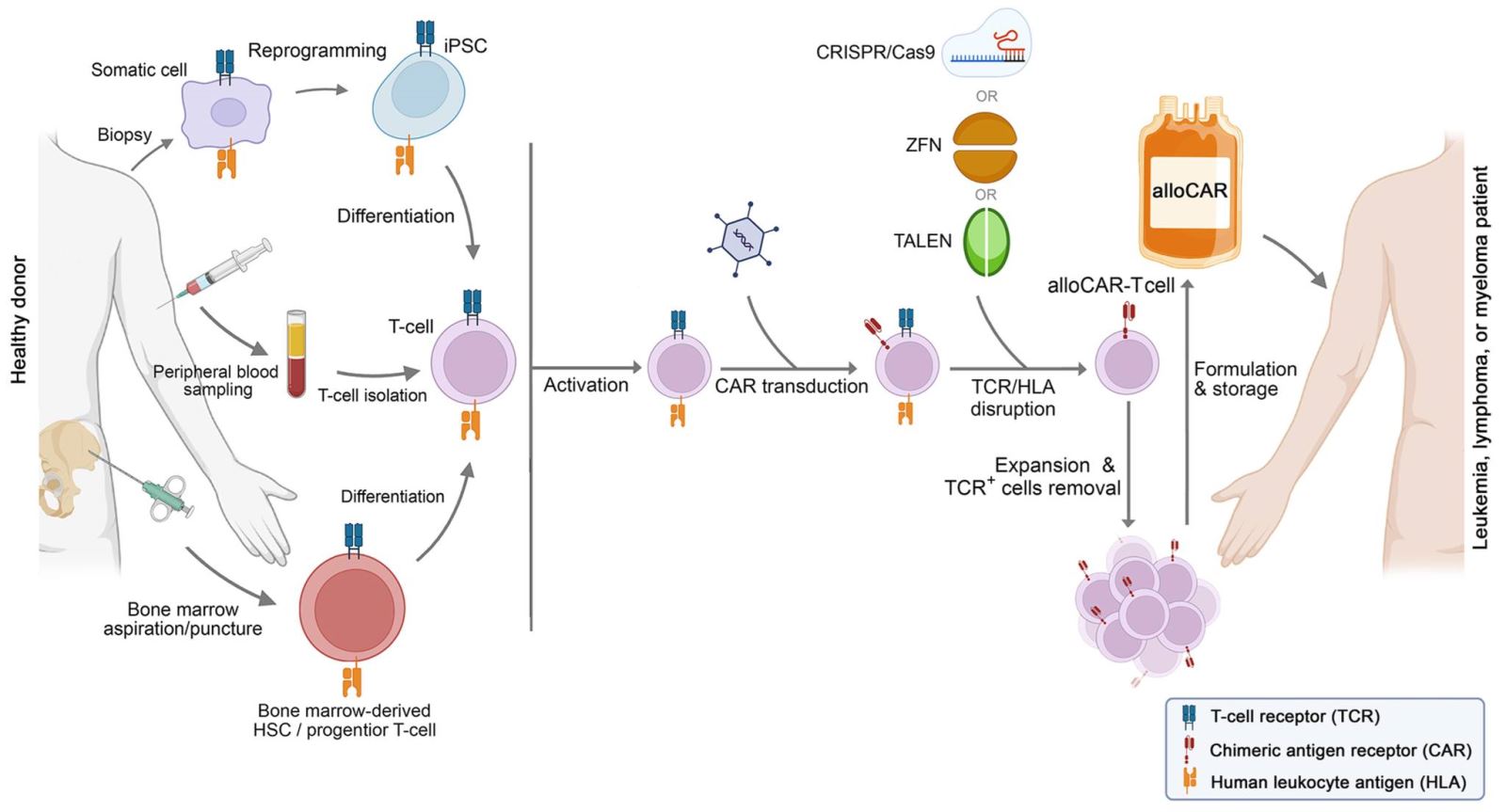
Quy trình sản xuất allo-CAR-T (hình ảnh minh họa) nhìn chung có nhiều điểm tương tự quy trình sản xuất CAR-T tự thân. Quá trình sản xuất được bắt đầu bằng việc lựa chọn người hiến tặng khỏe mạnh, sau đó thu thập một lượng tế bào T phù hợp từ máu ngoại vi, hoặc thu nhận tế bào T bằng các cách khác như sinh thiết tế bào soma (tái lập trình thành tế bào gốc đa năng cảm ứng (iPSC) và biệt hóa thành tế bào T), hoặc tách tế bào tủy xương (biệt hóa tế bào gốc tạo máu (HSC) hoặc tế bào tiền thân thành tế bào T). Sau đó, tế bào T được hoạt hóa và chuyển gen để biểu hiện cấu trúc CAR, đồng thời phá vỡ các cấu trúc có sẵn gây phản ứng miễn dịch thải ghép, với các công cụ chuyển gen như TALEN, ZFN, CRISPR/Cas9. Allo-CAR-T được nhân lên ex vivo, kết hợp loại bỏ những tế bào biểu hiện thụ thể tế bào T (TCR). Sản phẩm cuối cùng được chia thành các liều điều trị khác nhau và được bảo quản đông lạnh. Khi bệnh nhân có chỉ định sử dụng, allo-CAR-T được rã đông và truyền cho bệnh nhân.
1. Nguồn tế bào T trong sản xuất allo-CAR-T
Allo-CAR-T được nuôi cấy từ các tế bào T, tách ra trong hỗn hợp tế bào đơn nhân máu ngoại vi (Peripheral Blood Mononuclear Cell, PBMC) của người hiến khỏe mạnh. Trong số tất cả các tế bào T đang lưu thông, tế bào αβT (alpha-beta T) chiếm khoảng 95%, biểu hiện bề mặt với các chuỗi thụ thể tế bào T (T cell receptor, TCR) loại α và β, nhận diện kháng nguyên thông qua TCR của chúng phụ thuộc vào kháng nguyên bạch cầu người (Human Leukocyte Antigen, HLA). Điều đó khiến αβT dễ gây ra bệnh ghép chống chủ (Graft-versus-Host Disease, GvHD), biến chứng nguy hiểm do các tế bào của người hiến nhận diện mô vật chủ là tác nhân lạ và tấn công chúng. Vì vậy, để dùng tế bào αβT sản xuất allo-CAR-T, các biện pháp chống GvHD và đào thải đồng loại cần được tính đến, bao gồm phá vỡ/bất hoạt TCR, HLA, CD52,…
Tế bào γδT (gamma-delta T) biểu hiện bề mặt với các TCR-γ và TCR-δ, nhận diện kháng nguyên không phụ thuộc HLA, một nguồn thích hợp để tạo ra allo-CAR-T mà không gây GvHD. Trở ngại lớn nhất của chúng là chiếm tỷ lệ thấp (dưới 10%) trong PBMC.
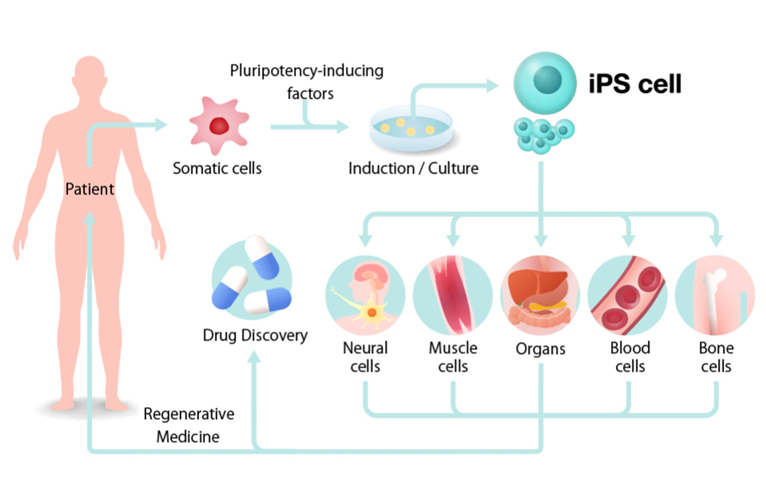
Một hướng đi khác là sinh thiết thu tế bào soma từ người hiến, sau đó tái lập trình thành tế bào gốc đa tiềm năng cảm ứng (induced Pluripotent Stem Cell, iPSC). Các nhóm iPSC với HLA xác định được lưu trữ trong ngân hàng, tạo nên nguồn tế bào hiến phù hợp HLA cho từng nhóm bệnh nhân, hơn nữa iPSC được can thiệp xóa HLA trở thành một nguồn tế bào hứa hẹn không gây phản ứng GvHD. Từ iPSC, người ta có thể biệt hóa thành tế bào T để sản xuất allo-CAR-T. Trở ngại của iPSC là khả năng tạo u quái dẫn đến hạn chế sử dụng lâm sàng đối với các sản phẩm có nguồn gốc từ chúng, tuy nhiên, nhiều nghiên cứu đã thiết lập các quy trình loại bỏ khả năng tạo u quái, đồng thời phát triển các quy trình sản xuất tốt (Good Manufacturing Practice, GMP) để sử dụng iPSC.
Ghép tế bào gốc tạo máu (Hematopoietic Stem Cell, HSC) đồng loại là một liệu pháp hứa hẹn cho các bệnh nhân ung thư máu, đồng thời HSC có thể biệt hóa thành dòng T để tạo ra allo-CAR-T. Các phương pháp tiêu chuẩn để đạt số lượng tế bào T cao bao gồm tách từ máu ngoại vi và lấy tủy xương, ngoài ra máu cuống rốn cũng là nguồn HSC đầy tiềm năng. Trở ngại đối với nguồn tế bào này là HSC (cũng như iPSC) có tính gốc mạnh, nên được xem xét duy trì tính gốc, tránh biệt hóa không mong muốn tạo nên nhiều dạng tế bào lạ, đồng thời thay đổi sự ổn định bộ gen và tính an toàn cho GMP của allo-CAR-T. Dạng tế bào tiền thân lympho (có nhiều trong tủy xương và máu cuống rốn) cũng đầy tiềm năng trong sản xuất allo-CAR-T, với khả năng biệt hóa hướng đích cao thành tế bào T (và NK).
2. Cải biến di truyền trong quá trình sản xuất allo-CAR-T
Khi sản xuất allo-CAR-T từ tế bào T thu nhận từ người hiến, các phương pháp biến đổi gen nhằm phá vỡ các cấu trúc liên quan đến GvHD và đào thải là rất quan trọng, như đã nói ở trên. Có ba chiến lược được sử dụng để thao tác với gen đích cụ thể, bao gồm TALEN (Transcription Activator-Like Effector Nuclease), ZFN (Zinc Finger Nuclease), CRISPR/cas9 (Clustered Regularly Interspaced Short Palindromic Repeats). Nhìn chung, đây là những công cụ phá bỏ hoặc bất hoạt những cấu trúc gây nên khả năng nhận diện kháng nguyên phụ thuộc HLA của tế bào αβT, trong đó TALEN và ZFN giúp thao tác chính xác tại vị trí mong muốn hơn so với CRISPR/cas9.
Phương pháp đưa gen CAR vào tế bào T được sử dụng rộng rãi nhất vẫn là các vector dựa trên virus. Cách thức này vẫn tiềm ẩn những nghi ngại về an toàn sinh học, khi sản phẩm có thể chứa các retrovirus có khả năng sao chép. Ngoài ra, một số hệ thống chuyển gen khác cũng được tính đến, bao gồm transposon (“gen nhảy”) và CRISPR/cas9, tuy nhiên hiệu quả chuyển gen thấp hơn nhiều so với vector virus.
Nhìn chung, việc cải biến di truyền tế bào T để biểu hiện cấu trúc CAR, đồng thời loại bỏ các yếu tố có thể gây GvHD và thải ghép cần thiết phải thực hiện trong quy trình sản xuất allo-CAR-T. Tuy nhiên, các kỹ thuật chỉnh sửa gen có thể dẫn đến các kết quả không mong muốn, như ảnh hưởng đến vị trí không mong muốn, hay tái sắp xếp lại bộ gen, ảnh hưởng đến độ an toàn của liệu pháp. Có lẽ vì vậy mà nhiều allo-CAR-T vẫn đang dừng lại trong các thử nghiệm lâm sàng.
3. Nuôi cấy tăng sinh, chia liều và bảo quản allo-CAR-T
Sau khi giải quyết các vấn đề trên, tế bào CAR-T được nuôi cấy tăng sinh lên số lượng lớn với quy trình được chuẩn hóa. Sau đó, sản phẩm được chia ra các liều lượng điều trị khác nhau với chất lượng đồng nhất và lưu trữ đông lạnh. Do không sản xuất liều lượng nhỏ phù hợp cho từng bệnh nhân, chi phí sản xuất allo-CAR-T thấp hơn rất nhiều so với CAR-T tự thân (ước chừng 3.990–10.000 USD, so với mức giá trên 300.000 USD của các sản phẩm CAR-T tự thân hiện có trên thị trường). Ngoài ra, CAR-T tự thân cần lấy máu từ bệnh nhân và sản xuất trong thời gian tối thiểu 2 tuần, với thời gian chờ đợi và khả năng thành công không chắc chắn, ngược lại allo-CAR-T đã được đóng gói sẵn, có thể truyền cho bệnh nhân ngay khi họ được chỉ định sẵn sàng sử dụng.
Mặc dù allo-CAR-T đã chứng minh hiệu quả chống khối u và tính an toàn tương tự như CAR-T tự thân, tuy nhiên vẫn cần có thêm nhiều nghiên cứu hơn nữa với thời gian theo dõi kéo dài. Khả năng chỉnh sửa đa gen của allo-CAR-T biến chúng thành ứng cử viên tuyệt vời với tiềm năng điều trị cao cho nhiều loại ung thư khác nhau.
TÀI LIỆU THAM KHẢO
1. Depil S., et al. (2020). ‘Off-the-shelf’allogeneic CAR T cells: development and challenges. Nature reviews Drug discovery, 19(3), 185-199. DOI: https://doi.org/10.1038/s41573-019-0051-2
2. Bedoya M. D., et al. (2021). Allogeneic CAR T cells: an alternative to overcome challenges of CAR T cell therapy in glioblastoma. Frontiers in immunology, 12, 640082. DOI: https://doi.org/10.3389/fimmu.2021.640082
3. Chen S., and van den Brink M. R. (2024). Allogeneic “Off-the-Shelf” CAR T cells: Challenges and advances. Best Practice & Research Clinical Haematology, 37(3), 101566. DOI: https://doi.org/10.1016/j.beha.2024.101566
4. Sasu B. J., et al. (2024). Allogeneic CAR T cell therapy for cancer. Annual Review of Cancer Biology, 8(2024), 227-243. DOI: https://doi.org/10.1146/annurev-cancerbio-062822-023316
5. Mansoori S., et al. (2024). Recent updates on allogeneic CAR-T cells in hematological malignancies. Cancer Cell International, 24(1), 304. DOI: https://doi.org/10.1186/s12935-024-03479-y
XEM THÊM
- Cải biến di truyền giúp tăng cường hiệu quả liệu pháp tế bào miễn dịch trong điều trị ung thư: TCR-T và CAR-T https://www.facebook.com/share/p/18mRyiUvJb/
- Liệu pháp CAR-T – bước đột phá của liệu pháp tế bào trong điều trị ung thư https://www.facebook.com/share/p/1ACHF2K2wY/
- Một số giải pháp giảm chi phí cho liệu pháp CAR-T trong điều trị ung thư https://www.facebook.com/share/p/1AAvzahvNA/
- Liệu pháp CAR-T đồng loại cho thấy tính an toàn và hiệu quả trong điều trị ung thư huyết học https://www.facebook.com/share/p/1APRfhAno5/
- Liệu pháp CAR-T đồng loại: giải pháp giúp bệnh nhân ung thư tăng khả năng tiếp cận phương pháp điều trị tiên tiến https://www.facebook.com/share/p/1AHFJQ6Wue/