TẾ BÀO HỌC
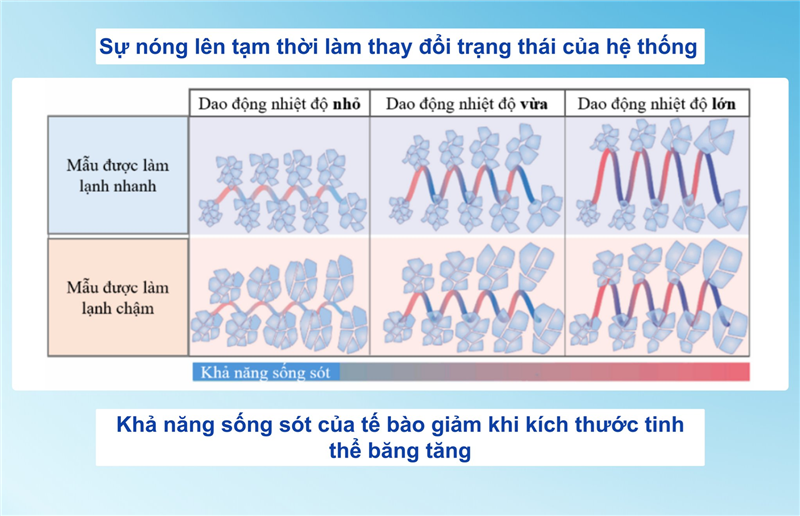
Sự cố nóng lên tạm thời trong bảo quản mẫu đông lạnh
Sự cố nóng lên tạm thời xảy ra khi mẫu được bảo quản lạnh bị tiếp xúc với nhiệt độ cao vượt mức kiểm soát trong khoảng thời gian ngắn. Mặc dù có vẻ không đáng kể, nhưng ngay cả việc tăng nhiệt độ nhỏ cũng có thể khởi động một chuỗi phản ứng sinh học bên trong tế bào.
09/03/2026
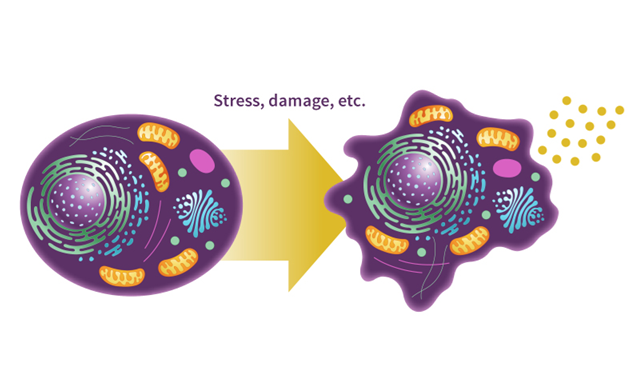
Các dấu hiệu đặc trưng cho sự lão hóa của tế bào gốc soma
Mặc dù tế bào gốc nhìn chung được bảo vệ khỏi một số cơ chế lão hóa so với các tế bào đã biệt hóa, tuy nhiên chúng vẫn dễ bị tổn thương bởi nhiều tác nhân gây căng thẳng (stress).
02/02/2026
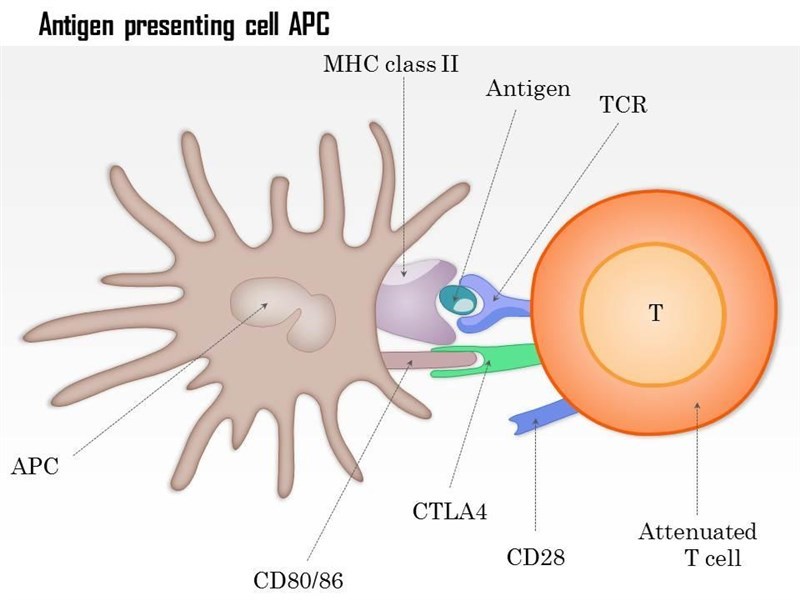
Tế bào trình diện kháng nguyên và sự kích hoạt miễn dịch
Tế bào trình diện kháng nguyên (APC) là những tế bào biểu hiện kháng nguyên lạ đã liên kết với MHC trên bề mặt của nó, nhờ đó tế bào T có thể nhận diện phức hợp này bằng cách thông qua thụ thể tế bào T (TCR).
25/01/2026
Vai trò của tương tác giữa đại thực bào liên quan đến khối u và nguyên bào sợi liên quan đến ung thư trong môi trường vi mô của sarcoma mô mềm
Sarcoma là một loại ung thư hiếm gặp phát triển từ các mô liên kết của cơ thể như xương, cơ, mỡ, dây thần kinh, mạch máu,… Sarcoma mô mềm (soft tissue sarcoma – STS) phát triển ở cơ, mỡ, gân, dây chằng, mô xơ, mạch máu, chiếm khoảng 80% các trường hợp sarcoma, là loại ung thư nguy hiểm, với tỷ lệ sống thêm 5 năm chỉ khoảng 15% nếu đã di căn và khoảng 81% nếu chưa lan rộng. Trong STS, vi môi trường khối u (tumor microenvironment – TME) không chỉ hoạt động như một chất nền tăng trưởng cho tế bào ung thư mà còn là một yếu tố quan trọng ảnh hưởng đến hành vi của khối u và đáp ứng điều trị. TME chứa hai thành phần tế bào trung tâm là đại thực bào liên quan đến khối u (tumor-associated macrophage – TAM) và nguyên bào sợi liên quan đến ung thư (cancer-associated fibroblast – CAF), sự tương tác giữa các tế bào và các phân tử tín hiệu giúp điều chỉnh sự tăng sinh, xâm lấn và di căn của khối u. CAF giải phóng nhiều phân tử tín hiệu như IL-6, TGF-β, PDGF, HIF-1α và SPP1, kích hoạt và thu hút TAM, đồng thời thúc đẩy sự phân cực của chúng về phía kiểu hình M2, được biết đến với hoạt động tiền ung thư. Các cytokine này kích thích sự hình thành mạch máu bất thường, tái cấu trúc chất nền ngoại bào (extracellular matrix – ECM) và cơ chế thoát miễn dịch. Đồng thời, TAM tiết ra IL-34, CSF1R, VEGF và MMP, giúp tăng cường hoạt hóa CAF và thúc đẩy sự tăng sinh và di cư của tế bào khối u. Tương tác hai chiều này tạo ra một vòng lặp: TAM kích hoạt CAF thông qua các yếu tố như SPP1, MMP2/9 và EGF, tăng cường khả năng tái cấu trúc ECM và hỗ trợ khối u xâm lấn của CAF. Ngược lại, CAF tiết ra các chất hoạt hóa PDGF và IL-6/STAT3, thúc đẩy sự tuyển dụng, sự sống sót và sự phân cực của TAM. Hơn nữa, trục này ức chế các phản ứng miễn dịch chống khối u: CAF sản xuất axit lactic và TGF-β, ức chế sự tăng sinh tế bào T, trong khi TAM biểu hiện PD-L1, ngăn chặn hoạt động của tế bào T thông qua con đường PD-1/PD-L1. Nhìn chung, mạng lưới kết hợp TAM-CAF tổ chức lại vi môi trường khối u theo hướng ủng hộ xơ hóa, ức chế miễn dịch và ủng hộ sinh mạch, tăng cường sự tăng sinh, di cư và trốn tránh miễn dịch của tế bào khối u trong các khối u mô mềm. TÀI LIỆU THAM KHẢO Zhou J., et al. (2025). The prognostic role of tumor-associated macrophage and cancer-associated fibroblast interactions in soft tissue sarcoma microenvironments. iScience 28(11): 113851. DOI: https://doi.org/10.1016/j.isci.2025.113851
24/01/2026
Atlas mới về tế bào miễn dịch giúp chẩn đoán và điều trị cá nhân hóa cho người châu Á
Các nhà khoa học từ Singapore, Hàn Quốc, Nhật Bản, Thái Lan và Ấn Độ đã cùng tham gia một nghiên cứu để tạo ra bản đồ đa dạng miễn dịch châu Á (Asian Immune Diversity Atlas – AIDA), phân tích toàn diện về các tế bào miễn dịch từ nhiều quần thể người châu Á khác nhau. Sự đa dạng sinh học của con người chịu ảnh hưởng của các yếu tố như tuổi tác, giới tính và nguồn gốc di truyền, tác động đáng kể đến kết quả sức khỏe, khiến cho những bản đồ tham chiếu theo từng nhóm dân số trở nên cần thiết để có những hiểu biết lâm sàng chính xác. Bản đồ này có thể hỗ trợ những chẩn đoán chính xác hơn và mang lại phương pháp điều trị cá thể hóa cho người châu Á, đồng thời giải quyết được một vấn đề quan trọng trong nghiên cứu hệ gen toàn cầu, vốn trước đây chủ yếu tập trung vào các nhóm dân số châu Âu. Các nhà khoa học đã phân tích hơn 1,2 triệu tế bào miễn dịch từ 625 người hiện khỏe mạnh, đồng thời đánh giá các yếu tố về dân tộc, độ tuổi, giới tính ảnh hưởng đến tỷ lệ tế bào miễn dịch và sự biểu hiện gen. Kết quả cho thấy tuổi tác và giới tính ảnh hưởng đến các tế bào miễn dịch khác nhau giữa các nhóm dân tộc châu Á. Trong một số trường hợp, các loại tế bào và biểu hiện gen được phát hiện phổ biến hơn 2-8 lần ở một số quần thể nhất định. Sự khác biệt đó có thể giúp cải thiện chẩn đoán bệnh và đánh giá rủi ro sức khỏe, giải thích tại sao một số người có khả năng mắc một số bệnh truyền nhiễm hoặc tự miễn cao hơn người khác. Ví dụ: người Thái Lan có tỷ lệ tế bào đơn nhân thấp hơn, cho thấy cần phải xem xét yếu tố dân tốc khi cân nhắc hiến mẫu; người Hàn Quốc có tỷ lệ tế bào T điều hòa thấp hơn, liên quan đến nguy cơ mắc các bệnh tự miễn cao hơn; người Singapore gốc Ấn có gen FCER1A hoạt động mạnh hơn người gốc Hoa, dẫn đến phản ứng miễn dịch có sự khác biệt; ngoài ra cũng tìm thấy mối liên hệ giữa các biến thể di truyền liên quan đến bệnh ở quần thể người Nhật Bản và các loại tế bào miễn dịch cụ thể, chẳng hạn biến thể liên quan đến viêm khớp dạng thấp với gen HIF1A. Những phát hiện này cho thấy việc kết hợp hồ sơ miễn dịch với dữ liệu di truyền có thể mở đường cho việc chẩn đoán và điều trị chính xác hơn theo từng nhóm dân số ở châu Á. Các bác sỹ có thể sử dụng AIDA để xây dựng xét nghiệm máu thế hệ mới nhằm chẩn đoán nhiều loại bệnh khác nhau. TÀI LIỆU THAM KHẢO Kock K.H., et al. (2025). Asian diversity in human immune cells. Cell, 188(8), 2288-2306. DOI: https://doi.org/10.1016/j.cell.2025.02.017
24/01/2026

Nghiên cứu tế bào gốc năm 2026: những lợi ích, hạn chế và ứng dụng chính
Tế bào gốc (stem cells) là những tế bào chưa phân hóa hoặc phân hóa một phần, có thể biến đổi thành nhiều loại tế bào khác nhau để thực hiện chức năng trong cơ thể. Tế bào gốc được kích hoạt quá trình biệt hóa tạo nên các tế bào chuyên hóa khi các mô/cơ quan trong cơ thể cần được bổ sung tế bào hoặc sửa chữa/tái tạo.
23/01/2026
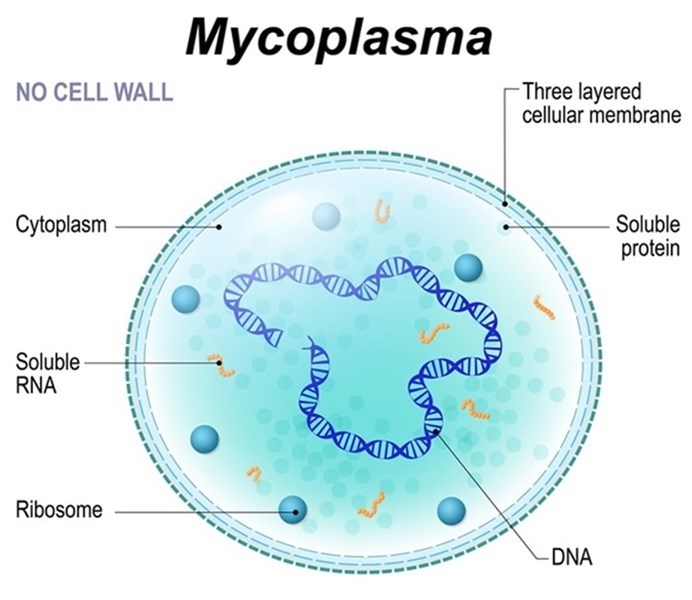
Nhiễm Mycoplasma trong nuôi cấy tế bào
1. Mycoplasma là gì? Tên gọi chung Mycoplasma thực ra để chỉ các loài trong lớp Mollicutes (với các chi Mycoplasma, Acholeplasma, Spiroplasma, Anaeroplasma và Ureaplasma). Đây là loại vi khuẩn tự sao chép nhỏ nhất (0,15-0,3 micromet) và đơn giản nhất, nhưng hoàn toàn không có thành tế bào (peptidoglycan) như các vi khuẩn điển hình nên kháng hầu hết các loại kháng sinh. Mollicutes có bộ gen rất nhỏ (0,58-2,20 Mb, so với E. coli là 4,64 Mb) nên chúng trao đổi chất rất hạn chế, chỉ vừa đủ để sao chép và tồn tại. Vì vậy, hầu hết các loài trong lớp Mollicutes đều sống ký sinh, nổi bật là bám dính, xâm nhập hoặc hợp nhất với tế bào chủ. 2. Nhiễm Mycoplasma – vấn đề nghiêm trọng trong nuôi cấy tế bào Nhiễm Mycoplasma thường gặp trong nuôi cấy tế bào, làm tế bào sinh trưởng chậm, ảnh hưởng đến các quá trình trao đổi chất và biểu hiện gen, gây chuyển dạng tế bào, từ đó làm thay đổi kết quả của các nghiên cứu/thử nghiệm, thậm chí đe dọa đến sự an toàn của người sử dụng đối với sản phẩm dùng trong y học. Nhiễm Mollicutes thường khó phát hiện vì môi trường nuôi cấy không biểu hiện đục hay thay đổi pH, tế bào cũng không bị ảnh hưởng rõ rệt, do đó thường bị bỏ sót. Nhiễm mycoplasma trong phòng nuôi cấy do nhiều nguyên nhân khác nhau, chủ yếu là nhiễm chéo từ các dòng tế bào nuôi cấy liên tục. Mycoplasma có thể lây lan qua các thiết bị, vật tư, hóa chất trong quá trình làm việc. Đặc biệt, các hóa chất có nguồn gốc động vật là nguồn lây mycoplasma cần được xem xét nghiêm túc, ví dụ các loài Mollicutes ký sinh trên bò được phát hiện ở huyết thanh thai bò (FBS), trong đó A. laidlawii và M. arginini được phát hiện thường xuyên nhất. Các nghiên cứu cho thấy tỷ lệ các dòng tế bào liên tục bị nhiễm mycoplasma tới 15-80%, trong khi tế bào nuôi cấy sơ cấp hiếm khi phát hiện. Trong số ít nhất 20 loài Mollicutes được biết là gây nhiễm trong nuôi cấy tế bào, 5 loài phổ biến nhất (Mycoplasma arginini, M. fermentans, M. hyorhinis, M. orale và Acholeplasma laidlawii) chiếm khoảng 95% các trường hợp, trong khi M. pneumoniae, M. hominis, M. genitalium, Ureaplasma parvum và U. urealyticum thường được tìm thấy nhất trong các mẫu lâm sàng. Cơ quan Dược phẩm châu Âu (EMA), Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) đều yêu cầu xét nghiệm Mycoplasma đối với các sản phẩm từ tế bào dự kiến được sử dụng trong lâm sàng. 3. Các cơ chế tương tác với tế bào chủ Bám dính: Hầu hết Mollicutes là vi sinh vật ngoại bào có khả năng bám dính vào bề mặt của tế bào chủ, sự bám dính là bước đầu tiên và thiết yếu trong quá trình xâm chiếm vật chủ. Xâm nhập: Một số Mollicutes phát triển các cơ chế xâm nhập vào trong tế bào, giúp chúng tránh được những tác động bất lợi ngoại bào, ví dụ kháng sinh. Điển hình trong số này là M. penetrans và M. fermentans. Chúng tồn tại lâu dài và nhân lên bên trong tế bào chủ, có thể được giải phóng qua quá trình xuất bào. Hợp nhất: Trong một số trường hợp hiếm gặp, Mollicutes có thể hợp nhất với tế bào chủ, chẳng hạn M. fermentans hợp nhất được với nhiều loại tế bào người. Sau đó, các thành phần của chúng có thể được đưa vào và ảnh hưởng đến các chức năng bình thường trong tế bào, ví dụ nuclease của mycoplasma phá hủy DNA của tế bào chủ. 4. Những tác động của mycoplasma đối với tế bào Cạnh tranh tiền chất: Mycoplasma có bộ gen rất nhỏ, hầu hết các loài đều không có các gen sinh tổng hợp axit amin, axit béo, cofactor, vitamin, do đó chúng lấy các tiền chất này từ vật chủ để phục vụ hoạt động trao đổi chất của chúng. Vì thế, các tế bào chủ bị mất tính toàn vẹn, thay đổi hoạt động sống và chức năng, đi vào sự chết theo chương trình (apoptosis). Gây độc cho tế bào: Mycoplasma giải phóng các chất chuyển hóa để phân hủy các thành phần của tế bào để lấy nguyên liệu (ví dụ phân giải DNA để lấy nucleotide), tiết ra các sản phẩm phụ gây độc tế bào, ảnh hưởng đến sự sinh trưởng và sức sống của tế bào chủ. Thay đổi chức năng, gây biệt hóa: Mycoplasma hoạt hóa các đại thực bào giải phóng những yếu tố tiền viêm, thúc đẩy sự trưởng thành của tế bào lympho, exosome của tế bào tua (DC) bị nhiễm mycoplasma kích thích tế bào B non phân chia và tiết immunoglobin,… Chuyển dạng tế bào: Tương tác kéo dài với mycoplasma làm tế bào có thể mất ổn định nhiễm sắc thể, gia tăng hoặc giảm biểu hiện của nhiều gen – nhất là các gen liên quan đến ung thư, từ đó tế bào có thể chuyển sang dạng ác tính. Thay đổi con đường truyền tin tế bào: Các chất tiết ra từ mycoplasma có thể tương tác với các thụ thể để kích hoạt hoặc ức chế các con đường truyền tin tế bào, kích hoạt các yếu tố phiên mã NF-B và AP-1. Các gen đích bị ảnh hưởng chủ yếu chịu trách nhiệm cho các protein tiền viêm, chuyển dạng tế bào sang ác tính, ít khi tác động đến các gen mã hóa protein khác. Ảnh hưởng đến sản phẩm: Mycoplasma có thể làm thay đổi sự thâm nhiễm của virus, hoạt động tương tự virus, nên có thể làm giảm hoặc tăng sản lượng virus, ảnh hưởng đến việc sử dụng tế bào nuôi cấy để sản xuất virus và dạng giống virus (dùng làm vaccine). Mycoplasma có khả năng gây bệnh ở người (phổ biến nhất là viêm phổi) nên đe dọa sự an toàn của các sản phẩm liệu pháp tế bào. --------- TÀI LIỆU THAM KHẢO 1. United States Food and Drug Administration (FDA). 2020. Chemistry, Manufacturing, and Control (CMC) Information for Human Gene Therapy Investigational New Drug Applications (INDs), 2020. 2. European Medicines Agency (EMA). (2019). Draft Guideline on quality, non-clinical and clinical requirements for investigational advanced therapy medicinal products in clinical trials. 3. AABB (2009). Cellular Therapy : Principles, Methods, and Regulations. 1st Edition, edition E.M. Areman and K. Loper. 4. Rottem S., Kosower N. S., and Kornspan J. D. (2012). Contamination of tissue cultures by mycoplasmas. In Biomedical Tissue Culture. IntechOpen. 5. Angart P., Kohnhorst C., Chiang M., Arden N. S. (2018) Considerations for risk and control of Mycoplasma in bioprocessing. Current Opinion in Chemical Engineering; 22: 161-166. Xem thêm: Xét nghiệm Mycoplasma trong nuôi cấy tế bào https://www.facebook.com/share/p/1FMPF7iXFT/?mibextid=WC7FNe
23/01/2026
Tạp nhiễm trong quá trình nuôi cấy
Những điều kiện mà tế bào phát triển mạnh khi nuôi cấy in vitro (môi trường giàu dinh dưỡng, oxy, độ ẩm, pH,…) cũng là những điều kiện lý tưởng để các tác nhân tạp nhiễm phát triển mạnh. Trong cơ thể sống, chúng ta có hệ miễn dịch bảo vệ cho tác tế bào và cơ thể tránh sự tạp nhiễm của vi sinh vật (hay chính xác hơn là duy trì sự cân bằng giữa tế bào của cơ thể và vi sinh vật), nhưng với điều kiện nuôi cấy trong phòng thí nghiệm, các tác nhân đó nhanh chóng gây nên những ảnh hưởng nghiêm trọng: tăng tỷ lệ tế bào chết, làm tế bào chậm phát triển, thay đổi hình thái, thay đổi trao đổi chất và biểu hiện gen, đe dọa độ an toàn của sản phẩm tế bào, thay đổi các kết quả thử nghiệm,…
23/01/2026
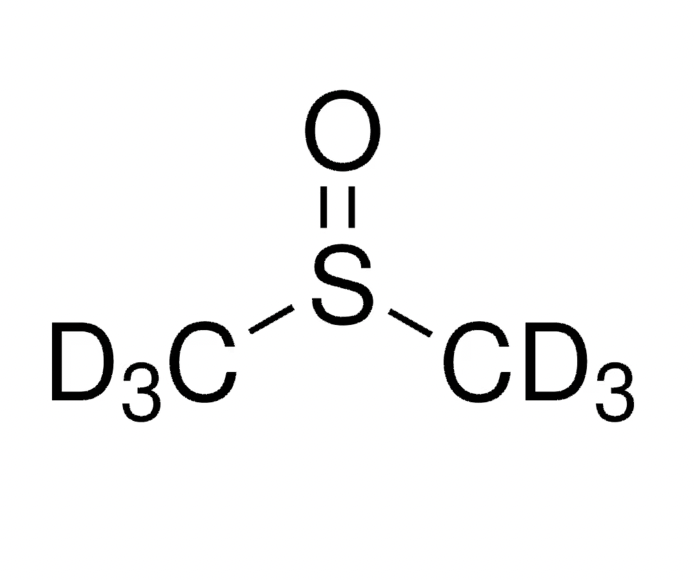
Những biến đổi vật lý xảy ra trong quá trình hạ lạnh tế bào T khi có dimethyl sulfoxide
Qua đây, chúng ta có thể hiểu vai trò của quá trình hạ lạnh, khả năng lưu trữ tế bào ở nhiệt độ -80*C và dưới -150*C (nitơ pha lỏng hoặc pha hơi), cũng như những ảnh hưởng khi tế bào đông lạnh không được đảm bảo nhiệt độ lưu trữ.
23/01/2026
Rã đông tế bào sau quá trình bảo quản đông lạnh
(Những sản phẩm thương mại như thiết bị, dụng cụ, hóa chất sinh phẩm xuất hiện trong bài viết mang tính chất tham khảo và chia sẻ kinh nghiệm thực tế, không nhằm mục đích quảng cáo) --------- Quy trình rã đông tế bào (Hình 1): - Lấy tế bào từ hệ thống lưu trữ (hệ thống nitơ -196*C hoặc tủ lạnh âm sâu -80*C), nhanh chóng rã đông mẫu. Trường hợp thời gian chờ rã đông lâu, cần bảo quản mẫu trong thiết bị vận chuyển sử dụng nitơ (-196*C) hoặc đá khô (-80*C) để mẫu tránh bị gia nhiệt tự nhiên. - Đặt mẫu vào bể ổn nhiệt 37*C (nắp ống cao hơn mực nước để tránh nhiễm khuẩn), lắc đều để băng nhanh tan (thời gian <1 phút) cho đến khi chỉ còn một mẩu đá nhỏ đang tan trong dung dịch (nhiệt độ mẫu ~0*C) - Nhanh chóng chuyển mẫu sang ống ly tâm chứa sẵn môi trường nuôi cấy đã làm ấm (nhiệt độ phòng hoặc 37*C), thể tích môi trường sử dụng gấp khoảng 10 lần so với thể tích mẫu đông lạnh - Ly tâm thu tế bào và thực hiện các thí nghiệm tiếp theo Hình 1. Các bước cơ bản của quá trình rã đông tế bào --------- Một số lưu ý để thực hiện tốt quá trình rã đông tế bào (Hình 2) - Quá trình rã đông cần thực hiện nhanh để tế bào tránh bị ảnh hưởng bởi các tinh thể băng trong lúc băng tan. Cần rã đông ở nhiệt độ 37*C thay vì nhiệt độ phòng hay nhiệt độ lạnh. - Ngay khi mẫu tan băng, cần nhanh chóng chuyển tế bào vào môi trường nuôi cấy để pha loãng dung dịch bảo quản, do DMSO là chất độc với tế bào ở nhiệt độ phòng. Nên sử dụng môi trường nuôi cấy để tế bào quen với môi trường trong quá trình nuôi cấy sau này, tránh tiếp xúc với nhiều dung môi khác nhau ảnh hưởng đến áp suất thẩm thấu - Tế bào sau rã đông khá yếu và nhạy cảm, hạn chế tác động mạnh đến tế bào: hạn chế pipeting, tránh hút tế bào bằng micropipet (lực hút mạnh) mà nên sử dụng pipet Pasteur, ly tâm tốc độ thấp,… Hình 2. Một số lưu ý để thực hiện tốt quá trình rã đông tế bào --------- Nhìn chung quá trình lưu trữ và rã đông tế bào để đạt hiệu quả tốt cần sự kết hợp của nhiều yếu tố: - Thao tác thực hiện hạ lạnh và rã đông, đặc biệt chú ý những lưu ý thực hành tốt - Hạ lạnh chậm 1*C/phút thường được áp dụng, với sự hỗ trợ của thiết bị hạ lạnh (VD: CryoMed™ Controlled-Rate Freezer của ThermoFisher Scientific), hoặc dụng cụ hạ lạnh mini (VD: Cell Freezing Container của Corning hoặc Biocision/ azenta) - Khả năng bảo vệ tế bào của môi trường bảo quản đông lạnh, VD: thực nghiệm cho thấy môi trường thương mại CryoStor CS10 (StemCell Technologies) có khả năng duy trì tỷ lệ tế bào sống hàng giờ ở nhiệt độ phòng, môi trường đông lạnh chứa hàm lượng huyết thanh càng cao giúp tỷ lệ tế bào chết càng thấp - Hệ thống lưu trữ được duy trì ổn định, không có sự biến động lớn về nhiệt độ --------- Hình 3. So sánh tỷ lệ tế bào sống của một mẫu tế bào gốc trung mô (tách từ wharton's jelly dây rốn, nuôi cấy trong môi trường StemMACS™ Expansion Media Kit XF – Miltenyi) ở các thời điểm: (a) trước lưu trữ: trước khi tiếp xúc môi trường bảo quản và hạ lạnh; (b) sau khi rã đông: bảo quản trong môi trường CryoStor® CS10 (StemCell Technologies), hạ lạnh bằng Coolcell® Container (Corning), lưu trữ trong tủ lạnh âm sâu -80*C trong 2 tháng và rã đông. Kết quả được đo bằng hệ thống Countess™ 3 Automated Cell Counter (ThermoFisher Scientific). Một số tiêu chí đánh giá chất lượng tế bào sau lưu trữ và rã đông: - Tỷ lệ tế bào sống - Khả năng duy trì đặc tính tế bào như tốc độ sinh trưởng, khả năng biệt hóa (với tế bào gốc), sự biểu hiện các marker bề mặt, các cytokine,… - Độ ổn định di truyền
23/01/2026

Bảo quản đông lạnh tế bào
1. Vai trò của bảo quản lạnh tế bào - Tạo nguồn dự trữ khi cần - Gián đoạn tạm thời quá trình sinh trưởng của tế bào, giúp tiết kiệm chi phí nuôi cấy tế bào khi chưa có nhu cầu cần thiết phải nuôi cấy - Bảo tồn các dòng tế bào với tuổi thọ hữu hạn hoặc hạn chế biến đổi trong quá trình nuôi cấy - Lưu trữ một loại tế bào ở một giai đoạn nhất định để đảm bảo tính đồng nhất trong nghiên cứu/thử nghiệm Hình 1. Các bước tiến hành thu hoạch và lưu trữ tế bào nuôi cấy bám dính 2. Các sự kiện chính trong quá trình hạ lạnh tế bào Trong quá trình đông lạnh, các tinh thể đá hình thành cả bên trong và bên ngoài tế bào, phần ngoại bào đông lạnh trước làm tăng nồng độ các chất điện giải bên trong tế bào, làm thay đổi áp suất thẩm thấu, gây mất nước của tế bào. Quá trình này có thể làm giảm sức sống của tế bào. Các sự kiện chính trong quá trình hạ lạnh tế bào được thể hiện trong Hình 2. Hình 2. Các sự kiện chính diễn ra trong quá trình hạ lạnh tế bào 3. Môi trường bảo quản lạnh tế bào - Thường chứa DMSO, hoặc glycerol, propylene glycol, trehalose,... (khoảng 10% v/v) để làm hạ thấp điểm đóng băng và ổn định áp suất thẩm thấu của tế bào trong quá trình hạ lạnh - Chứa huyết thanh (nếu môi trường nuôi cấy có huyết thanh), hoặc cell culture–grade BSA, hay albumin huyết thanh (nồng độ càng cao càng giúp giảm tỷ lệ tế bào chết trong quá trình bảo quản) Một số môi trường đông lạnh thương mại được sử dụng phổ biến như CryoStor CS10 Cell Freezing Medium (Stemcell Technologies), Recovery Cell Culture Freezing Medium và Synth-a-Freeze Cryopreservation Medium (ThermoFisher Scientific), NutriFreez® D10 Cryopreservation Medium (Sartorius),… - Một số nhóm nghiên cứu đang phát triển các vật liệu polymer để đông lạnh tế bào được cho là có độ phù hợp cao hơn với tế bào nuôi cấy 3D 4. Phương pháp hạ lạnh - Hạ lạnh chậm: thường sử dụng nhất, tốc độ hạ lạnh 1*C/phút. Thiết bị hỗ trợ có thể sử dụng như hệ thống hạ lạnh theo chương trình (VD: CryoMed™ Controlled-Rate Freezer của ThermoFisher Scientific), hoặc dụng cụ hạ lạnh mini (VD: Cell Freezing Container của Corning hoặc Biocision/ azenta) với chất liệu xốp đặc biệt hoặc sử dụng isopropanol. Thường tế bào bắt đầu hạ lạnh đều đặn 1*C/phút từ 4*C đến -80*C trước khi cho vào hệ thống lưu trữ. - Hạ lạnh nhanh: tốc độ hạ lạnh có thể lên đến 120*C/phút - Thủy tinh hóa: chuyển thẳng mẫu vào nitơ lỏng (-196*C), tạo nên các tinh thể như sợi thủy tinh Hình 3. Sự thay đổi nhiệt độ của một mẫu hạ lạnh bằng hệ thống tự động CryoMed™ Controlled-Rate Freezer (ThermoFisher Scientific). Trục tung: nhiệt độ (oC), trục hoành: thời gian (phút). Đường màu xanh: nhiệt độ buồng chứa mẫu, đường màu đỏ: nhiệt độ mẫu. 5. Một số lưu ý khi bảo quản đông lạnh tế bào - Nên bảo quản tế bào khi chúng đang ở pha sinh trưởng (pha log), có sức sống tốt nhất - Môi trường bảo quản nên được pha vào ngày bảo quản, trước khi bảo quản tế bào ít nhất 30 phút (để kịp làm lạnh), hoặc có thể sử dụng môi trường thương mại. Nên làm lạnh đến 2-8*C trước khi sử dụng. - Nồng độ tế bào bảo quản dao động từ 0,5-10 triệu tế bào/mL tùy từng loại tế bào, - Thể tích dung dịch bảo quản thường khuyến cáo bằng khoảng 1/2 thể tích tối đa của ống lưu trữ (VD: 1 mL dung dịch cho ống 2 mL, 2-3 mL dung dịch cho ống 5 mL) - Trường hợp không có thiết bị/dụng cụ hạ lạnh có thể sử dụng các tủ lạnh: chuyển tế bào trong dung dịch bảo quản vào tủ mát 2-8*C trong 15-30 phút (nếu trước đó chưa làm lạnh dung dịch bảo quản), chuyển sang tủ -20*C trong 1-2 giờ, sau đó chuyển sang tủ -80*C trong tối thiểu 4 giờ - Có thể lưu trữ tế bào ngắn hạn trong điều kiện -80*C (dưới 6 tháng, hoặc tối đa 12 tháng), nếu lưu trữ lâu dài cần bảo quản trong nitơ lỏng (-196*C). Bảo quản tế bào lâu dài ở điều kiện -80*C làm tế bào giảm sức sống và có thể diễn ra những biến đổi không mong muốn. TÀI LIỆU THAM KHẢO - Jang T. H., et al. (2017). Cryopreservation and its clinical applications. Integrative medicine research, 6(1), 12-18. - Deliorman M., et al. (2020). A Method to Efficiently Cryopreserve Mammalian Cells on Paper Platforms. Bio-protocol, 10(18), e3764-e3764. - ThermoFisher Scientific, Cryopreservation of Mammalian Cells (https://www.thermofisher.com/vn/en/home/references/gibco-cell-culture-basics/cell-culture-protocols/freezing-cells.html)
22/01/2026

Thành phần môi trường nuôi cấy: kháng sinh và kháng nấm – bạn hay thù?
Theo quan điểm hiện nay, không nên sử dụng kháng sinh trong nuôi cấy tế bào vì những tác động xấu của nó làm thay đổi đặc tính của tế bào. Các công cụ hiện đại như cơ sở vật chất, trang thiết bị, nguyên tắc thực hành và kỹ thuật vô trùng khiến những hợp chất này trở nên không cần thiết.
22/01/2026