LIỆU PHÁP TẾ BÀO
Thuật ngữ liệu pháp tế bào (cell therapy) dùng để chỉ việc chuyển vật liệu tế bào vào bệnh nhân cho mục đích điều trị. Liệu pháp tế bào bao gồm nhiều lĩnh vực điều trị như liệu pháp tế bào gốc, liệu pháp tế bào miễn dịch, liệu pháp tế bào cải biến gen,...

Liệu pháp tế bào gốc trung mô (MSC) giúp giảm nguy cơ suy tim sau nhồi máu cơ tim
Thử nghiệm lâm sàng PREVENT-TAHA8 cho thấy những kết quả đáng ngạc nhiên về tiềm năng giảm nguy cơ suy tim sau nhồi máu cơ tim của MSC
23/01/2026
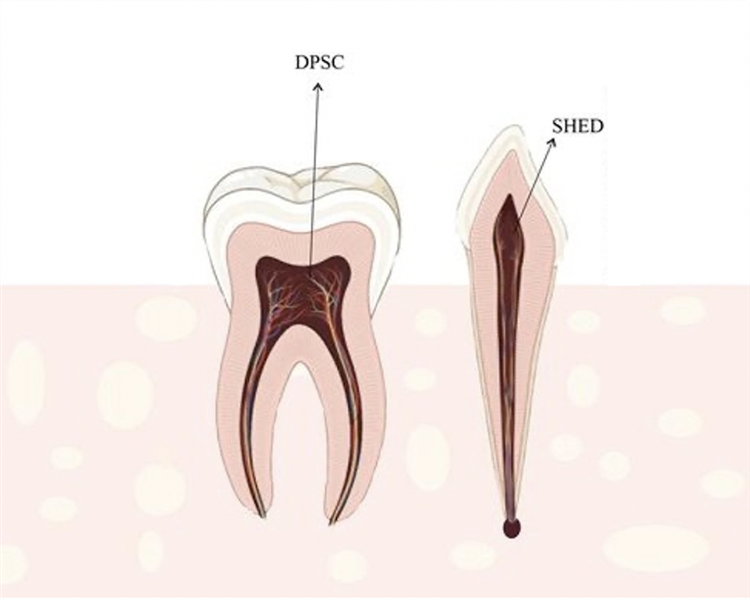
Tính đa tiềm năng và điều hòa miễn dịch của tế bào gốc tủy răng sữa
1. Tế bào gốc tủy răng sữa Tế bào gốc từ tủy răng sữa (Stem cells from human exfoliated deciduous teeth – SHED) được coi là quần thể tế bào đầy hứa hẹn cho liệu pháp tế bào và kỹ thuật mô. Đây là những tế bào gốc còn non, có khả năng tăng sinh và hình thành các loại tế bào chuyên hóa tốt hơn so với tế bào gốc từ người trưởng thành. SHED nhận được sự quan tâm lớn của các nhà nghiên cứu, nhờ quá trình thu thập mẫu răng không xâm lấn mà chỉ tận dụng rác thải sinh học của quá trình thay răng tự nhiên, đồng thời tăng sinh mạnh, biệt hóa thành nhiều loại tế bào khác nhau và có khả năng điều hòa miễn dịch. 2. Tính đa tiềm năng của tế bào gốc tủy răng sữa SHED mang các đặc điểm của tế bào gốc trung mô (Mesenchymal stem cell – MSC), nên có khả năng biệt hóa thành các loại tế bào của mô liên kết như xương, sụn, mỡ, cơ,… SHED đã được chứng minh là có khả năng biệt hóa xương cao hơn so với MSC từ các nguồn khác như mô mỡ, dây rốn, tủy xương,... Nhờ đặc tính này, SHED đã và đang được thử nghiệm nhiều trong các nghiên cứu về tái tạo xương và răng. Ví dụ, nhóm nhà khoa học Lee và cộng sự (Hàn Quốc) đã sản xuất các tấm tế bào từ SHED để ghép vào bên trong các trường hợp khe hở vòm miệng giúp tái tạo xương. Prahasanti và cộng sự cũng đã sử dụng vật liệu carbonate apatit để kết hợp với SHED thúc đẩy quá trình tái tạo xương. SHED và các tế bào gốc nha khoa khác có nguồn gốc từ tế bào mào thần kinh (Neural crest cells), nên có khả năng biệt hóa thần kinh cao hơn so với MSC từ các nguồn khác, tạo nên nguồn nguyên liệu đầy hứa hẹn cho các rối loạn thần kinh như chấn thương tủy sống, Parkinson, Alzheimer,… SHED có thể hình thành các quả cầu giống thần kinh, khi cấy vào thể vân của chuột mắc bệnh Parkinson đã cải thiện các rối loạn hành vi, bảo vệ các tế bào sản xuất dopamine và một số loại tế bào thần kinh khác trong cơ thể chuột. Bằng cách cảm ứng với nhiều chất khác nhau, các nhà khoa học đã biệt hóa in vitro được SHED thành tế bào giống thần kinh hoạch xoắn ốc, tế bào thần kinh ngoại biên, tế bào thần kinh đệm hình sao (astrocyte),… SHED cũng được sử dụng trong tái tạo nhiều loại mô khác. Yếu tố tăng trưởng nội mô mạch máu (Vascular endothelial growth factor) có thể kích thích SHED biệt hóa nội mô – sinh mạch, thúc đẩy quá trình tái tạo mạch máu. SHED cũng có thể biệt hóa thành tế bào gan, tế bào ống đường mật, tế bào beta tiết insulin, tế bào thụ cảm ánh sáng võng mạc. 3. Khả năng điều hòa miễn dịch SHED và các tế bào gốc nha khoa khác có thể tương tác với vi môi trường viêm để điều hòa miễn dịch tại chỗ. Nhiều nghiên cứu cho thấy môi trường điều kiện hóa không huyết thanh của SHED (serum-free conditioned media of SHED, SHED-CM) hoặc các thể tiết ngoại bào (extracellular vesicle, EV) có chức năng điều hòa các tế bào hoặc mô khác, cho thấy liệu pháp không sử dụng trực tiếp tế bào là một chiến lược hiệu quả trong y học tái tạo. Nhiều nghiên cứu đã sử dụng SHED-CM để điều trị thoái hóa khớp, viêm võng mạc sắc tố, Parkinson, tái tạo xương, … SHED-EV được thử nghiệm trong điều trị viêm nha chu, lupus ban đỏ hệ thống, chống viêm sụn khớp thái dương hàm,… Với tác dụng điều biến các tế bào miễn dịch, SHED, SHED-CM và SHED-EV đã có tác dụng tích cực với nhiều bệnh toàn thân như Alzheimer, suy gan cấp, xơ gan, tổn thương thận cấp, trẻ hóa da,… Như vậy, nhờ việc được thu từ nguồn mô không xâm lấn và khả năng tinh mạnh mẽ, SHED đang trở thành một nguồn nguyên liệu đầy hứa hẹn cho liệu pháp tế bào. Đặc tính đa tiềm năng và khả năng điều hòa miễn dịch đã thúc đẩy chúng tham gia nhiều hơn trong các thử nghiệm điều trị bệnh. Liệu pháp tế bào dựa trên SHED có thể sử dụng trực tiếp tế bào, hay sử dụng môi trường cảm ứng (SHED-CM) và thể tiết ngoại bào (SHED-EV), đều mang lại những tín hiệu đầy hứa hẹn. Tuy nhiên, các cơ chế hoạt động của quá trình biệt hóa cần được nghiên cứu sâu hơn để có thể đưa liệu pháp dựa trên SHED trở thành hiện thực lâm sàng. TÀI LIỆU THAM KHẢO 1. Rosa V., et al. (2016). Pluripotency of stem cells from human exfoliated deciduous teeth for tissue engineering. Stem Cells International, 2016(1), 5957806. https://doi.org/10.1155/2016/5957806 2. Guo R., and Yu J. (2022). Multipotency and immunomodulatory benefits of stem cells from human exfoliated deciduous teeth. Frontiers in Dental Medicine, 3, 805875. https://doi.org/10.3389/fdmed.2022.805875
23/01/2026
Lưu trữ tế bào gốc răng sữa: quy trình thực hiện và kiểm soát chất lượng mẫu
1. Lưu trữ tế bào gốc răng sữa Tế bào gốc răng sữa được lấy từ tủy của răng sữa rụng tự nhiên ở trẻ em, có khả năng tự tái tạo và biệt hóa thành nhiều loại tế bào khác nhau trong cơ thể. Tế bào gốc từ răng sữa (Stem Cell from Human Exfoliated Deciduous Teeth – SHED) mang các đặc điểm tương tự tế bào gốc trung mô từ tủy xương, mô mỡ, dây rốn, đồng thời có một số lợi thế như thu thập mẫu không xâm lấn, tốc độ tăng sinh nhanh, khả năng biệt hóa mạnh mẽ, đặc biệt là biệt hóa thần kinh và xương. Vì vậy, việc lưu trữ tế bào gốc tủy răng sữa mang lại hy vọng ứng dụng điều trị các bệnh lý cho tương lai của trẻ. Ngoài răng sữa, các loại tế bào gốc nha khoa khác cũng được quan tâm trong các nghiên cứu, thử nghiệm lâm sàng và lưu trữ như tế bào gốc từ tủy răng trưởng thành (Dental Pulp Stem Cell – DPSC), tế bào gốc dây chằng nha chu (Periodontal Ligament Stem Cell – PDLSC), tế bào gốc nhú đỉnh (Stem Cell from Apical Papilla – SCAP),… Trên thế giới, nhiều ngân hàng đã hoạt động lưu trữ các loại tế bào gốc nha khoa (chủ yếu là SHED và DPSC) như BioEden (Hoa Kỳ), Future Health (Anh), Dentcell (Mexico), Mothercell (Ấn Độ),… Ở Việt Nam, lĩnh vực này cũng được quan tâm trong vài năm trở lại đây, tiêu biểu là Ngân hàng mô thuộc Hệ thống Y tế Vinmec, Ngân hàng mô Fbiomed VN. 2. Quy trình thực hiện 2.1. Thu thập mẫu - Sàng lọc mẫu: Người hiến được thực hiện các xét nghiệm để sàng lọc ban đầu nguy cơ nhiễm khuẩn, nhiễm virus cho mẫu lưu trữ. Đồng thời, các ngân hàng sinh học cũng đưa ra những tiêu chuẩn lựa chọn và tiêu chuẩn loại trừ để đảm bảo chất lượng tốt nhất. - Thu thập mẫu: Người hiến cần được vệ sinh răng miệng, răng sau khi thu thập được đưa ngay vào dung dịch chuyên dụng để đảm bảo tủy được bảo tồn. Nhiều ngân hàng khuyến cáo cần nhổ răng ngay khi mới lung lay, nhiều ngân hàng khác chấp nhận việc để răng rụng tự nhiên. - Vận chuyển mẫu: Dung dịch vận chuyển thường là các loại đệm như PBS hoặc HBSS, cá biệt BioEden và một số ngân hàng khuyến cáo bảo quản mẫu trong sữa bò. Thời gian vận chuyển từ khi nhổ răng đến ngân hàng lưu trữ thường từ một đêm đến 48 giờ. 2.2. Phân lập và nuôi cấy tăng sinh tế bào gốc - Việc phân lập và nuôi cấy tăng sinh tế bào gốc cần được thực hiện trong môi trường phòng sạch và có tủ an toàn sinh học cấp II - Mẫu răng được vệ sinh, tiếp cận mô (tủy răng) và phân lập tế bào gốc, sau đó nuôi cấy tăng sinh để nhân lên số lượng lớn - Quy trình phân lập và nuôi cấy tăng sinh cần đảm bảo “…quá trình xử lý không làm thay đổi các đặc điểm sinh học liên quan của tế bào hoặc mô” 2.3. Kiểm soát chất lượng tế bào gốc - Định danh tế bào: SHED hay DPSC cần thể hiện các đặc điểm cơ bản của tế bào gốc trung mô, bao gồm (i) bám dính trên bề mặt đĩa nuôi cấy nhựa và thể hiện hình thái đặc trưng; (ii) biểu hiện các dấu ấn bề mặt đặc trưng, bao gồm tỷ lệ dương tính CD105, CD73 và CD90 đạt trên 95%, tỷ lệ dương tính CD45, CD34, CD14 hoặc CD11b, CD79α hoặc CD19 và HLA‐DR không quá 2%; (iii) có khả năng biệt hóa ba dòng, gồm dòng tạo xương, tạo mỡ, tạo sụn. - Tỷ lệ tế bào sống: Tỷ lệ ngày trước lưu trữ thường yêu cầu ở mức 80-100% - Độ tinh sạch: Không nhiễm vi khuẩn, vi nấm, mycoplasma, virus - Tính xác thực: Cần đảm bảo loại trừ các yếu tố định danh mẫu sai như nhiễm chéo, thay đổi vị trí hoặc dán nhãn sai, một số đơn vị như Cơ quan Dược phẩm Châu Âu (European Medicines Agency, EMA) yêu cầu xét nghiệm trình tự DNA lặp lại ngắn (Short Tandem Repeat – STR) để đảm bảo định danh mẫu chính xác khi xuất mẫu. - Sự ổn định di truyền: Các mẫu SHED và DPSC cần thời gian nuôi cấy và số lần cấy chuyển tối thiểu để duy trì tính ổn định di truyền, và cần có phương pháp đánh giá thích hợp 2.4. Bảo quản đông lạnh tế bào gốc - Mẫu tế bào gốc được hạ lạnh từ nhiệt độ phòng về nhiệt độ phù hợp (khoảng -80oC đến -90oC) và lưu trữ trong nitơ pha lỏng (-196oC) hoặc pha hơi (<-135oC) -Môi trường bảo quản đông lạnh chứa các chất bảo quản đông lạnh như dimethyl sulfoxide (DMSO), propylene glycerol, polyvinylpyrrolidone,… để ức chế sự phát triển của tinh thể băng, vốn có thể phá vỡ màng tế bào làm tế bào bị vỡ - Một số ngân hàng thực hiện đông lạnh toàn bộ răng hoặc mô răng, nhưng gặp nhiều hạn chế kỹ thuật liên quan khả năng tách tế bào gốc sau rã đông và ứng dụng lâm sàng 2.5. Kiểm soát chất lượng trong quá trình lưu trữ - Để đánh giá chất lượng của ngân hàng sinh học, kiểm soát chất lượng sau khi rã đông phải là một phần của quy trình ngân hàng và phải được thực hiện trên một ống mẫu đông lạnh, vài tháng sau khi bảo quản lạnh - Các tiêu chí kiểm soát chất lượng sau khi rã đông mẫu bao gồm: tỷ lệ tế bào sống, định danh tế bào (hình thái, biểu hiện dấu ấn bề mặt, biệt hóa ba dòng) 3. Chuẩn hóa và chứng nhận ngân hàng tế bào gốc răng sữa - Các ngân hàng cần được kiểm tra, đánh giá và chứng nhận bởi các cơ quan có thẩm quyền trước khi hoạt động, bao gồm các quy trình vận hành dịch vụ, quy trình kỹ thuật, quản lý rủi ro,… - Từng mẫu lưu trữ cần được lập hồ sơ và kiểm soát thông tin, sẵn sàng cung cấp cho các cơ quan có thẩm quyền để kiểm tra, giám sát TÀI LIỆU THAM KHẢO 1. Zeitlin B. D. (2020). Banking on teeth–Stem cells and the dental office. Biomedical journal, 43(2), 124-133. DOI: https://doi.org/10.1016/j.bj.2020.02.003 2. Khaseb S., et al. (2021). Dental stem cell banking: Techniques and protocols. Cell Biology International, 45(9), 1851-1865. DOI: https://doi.org/10.1002/cbin.11626 Xem thêm - Tế bào gốc từ tủy răng sữa (SHED) https://ysinhtebao.com/tbg-trung-mo/te-bao-goc-tu-tuy-rang-sua - Các loại tế bào gốc nha khoa (Dental Stem Cell): nguồn thu nhận và tiềm năng ứng dụng của chúng https://ysinhtebao.com/tbg-trung-mo/cac-loai-te-bao-goc-nha-khoa - Bảo quản đông lạnh tế bào https://ysinhtebao.com/nuoi-cay-tb/bao-quan-dong-lanh-te-bao - Quy định về sàng lọc người hiến mẫu để tạo ra sản phẩm Liệu pháp tế bào tại châu Âu và Hoa Kỳ https://ysinhtebao.com/quy-dinh/quy-dinh-ve-sang-loc-nguoi-hien-mau-de-tao-ra-san-pham-lieu-phap-te-bao-tai-hoa-ky-va-chau-au - ISCT nói gì và quy ước thế nào về tế bào gốc trung mô (MSC) https://ysinhtebao.com/quy-dinh/isct-noi-gi-va-quy-uoc-the-nao-ve-msc - Tạp nhiễm trong quá trình nuôi cấy tế bào https://ysinhtebao.com/nuoi-cay-tb/tap-nhiem-trong-qua-trinh-nuoi-cay, xét nghiệm vi sinh vật https://ysinhtebao.com/qc/xet-nghiem-vi-sinh-vat-trong-nuoi-cay-te-bao-dong-vat và xét nghiệm mycoplasma https://ysinhtebao.com/qc/xet-nghiem-mycoplasma-trong-nuoi-cay-te-bao
23/01/2026
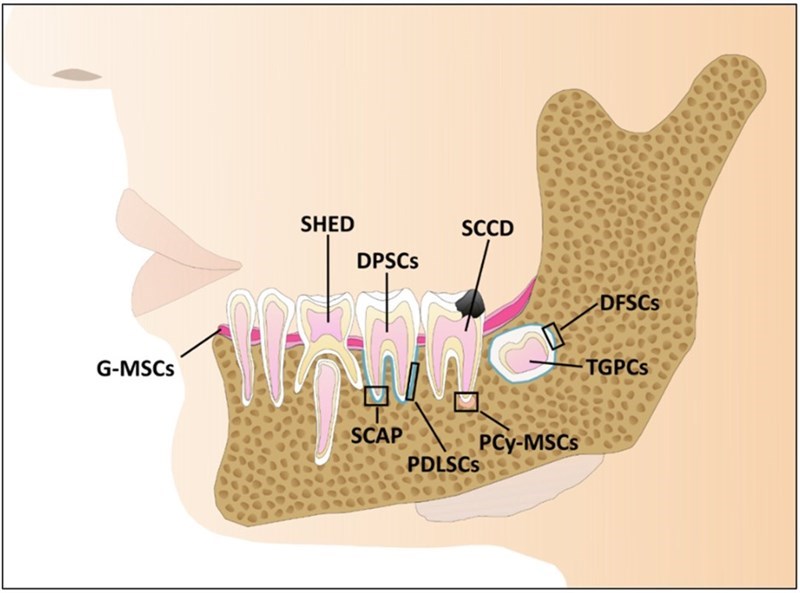
Các loại tế bào gốc nha khoa (Dental Stem Cell): nguồn thu nhận và tiềm năng ứng dụng của chúng
Tế bào gốc trung mô (Mesenchymal stromal/stem cells – MSC) có thể được phân lập từ những mô khác nhau như tủy xương, mô mỡ, dây rốn,… đồng thời có khả năng biệt hóa thành nhiều loại tế bào trong cơ thể như tế bào thần kinh, gan, thận, xương, sụn, mỡ,… Đây là một trong những loại tế bào đang được nghiên cứu và thử nghiệm lâm sàng nhiều nhất hiện nay. Từ những năm 2000, các nhà khoa học đã phân lập được tế bào gốc từ các vị trí khác nhau trong vùng miệng, những loại tế bào gốc nha khoa (Dental Stem Cell – DSC) này đều thể hiện các đặc điểm của MSC, đồng thời có những đặc trưng độc đáo, mang lại tiềm năng lớn trong ứng dụng điều trị các bệnh.
23/01/2026
Tế bào gốc từ tủy răng sữa (SHED)
1. Răng sữa - một nguồn tế bào gốc độc đáo ở trẻ em Răng sữa được mọc từ giai đoạn sớm (khoảng 6 tháng tuổi), đến 3-4 tuổi thì hầu hết trẻ có 20 răng. Răng sữa đóng vai trò quan trọng trong nhai, nói, thẩm mỹ của khuôn mặt. Đến khoảng 5-6 tuổi, răng sữa bắt đầu lung lay và được thay thế bởi răng vĩnh viễn. Thông thường, những chiếc răng này sẽ bị vứt bỏ, tuy nhiên người ta có thể tách được tế bào gốc từ tủy răng sữa. Những tế bào gốc thu nhận từ đây có các đặc điểm của tế bào gốc trung mô – chìa khóa của y học tái tạo hiện nay. 2. Đặc điểm của tế bào gốc từ tủy răng sữa Tế bào gốc từ tủy răng sữa (Stem Cells from Human Exfoliated Deciduous Teeth – SHED) mang những đặc điểm giống tế bào gốc trung mô (Messenchymal Stem Cell – MSC), có thể biệt hóa thành nhiều loại tế bào khác nhau như tế bào thần kinh, mỡ, sụn, xương, cơ, phổi, gan, thận… đồng thời có khả năng điều hòa miễn dịch. Những nghiên cứu gần đây cho thấy SHED có tiềm năng biệt hóa thần kinh và xương cao hơn MSC từ các nguồn khác (mỡ, tủy xương, dây rốn,…) nên được quan tâm nhiều trong điều trị các bệnh lý thần kinh, tái tạo xương và các bệnh nha khoa. SHED có tốc độ tăng sinh cao, khả năng duy trì đặc điểm khi nuôi cấy lâu dài, giữ được các đặc tính sau quá trình bảo quản lạnh lâu dài, do đó có thể được lưu trữ để sử dụng trong tương lai, tương tự như tế bào gốc từ các nguồn khác như máu cuống rốn, dây rốn, mô mỡ,… 3. Tiềm năng ứng dụng của tế bào gốc tủy răng sữa SHED đang được sử dụng trong nhiều thử nghiệm lâm sàng tương tự như MSC, đồng thời những đặc điểm độc đáo giúp SHED được quan trâm nhiều trong các bệnh lý thần kinh và tái tạo xương, các bệnh nha khoa - Nha khoa: tái tạo tủy răng, phục hồi khả năng tưới máu trong ống tủy hoại tử, tái tạo xương răng - Tái tạo xương: sửa chữa khe hở vòm miệng, phục hồi xương hàm - Các bệnh lý thần kinh: điều trị tổn thương não, rối loạn thoái hóa thần kinh, cải thiện chứng đau thần kinh - Điều trị tổn thương ở các cơ quan: phục hồi tổn thương thận do thiếu máu cục bộ, suy gan - Chữa lành vết thương ngoài da - Điều trị bệnh rối loạn chuyển hóa: tiểu đường type 2 - Điều trị bệnh tự miễn: Lupus ban đỏ hệ thống TÀI LIỆU THAM KHẢO Miura M., et al. (2003). SHED: stem cells from human exfoliated deciduous teeth. Proceedings of the National Academy of Sciences, 100(10), 5807-5812. https://doi.org/10.1073/pnas.0937635100 Martinez Saez D., et al. (2016). Stem cells from human exfoliated deciduous teeth: a growing literature. Cells Tissues Organs, 202(5-6), 269-280. https://doi.org/10.1159/000447055 Ko C. S., et al. (2020). Stem cells from human exfoliated deciduous teeth: a concise review. Current Stem Cell Research & Therapy, 15(1), 61-76. https://doi.org/10.2174/1574888X14666191018122109 Naderi F., et al. (2022). The therapeutic effects of stem cells from human exfoliated deciduous teeth on clinical diseases: A narrative review study. American Journal of Stem Cells, 11(2), 28. https://pmc.ncbi.nlm.nih.gov/articles/PMC9123506/ Xem thêm: - Đại cương về tế bào gốc: Tế bào gốc trung mô https://ysinhtebao.com/tbg/te-bao-goc-trung-mo-msc - ISCT nói gì và quy ước thế nào về tế bào gốc trung mô (MSC) https://ysinhtebao.com/quy-dinh/isct-noi-gi-va-quy-uoc-the-nao-ve-msc
23/01/2026
Triển vọng của liệu pháp tế bào gốc trung mô (MSC) trong điều trị đột quỵ thiếu máu cục bộ gây tổn thương não ở trẻ sơ sinh
Đột quỵ thiếu máu cục bộ động mạch trong giai đoạn sinh (Perinatal arterial ischemic stroke – PAIS) là tình trạng cục máu đông xuất hiện ở động mạch não của trẻ ở thời điểm trước, trong hoặc ngay sau khi sinh. Tình trạng này xuất hiện ở khoảng 1/2.300 trẻ sơ sinh đủ tháng sinh ra còn sống, với tỷ lệ tử vong là 3,49/100.000 trẻ. Tình trạng này gây tổn thương não và các khuyết tật thần kinh suốt đời, bao gồm bại não, các vấn đề về hành vi, khó khăn về nhận thức và ngôn ngữ. Điều trị hiện tại cho PAIS tập trung vào kiểm soát co giật và các bệnh nhiễm trùng liên quan, chưa có phương pháp hiệu quả để làm giảm tổn thương não. Gần đây, nhiều bằng chứng cho thấy tế bào gốc trung mô (Mesenchymal stem/stromal cell – MSC) có khả năng cải thiện chức năng ở các trường hợp đột quỵ, cả trên mô hình động vật và ở người trưởng thành, mở ra chiến lược điều trị bệnh lý này bằng phương pháp tế bào gốc.
23/01/2026

Liệu pháp tế bào gốc trung mô điều trị tự kỷ được chấp thuận tại Nhật Bản
Ngày 7 tháng 8 năm 2025, Biostar (một công ty công nghệ tế bào gốc hàng đầu tại Hàn Quốc) đã công bố rằng bệnh viện Trinity Clinic (đơn vị hợp tác của công ty tại Osaka, Nhật Bản) đã được Bộ Y tế, Lao động và Phúc lợi Nhật Bản chấp thuận điều trị chứng tự kỷ bằng liệu pháp tế bào gốc trung mô từ mô mỡ tự thân của Biostar.
23/01/2026
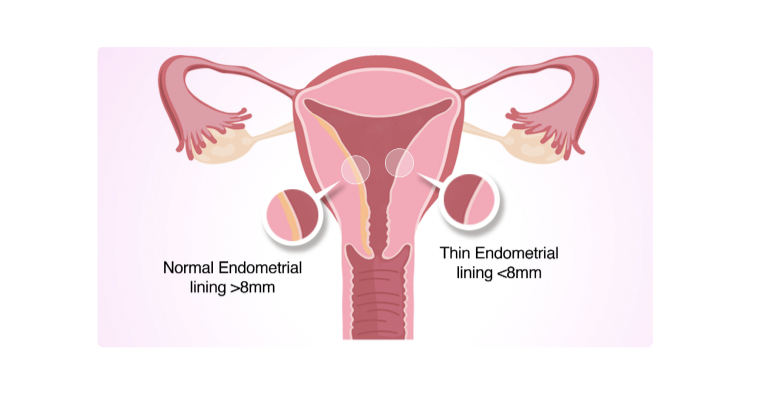
Tăng cường tái tạo niêm mạc tử cung: tiềm năng điều trị của tế bào gốc trung mô dây rốn và dịch ly giải tiểu cầu siêu hoạt hóa
Niêm mạc tử cung (hay nội mạc tử cung) là một lớp tế bào lót bên trong bề mặt tử cung phụ nữ, có độ xốp nhất định để thai nhi làm tổ và lấy chất dinh dưỡng. Niêm mạc tử cung có độ dày mỏng tùy thuộc cơ địa và ảnh hưởng lớn đến quá trình thụ thai. Lớp này quá mỏng ( 20 mm) khiến phôi khó làm tổ. Trong điều trị niêm mạc tử cung mỏng, một số biện pháp khắc phục được chú ý đến bao gồm liệu pháp estrogen, huyết tương giàu tiểu cầu, tế bào gốc,…
23/01/2026
Tế bào gốc trung mô dây rốn (UC-MSC) cho thấy triển vọng chống lại sự lão hóa miễn dịch
Sự lão hóa miễn dịch (Immunosenescence) là sự suy giảm của hệ thống miễn dịch liên quan đến lão hóa, thường dẫn đến phản ứng miễn dịch bị suy yếu và tăng khả năng mắc các bệnh nhiễm trùng, các bệnh tuổi già và nhiều loại bệnh khác. Tuyến ức (nơi tế bào T trưởng thành) và lá lách (quan trọng đối với chức năng miễn dịch) đều bị teo đáng kể theo thời gian, làm giảm chức năng của chúng.
23/01/2026
Điều trị chấn thương tủy sống bằng tế bào gốc trung mô tự thân: kết quả thử nghiệm lâm sàng tại Nhật Bản
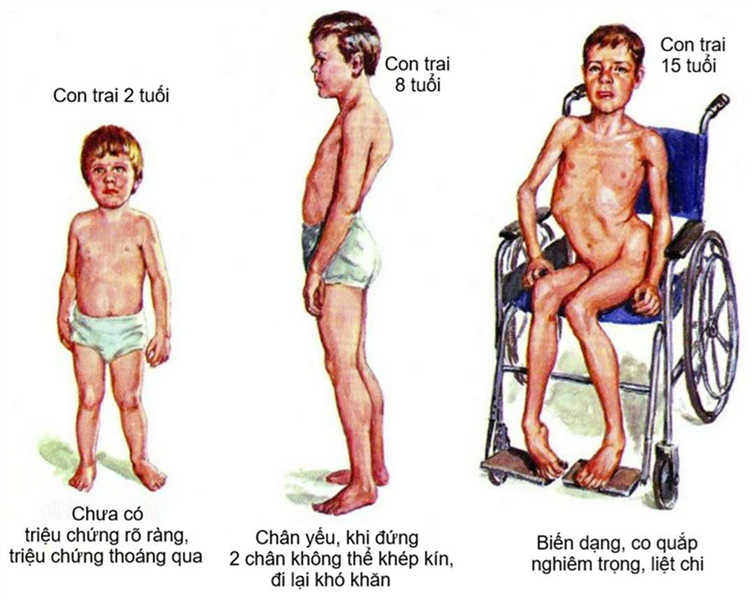
Tủy sống bao gồm dây thần kinh và các tế bào trong ống tủy chạy dọc phía sau lưng từ não đến gần mông, giúp nó thực hiện chức năng gửi tín hiệu thần kinh từ não đến các bộ phận trên cơ thể. Chấn thương tủy sống dẫn đến các tín hiệu thần kinh có thể không được dẫn truyền, dẫn đến mất cảm giác và mất khả năng vận động ở vị trí dưới vùng tổn thương. Các nhà khoa học tại Đại học Yale (Hoa Kỳ) kết hợp cùng Đại học Sapporo (Nhật Bản) đã đánh giá tính khả thi, độ an toàn và hiệu quả điều trị cho bệnh nhân chấn thương tủy sống bằng tế bào gốc trung mô (MSC) tự thân từ tủy xương. Trong thử nghiệm lâm sàng pha II này, 13 bệnh nhân chấn thương tủy sống được thu thập tủy xương, nuôi cấy tăng sinh MSC và truyền theo đường tĩnh mạch. Sau 6 tháng điều trị, 12/13 bệnh nhân đã có cải thiện chức năng thần kinh, được đánh giá theo thang điểm suy giảm của Hiệp hội Chấn thương cột sống Hoa Kỳ (the American Spinal Injury Association Impairment Scale – ASIA). Theo Tiêu chuẩn Quốc tế về Phân loại Chức năng và Thần kinh của Tủy sống (International Standards for Neurological and Functional Classification of Spinal Cord – ISCSCI-92) và Phép đo Độc lập Tủy sống (Spinal Cord Independence Measure – SCIM-III) về khả năng sinh hoạt hàng ngày, cả 13/13 bệnh nhân đều có sự cải thiện chức năng. Một trường hợp điều trị chấn thương tủy sống bằng tế bào gốc trung mô (MSC) tự thân trong thử nghiệm. Bệnh nhân nữ, 56 tuổi, chấn thương do đập trán vào tường và cổ bị ngửa ra sau quá mức khi bất tỉnh. Bệnh nhân nằm liệt giường trước khi truyền tế bào gốc (điểm ASIA là A). Sau 49 ngày gặp chấn thương tủy sống và điều trị, bệnh nhân được ghép 102 triệu MSC tủy xương tự thân, và nhanh chóng cải thiện chức năng vận động. Điểm SCIM-III được cải thiện chỉ sau 2 tuần truyền MSC, sau đó là sự cải thiện dần về điểm vận động và cảm giác. Sau 181 ngày truyền MSC, điểm ASIA đã cải thiện từ A sang C. Những thành công này cho thấy khá rõ khả năng hồi phục chức năng thần kinh sau chấn thương tủy sống bằng cách sử dụng liệu pháp tế bào gốc trung mô. --------- TÀI LIỆU THAM KHẢO Honmou O., et al. (2021). Intravenous infusion of auto serum-expanded autologous mesenchymal stem cells in spinal cord injury patients: 13 case series. Clinical Neurology and Neurosurgery, 203, 106565.
23/01/2026
Các dấu ấn sinh học để dự đoán khả năng đáp ứng với liệu pháp TIL
Liệu pháp tế bào lympho thâm nhiễm khối u (Tumor Infiltrating Lymphocyte - TIL) là phương pháp điều trị ung thư bằng cách phân lập các tế bào lympho T từ khối u của bệnh nhân, nuôi cấy tăng sinh, sau đó truyền trở lại cơ thể bệnh nhân. Liệu pháp TIL đã được chứng minh hiệu quả trong điều trị ung thư hắc tố (trong đó sản phẩm AMTAGVI (Lifileucel) đã được FDA phê duyệt), bên cạnh những tác dụng tích cực trên bệnh nhân ung thư cổ tử cung, đại trực tràng, đường mật,…
23/01/2026
Liệu pháp TIL trong điều trị u đặc: Triển vọng và thách thức
Liệu pháp tế bào lympho thâm nhiễm khối u (Tumor Infiltrating Lymphocyte - TIL) là một loại liệu pháp miễn dịch sử dụng các tế bào lympho T được lấy từ khối u của bệnh nhân, nuôi cấy và nhân lên trong phòng thí nghiệm, sau đó truyền trở lại cơ thể bệnh nhân để tấn công các tế bào ung thư. Hiện nay, nhiều trung tâm ung thư lâm sàng trên thế giới triển khai liệu pháp TIL và đã cho thấy những kết quả ấn tượng trong điều trị nhiều loại u đặc khác nhau. 1. Dữ liệu lâm sàng về liệu pháp TIL trong điều trị u đặc Tháng 02/2024, Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (U.S. Food and Drug Administration – US FDA) đã chấp thuận sản phẩm AMTAGVI (Lifileucel) của Iovance Biotherapeutics trong điều trị ung thư hắc tố – liệu pháp TIL đầu tiên và duy nhất tính đến nay được FDA phê duyệt. Việc chấp thuận này dựa trên những kết quả thử nghiệm lâm sàng trên hơn 70 bệnh nhân, trong đó tỷ lệ kiểm soát bệnh là 80%, kích thước khối u giảm ở 1/3 số bệnh nhân, trong đó có một số bệnh nhân đáp ứng hoàn toàn (không còn u), khoảng 40% bệnh nhân đáp ứng liệu pháp không thấy bệnh tiến triển sau 1 năm. Ngoài Lifileucel đã được chấp thuận, có rất nhiều sản phẩm liệu pháp TIL đang được thử nghiệm lâm sàng, chủ yếu để điều trị bước hai cho các loại u đặc. U hắc tố vẫn là loại ung thư chiếm hầu hết các thử nghiệm, với những kết quả rất khả quan về tỷ lệ đáp ứng, ngoài ra TIL có lợi ích lâm sàng ấn tượng với bệnh nhân ung thư cổ tử cung, có hiệu quả ban đầu trong ung thư phối không tế bào nhỏ, đại trực tràng, đường mật và vú. 2. Quy trình thực hiện liệu pháp TIL trong điều trị u đặc - Phẫu thuật cắt khối u từ bệnh nhân - Phân lập tế bào lympho T từ mô khối u - Nuôi cấy tăng sinh TIL, sàng lọc TIL có hoạt tính - Chuẩn bị bệnh nhân: làm suy giảm lympho mà không phá hủy tủy bằng cách hóa trị hoặc xạ trị toàn thân - Truyền các tế bào TIL cho bệnh nhân, kích thích TIL khi vào cơ thể bằng Interleukin-2 (IL-2) 3. Các liệu pháp kết hợp với TIL trong điều trị u đặc - Chất ức chế điểm kiểm soát miễn dịch: Ở bệnh nhân ung thư, sự tăng cường biểu hiện các điểm kiểm soát miễn dịch (PD-1/PD-L1, CTLA-4, LAG-3,…) làm ức chế chức năng của tế bào T. Việc sử dụng TIL kết hợp các chất ức chế PD-1/PD-L1 và CTLA-4 làm tăng hiệu quả điều trị. - Chất ức chế BRAF: Đột biến BRAF là đột biến phổ biến nhất gây ra hoạt hóa quá mức con đường truyền tin tế bào MAPK, làm tế bào tăng sinh mất kiểm soát, có thể gây cơ chế thoát miễn dịch. Chất ức chế BRAF như vemurafenib có thể làm giảm tín hiệu ức chế miễn dịch liên quan, giảm các tế bào ức chế miễn dịch, tạo điều kiện cho sự xâm nhập của tế bào lympho và tăng cường hiệu quả của liệu pháp TIL. - Vaccine tế bào tua (DC): Vaccine DC có thể gây các phản ứng miễn dịch, kích hoạt và tăng số lượng TIL. Sự kết hợp của nó với TIL đang được đánh giá. - Virus tiêu ung thư: Virus có thể chống lại tình trạng ức chế miễn dịch của khối u bằng cách sản xuất các cytokine thúc đẩy tác dụng chống khối u của TIL. Một thử nghiệm cho thấy TIL kết hợp adenovirus trong điều trị u hắc tố di căn đã mang lại những lợi ích lâm sàng đáng khích lệ 4. Những hạn chế của liệu pháp TIL và triển vọng trong tương lai Liệu pháp TIL có một số ưu điểm so với các liệu pháp tế bào miễn dịch khác như: TIL mang nhiều thụ thể tế bào T (T Cell Receptor – TCR) nên có thể tác động lên phổ rộng kháng nguyên đặc hiệu khối u, giúp hiệu quả hơn trong việc đáp ứng với tính không đồng nhất của khối u; TIL dễ dàng định vị trong mô khối u sau khi truyền; có độc tính thấp do lấy tự thân mà chưa qua chỉnh sửa gen. Tuy nhiên, liệu pháp TIL cũng có những hạn chế: không phải tách được TIL từ tất cả các khối u, do tế bào T hiệu lực có hoạt tính kháng u nhiều khi không có mặt trong khối u; việc lựa chọn TIL có hoạt tính gặp khó khăn đối với những khối u mang kháng nguyên đặc mới; vi môi trường khối u ức chế miễn dịch làm giảm mạnh các tế bào T độc thâm nhiễm khối u; TIL có thời gian sống sót ngắn trong cơ thể sau khi truyền. Những hạn chế này đang được các nhà khoa học đẩy lùi dần với nhiều cách thức khác nhau. Hiện tại, nhiều nghiên cứu và thử nghiệm lâm sàng vẫn đang tìm cách xây dựng các chiến lược để khắc phục những hạn chế trên, đẩy mạnh hiệu quả của TIL, đồng thời khám phá những liệu pháp kết hợp thay thế. --------- TÀI LIỆU THAM KHẢO 1. Zhao Y., et al. (2022). Tumor infiltrating lymphocyte (TIL) therapy for solid tumor treatment: progressions and challenges. Cancers, 14(17), 4160. DOI: 10.3390/cancers14174160. 2. https://www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-accelerated-approval-lifileucel-unresectable-or-metastatic-melanoma
23/01/2026