LIỆU PHÁP TẾ BÀO
Thuật ngữ liệu pháp tế bào (cell therapy) dùng để chỉ việc chuyển vật liệu tế bào vào bệnh nhân cho mục đích điều trị. Liệu pháp tế bào bao gồm nhiều lĩnh vực điều trị như liệu pháp tế bào gốc, liệu pháp tế bào miễn dịch, liệu pháp tế bào cải biến gen,...
Liệu pháp tế bào KIR-CAR T mô phỏng tế bào NK và triển vọng trong điều trị ung thư dạng u đặc
Dữ liệu thử nghiệm lâm sàng giai đoạn I cho thấy liệu pháp mới KIR-CAR T thể hiện tính an toàn và đặc biệt là hiệu quả đầy triển vọng trong điều trị ung thư buồng trứng, ung thư đường mật và u trung biểu mô.
24/04/2026

Chỉnh sửa vùng khởi động của gen HBG1 và HBG2 trên tế bào gốc tạo máu để điều trị bệnh thiếu máu hồng cầu hình liềm
Thử nghiệm lâm sàng RUBY (https://clinicaltrials.gov/study/NCT04853576) cho thấy phương pháp điều trị đầy hứa hẹn bằng cách chỉnh sửa gen trên tế bào gốc tạo máu đối với bệnh hồng cầu hình liềm, một rối loạn di truyền có rất ít lựa chọn chữa khỏi.
06/04/2026

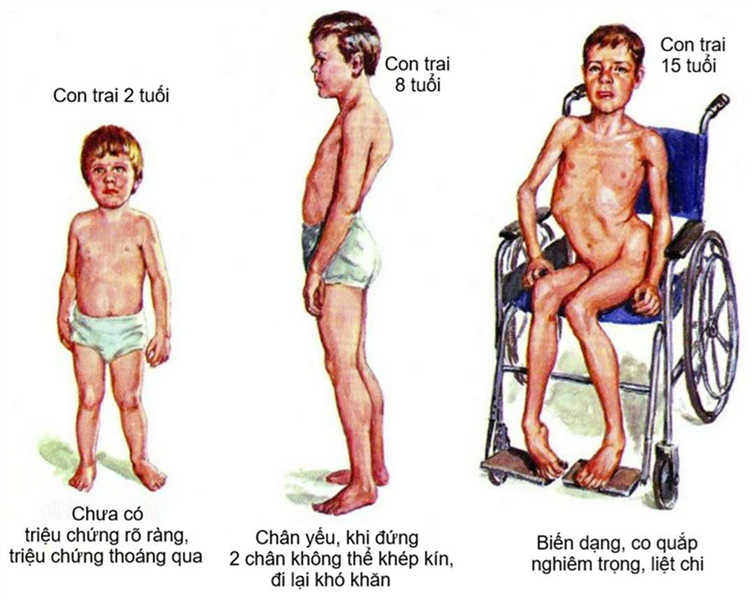
Marne-Cel - liệu pháp tế bào gốc chỉnh sửa gen được FDA phê duyệt nhanh để điều trị hội chứng thiếu hụt sự bám dính bạch cầu loại I (LAD-I)
Ngày 26/03/2026, FDA đã phê duyệt marnetegragene autotemcel (marne-cel, tên thương mại: Kresladi, sản phẩm của hãng Rocket Pharmaceuticals) để điều trị hội chứng thiếu hụt sự bám dính bạch cầu loại I nghiêm trọng ở bệnh nhân nhi không thể ghép tế bào gốc tạo máu đồng loại.
30/03/2026
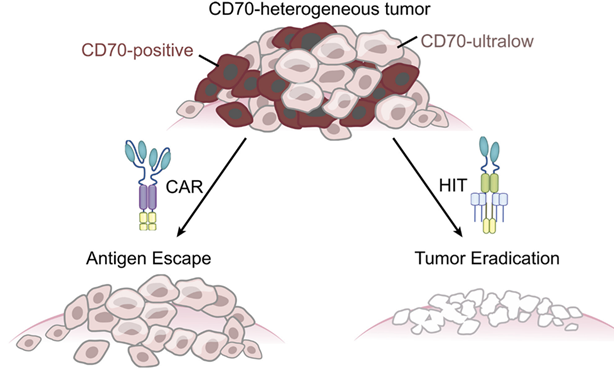
Liệu pháp CAR-T có độ nhạy cao với CD70 mang lại triển vọng loại bỏ hoàn toàn tế bào ung thư trong khối u đặc
Liệu pháp CAR-T đã chứng minh hiệu quả trong điều trị nhiều bệnh huyết học ác tính, nhưng lại gặp rất nhiều hạn chế với các khối u đặc. Một nghiên cứu một công bố trên tạp chí Science cho thấy liệu pháp CAR-T có độ nhạy cao hướng đích CD70 có thể loại bỏ hoàn toàn tế bào ung thư thận, tuyến tụy và buồng trứng ở chuột.
23/03/2026
Liệu pháp tế bào miễn dịch mang cấu trúc CAR: so sánh CAR-T, CAR-NK và CAR-M
Cấu trúc CAR có thể được thiết kế cho nhiều loại tế bào miễn dịch khác nhau, như tế bào T (CAR-T), tế bào giết tự nhiên (CAR-NK), đại thực bào (CAR-M) - mỗi loại đều có những ưu điểm để mang lại tiềm năng điều trị, và có những rào cản cần vượt qua để ứng dụng lâm sàng.
16/03/2026
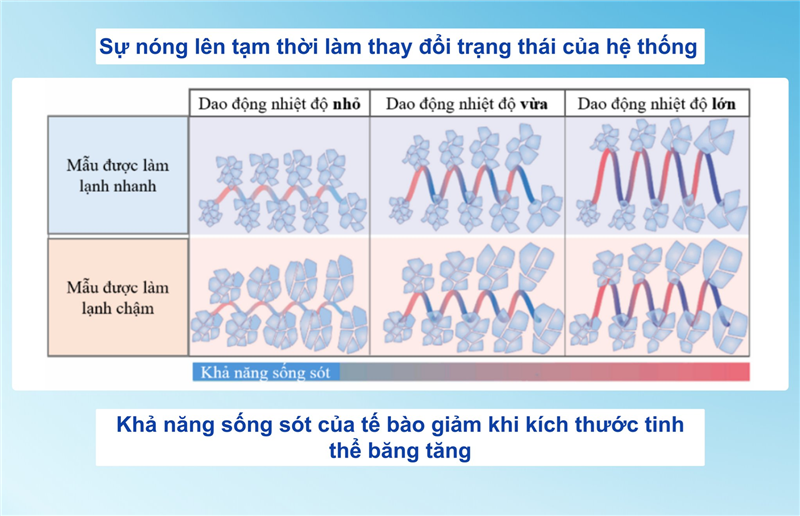
Sự cố nóng lên tạm thời trong bảo quản mẫu đông lạnh
Sự cố nóng lên tạm thời xảy ra khi mẫu được bảo quản lạnh bị tiếp xúc với nhiệt độ cao vượt mức kiểm soát trong khoảng thời gian ngắn. Mặc dù có vẻ không đáng kể, nhưng ngay cả việc tăng nhiệt độ nhỏ cũng có thể khởi động một chuỗi phản ứng sinh học bên trong tế bào.
09/03/2026
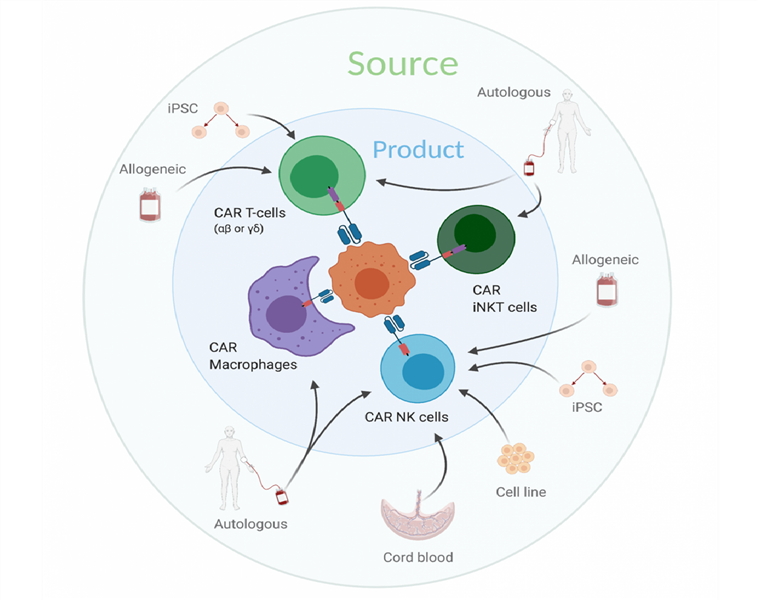
Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh (P4)
Phần 4: Liệu pháp CAR cho các loại tế bào miễn dịch bẩm sinh và những chiến lược kết hợp khi sử dụng lâm sàng
05/03/2026
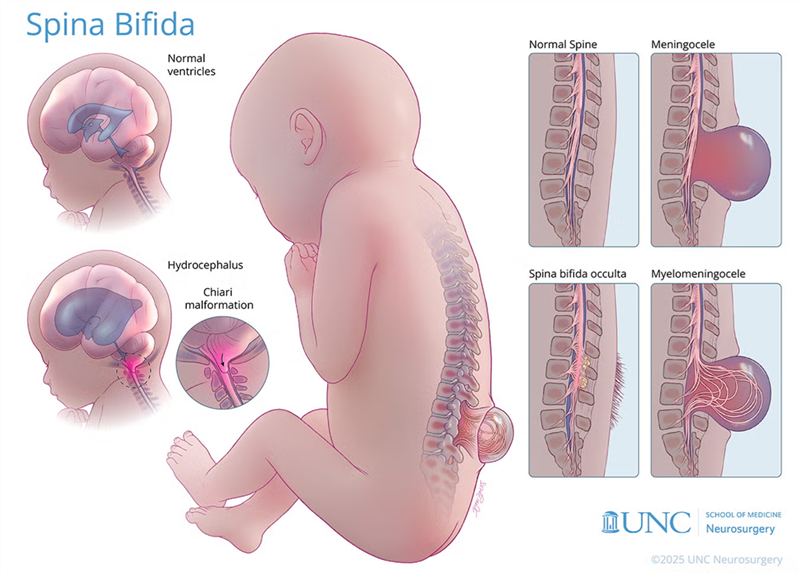
Liệu pháp tế bào gốc trung mô (MSC) an toàn và khả thi trong hỗ trợ điều trị tật nứt đốt sống ở thai nhi
Một thử nghiệm lâm sàng giai đoạn I cho thấy việc kết hợp liệu pháp tế bào gốc trung mô với phẫu thuật bào thai là phương pháp an toàn và đầy hứa hẹn để điều trị thoát vị màng tủy, một dạng nghiêm trọng của tật nứt đốt sống.
02/03/2026
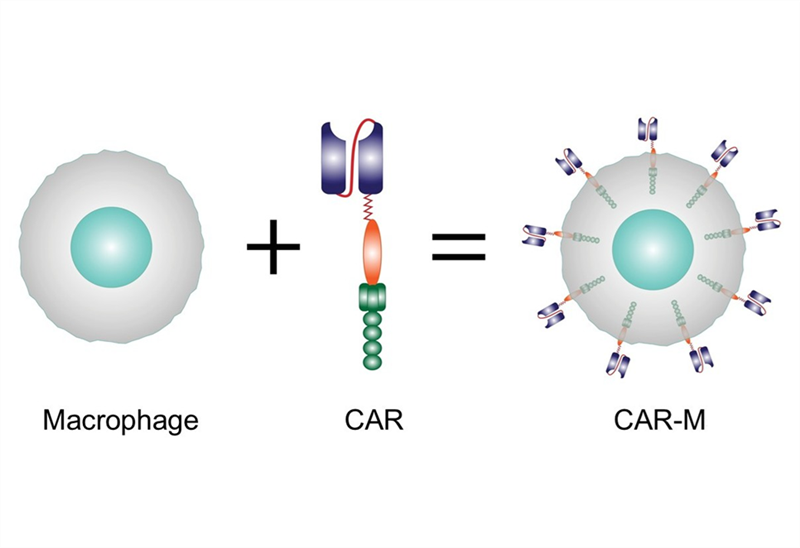
Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh (P3)
Phần 3. Liệu pháp CAR-M – giải pháp đến từ các đại thực bào
26/02/2026

Cập nhật 2025 về các liệu pháp tế bào gốc đa tiềm năng trong các thử nghiệm lâm sàng
Tế bào gốc đa tiềm năng (Pluripotent Stem Cell – PSC) là những tế bào có khả năng biệt hóa thành tất cả các loại tế bào có trong cơ thể, nhưng không biệt hóa được thành các tế bào thuộc phần phụ ngoài phôi (nhau thai, cuống rốn) nên không phát triển được thành cơ thể hoàn chỉnh. Những loại tế bào gốc đa tiềm năng được quan tâm nhiều nhất bao gồm tế bào gốc phôi (Embryonic Stem Cell – ESC) và tế bào gốc đa tiềm năng cảm ứng (induced Pluripotent Stem Cell – iPSC). Xem thêm về tế bào gốc đa tiềm năng tại https://ysinhtebao.com/tbg/tbg-da-tiem-nang. Các hướng tiếp cận tế bào gốc đa tiềm năng người (hPSC) để tạo sản phẩm thử nghiệm lâm sàng. Hai loại tế bào được sử dụng trong các ứng dụng là tế bào gốc phôi (hESC) thu nhận từ nút phôi (inner cell mass) của túi phôi (blastocyst), và tế bào gốc đa tiềm năng cảm ứng (iPSC) được tái lập trình (reprogramming) từ tế bào soma. Nguồn: Huang J., et al. (2021). Human pluripotent stem cell-derived cardiac cells: application in disease modeling, cell therapy, and drug discovery. Frontiers in Cell and Developmental Biology, 9, 655161. https://doi.org/10.3389/fcell.2021.655161 PSC ở người lần đầu tiên được thu nhận năm 1998 với việc Thompson và cộng sự phân lập thành công ESC, mở ra cơ hội sử dụng nguồn tế bào gốc có tiềm năng không hạn chế để ứng dụng trong trị liệu. Những tiến bộ trong kỹ thuật về việc tạo phôi chuyển nhân, đặc biệt là tái lập trình soma tạo nên iPSC năm 2007 giúp các nhà khoa học có thể tạo nên PSC tự thân để tiến gần hơn đến ứng dụng điều trị. Tính đến tháng 12 năm 2024, đã có 115 thử nghiệm lâm sàng tại 19 quốc gia được cơ quan quản lý chấp thuận, thực hiện trên hơn 1.200 bệnh nhân, sử dụng 83 sản phẩm PSC với 34 chỉ định khác nhau. Trong giai đoạn đầu (từ sau năm 2010), các sản phẩm điều trị các bệnh về mắt và hệ thần kinh trung ương chiếm đa số, tuy nhiên hiện nay các sản phẩm chuyển dịch phần nhiều sang tế bào miễn dịch điều trị ung thư (NK, T, NKT, DC từ PSC), các bệnh tim mạch và nội tiết. Các chiến lược chính để tránh tình trạng đào thải miễn dịch ở bệnh nhân: (1) ghép tế bào tự thân của chính bệnh nhân, (2) sử dụng các ngân hàng iPSC đã được xác định phù hợp kiểu gen HLA, (3) chỉnh sửa gen ở các dòng tế bào để có thể tránh sự nhận diện của tế bào miễn dịch của vật chủ và (4) bao bọc bảo vệ các tế bào được ghép để bảo vệ vật lý tránh khỏi các tế bào miễn dịch ở vật chủ. Chiến lược chỉnh sửa gen để giảm đáp ứng miễn dịch là hướng được sử dụng nhiều nhất, đặc biệt khi công nghệ cải biến di truyền CRISPR đang phát triển mạnh. Ngược lại, hướng đi tiềm năng ban đầu là ghép tế bào tự thân, thực tế chỉ được thực hiện trên 11 bệnh nhân ở 9 thử nghiệm khác nhau. Tổng quan về các thử nghiệm lâm sàng sử dụng tế bào gốc đa tiềm năng (hPSC). (A) Số lượng thử nghiệm được khởi xướng mỗi năm (từ 2010) theo loại sản phẩm (số liệu năm 2025 chưa đầy đủ, dựa trên các thử nghiệm hiện đã được chấp thuận). (B) Tổng số thử nghiệm được khởi xướng từ năm 2010 theo loại sản phẩm. (C) Số lượng thử nghiệm được khởi xướng mỗi năm theo nguồn tế bào được sử dụng. (D) Tỷ lệ các thử nghiệm theo nguồn tế bào. (E) Tỷ lệ các giai đoạn thử nghiệm lâm sàng khác nhau. (F) Số lượng các loại sản phẩm khác nhau được chấp thuận cho thử nghiệm lâm sàng. (G) Số lượng bệnh nhân được dùng liều tổng cộng với từng loại sản phẩm. (H) Các loại tế bào sản phẩm (hình tròn trong) được áp dụng cho mỗi chỉ định bệnh (hình tròn ngoài) cho các thử nghiệm sản phẩm về mắt, hệ thần kinh trung ương và miễn dịch. (I) Liều trung bình được dùng cho mỗi bệnh nhân đối với các loại sản phẩm khác nhau. Từ viết tắt: AMD – thoái hóa điểm vàng do tuổi tác; SMD – thoái hóa điểm vàng Stargardt; RP – viêm võng mạc sắc tố; RID – bệnh suy giảm RPE; LSCD – suy giảm tế bào gốc rìa giác mạc; BK – bệnh giác mạc bóng nước; PPD – bệnh thụ thể ánh sáng nguyên phát; DA – dopamine; PD – bệnh Parkinson; SCI – chấn thương tủy sống; HD – bệnh Huntington; NSC – tế bào gốc thần kinh; OPC – tế bào tiền thân của oligodendrocyte; ALS – xơ cứng teo cơ một bên, SLE – lupus ban đỏ hệ thống; NSCLC – ung thư phổi không tế bào nhỏ. Nguồn: Kirkeby A., Main H., and Carpenter M. (2025). Pluripotent stem-cell-derived therapies in clinical trial: A 2025 update. Cell stem cell, 32(1), 10-37 Phần lớn các thử nghiệm này là thử nghiệm giai đoạn I/IIa, được thiết kế để kiểm tra độ an toàn và tính khả thi, chỉ một số ít thử nghiệm đánh giá hiệu quả. Cho đến nay không cho thấy bất kỳ mối lo ngại nào về tính an toàn, ngay cả khi được theo dõi tới 10 năm sau khi ghép. Điều quan trọng nhất để đảm bảo tính an toàn khi thử nghiệm liệu pháp PSC là quy trình sản xuất, kiểm soát chất lượng và phân phối đúng cách các sản phẩm dưới sự giám sát của cơ quan quản lý. Việc đưa các sản phẩm PSC vào thử nghiệm và ứng dụng lâm sàng gặp những rào cản về công nghệ và quy định: (1) cần nhiều thập kỷ nghiên cứu đánh giá về đặc điểm PSC trong cơ thể, nhất là khả năng biệt hóa thành tế bào mong muốn với hiệu suất cao, tránh biệt hóa thành loại tế bào khác có thể gây nguy hiểm, (2) cần nhiều thời gian và chi phí để phát triển các mô hình động vật mang bệnh để nghiên cứu lâu dài, (3) quy trình sản xuất sản phẩm PSC phức tạp, cần thực hiện theo tiêu chuẩn Thực hành Sản xuất Tốt (GMP), tuy nhiên trên thị trường chưa có đầy đủ phương tiện đánh giá chất lượng sản phẩm, (4) sự cần thiết phải nghiên cứu về độc tính, phân bố sinh học và khả năng gây ung thư trong thời gian dài theo thực hành phòng thí nghiệm tốt (GLP), đòi hỏi phải đào tạo lại đội ngũ nhân viên tại các tổ chức nghiên cứu, (5) chưa có các hướng dẫn quản lý sản phẩm hPSC và vẫn đang gặp thách thức trong việc ban hành hướng dẫn do thiếu tính nhất quán giữa các khu vực pháp lý. Con đường đi tiếp theo sẽ là thiết kế các thử nghiệm giai đoạn II/III để đánh giá hiệu quả của sản phẩm PSC, song song với việc mở rộng quy mô sản xuất tế bào cũng như xác định chiến lược tránh đào thải miễn dịch một cách hiệu quả nhất có thể. TÀI LIỆU THAM KHẢO Kirkeby A., Main H., and Carpenter M. (2025). Pluripotent stem-cell-derived therapies in clinical trial: A 2025 update. Cell stem cell, 32(1), 10-37. https://doi.org/10.1016/j.stem.2024.12.005
22/02/2026

Các nhà lập pháp bang Wyoming (Hoa Kỳ) tìm cách bỏ qua FDA trong việc phê duyệt các phương pháp điều trị tế bào gốc
Ngày 13/02/2026, các nhà lập pháp bang Wyoming đã thông qua Đạo luật Tự do Tế bào gốc.
19/02/2026
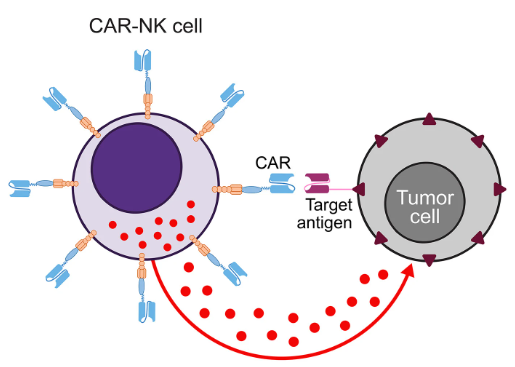
Liệu pháp CAR với các tế bào thuộc hệ miễn dịch bẩm sinh (P2)
Phần 2. Liệu pháp CAR-NK – hiện trạng, thách thức và triển vọng tương lai
15/02/2026